2015-2016學年河北省衡水市武邑中學高一(下)化學暑假作業(23)
發布:2024/4/20 14:35:0
一、選擇題(共12小題、共0分)
-
1.下列有關化學用語表示正確的是( )
A.過氧化鈉的電子式: 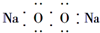
B.碳正離子 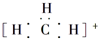 中質子數與電子數的比值為3:2
中質子數與電子數的比值為3:2C.硫離子的結構示意圖: 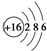
D.質子數為35、中子數為45的溴原子: Br8035組卷:17引用:2難度:0.9 -
2.正確掌握化學用語是學好化學的基礎,下列有關表述正確的是( )
A.H2、D2互為同位素 B.氨分子中的化學鍵都為非極性共價鍵 C.NH4Cl的電子式: 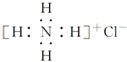
D.S2-的結構示意圖: 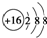 組卷:29引用:3難度:0.9
組卷:29引用:3難度:0.9 -
3.中國科學技術名詞審定委員會已確定第116號元素Lv的名稱為鉝,質量數293.關于
Lv的敘述錯誤的是( )293116A.原子序數116 B.中子數177 C.核外電子數116 D.相對原子質量293 組卷:481引用:54難度:0.9 -
4.下列說法正確的是( )
A.As的原子半徑大于P,AsH3比PH3的熱穩定性強 B.P的非金屬性強于Si,H3PO4比H2SiO3的酸性強 C.Al2O3和MgO均可與NaOH溶液反應 D.SO2和SO3混合氣體通入Ba(NO3)2溶液可得到BaSO3和BaSO4 組卷:12引用:2難度:0.9 -
5.下列離子中半徑最大的是( )
A.Na+ B.Mg2+ C.O2- D.F- 組卷:1971引用:53難度:0.9
二、解答題(共5小題,滿分55分)
-
16.磷酸鐵鋰動力電池的正極與負極中間是聚合物的隔膜隔開的,鋰離子可以通過.該電池的總反應式為:Li1-xFePO4+LixC6═C6+LiFePO4 (注:LixC6是單質Li附在碳電極上的一種形式)
(1)磷酸鐵鋰電池放電時,負極反應式為.
(2)若用該電池電解精煉銅,陰極質量增重19.2g時,則電池中通過聚合物隔膜的Li+數目為.
(3)以該電池為電源,用Fe2O3為陽極,石墨為陰極,NaOH溶液為電解質溶液制備高鐵酸鈉(Na2FeO4),寫出陽極的電極反應式.
(4)以該電池為電源,用惰性電極電解2L硫酸銅和氯化鈉的混合溶液,若兩極均產生0.14mol氣體,電路中共有0.4mol的電子轉移,則電解后溶液的C(OH-)為.組卷:23引用:2難度:0.3 -
17.運用化學反應原理研究碳、氮等單質和化合物的反應有重要意義。
(1)有科學家提出可利用FeO吸收和利用CO2,相關熱化學方程式如下:
6FeO(s)+CO2(g)═2Fe3O4(s)+C(s)△H=-76.0kJ?mol一1
①上述反應中每生成1mol Fe3O4,轉移電子的物質的量為mol。
②已知:C(s)+2H2O(g)═CO2 (g)+2H2(g)△H=+113.4kJ?mol一1,
則反應:3FeO(s)+H2O (g)═Fe3O4 (s)+H2 (g)的△H=。
(2)工業生產可以用NH3(g)與CO2(g)經兩步反應生成尿素[CO(NH2)2],兩步反應的能量變化示意圖如下: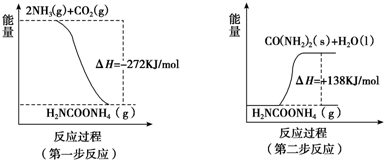
則NH3(g)與CO2(g)反應生成尿素的熱化學方程式為。
(3)氨氣在純氧中燃燒,生成一種單質和水,科學家利用此原理,設計成氨氣一氧氣燃料電池,則通入氨氣的電極是(填“正極”或“負極”);堿性條件下,該電極發生反應的電極反應式為。
(4)華盛頓大學的研究人員研究出一種方法,可實現水泥生產時CO2零排放,其基本原理如圖所示: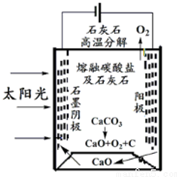
①上述生產過程的能量轉化方式是。
a、電能轉化為化學能
b、太陽能轉化為電能
c、太陽能轉化為化學能
d、化學能轉化為電能
②上述電解反應在溫度小于 900℃時進行,碳酸鈣先分解為CaO和CO2,電解質為熔融碳酸鈉,陰極反應式為3CO2+4e-═C+2CO32-,則陽極的電極反應式為。組卷:11引用:2難度:0.6


