2021-2022學年浙江省杭州市“六縣九校”聯盟高二(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本大題共25小題,每小題只有一個正確選項,每題2分,共50分)
-
1.水溶液呈堿性的鹽是( )
A.Na2O B.CH3COONa C.NH4Cl D.NH3?H2O 組卷:7引用:1難度:0.8 -
2.下列物質屬于電解質的是( )
A.CCl4 B.SO2 C.CH3COOH D.CH2=CH2 組卷:2引用:1難度:0.7 -
3.科學家在20℃時,將水置于足夠強的電場中,水分子瞬間凝固成“暖冰”,對“暖冰”與其它物質比較正確的是( )
A.與Na2O晶體類型相同 B.與SiO2晶體類型相同 C.與H2S化學鍵類型不相同 D.與普通的冰化學性質相同 組卷:16引用:2難度:0.6 -
4.下列物質對應的化學式不正確的是( )
A.氯仿:CHCl3 B.水晶:SiO2 C.鐵紅:Fe2O3 D.漂白粉的有效成分:CaCl2 組卷:1引用:1難度:0.7 -
5.下列化學用語表示正確的是( )
A.中子數為20的K原子: 2019KB.基態C原子的軌道表示式: 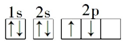
C.Fe2+結構示意圖: 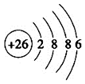
D.N原子2p能級電子云輪廓圖: 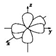 組卷:7引用:1難度:0.7
組卷:7引用:1難度:0.7 -
6.下列說法不正確的是( )
A.汽油和柴油屬于油脂 B.芳香族化合物一定含有苯環 C.氨基酸都含有氨基和羧基 D.葡萄糖能發生銀鏡反應是因為含有醛基 組卷:19引用:1難度:0.7 -
7.用VSEPR模型預測下列分子或離子的空間結構,其中正確的是( )
A.CHCl3為正四面體形 B.CS2為直線形 C.BF3為三角錐形 D. 為平面三角形SO2-3組卷:6引用:2難度:0.6 -
8.下列說法不正確的是( )
A.還原鐵粉常用作食品干燥劑 B.硬鋁(一種鋁合金)密度較小、強度高,可用于制造飛機和宇宙飛船部件 C.氯氣、臭氧、二氧化氯都可用于飲用水的消毒 D.過氧化鈉可在呼吸面具或潛水艇中作為供氧劑 組卷:6引用:2難度:0.7 -
9.在有機物分子中,若一個碳原子連接四個不同的原子或原子團,該碳原子稱為手性碳原子,以*C表示。具有手性碳原子的有機物具有光學活性。下列分子中有光學活性的是( )
A.丙二酸:HOOCCHH2COOH B.甘油:CH2(OH)CH(OH)CH2OH C.核糖:CH2(OH)CH(OH)CH(OH)CH(OH)CHO D.對羥基苯甲酸( 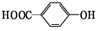 )組卷:19引用:1難度:0.8
)組卷:19引用:1難度:0.8 -
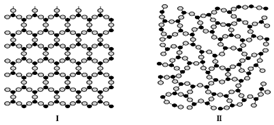 10.如圖是某固體的微觀結構示意圖,請認真觀察兩圖,判斷下列說法正確的是( )
10.如圖是某固體的微觀結構示意圖,請認真觀察兩圖,判斷下列說法正確的是( )A.兩種物質在一定條件下都會自動形成有規則的幾何外形的晶體 B.Ⅰ形成的固體的許多物理性質有各向異性 C.Ⅱ形成的固體有固定的熔點 D.二者的X射線衍射圖譜是相同的 組卷:97引用:3難度:0.7
二.非選擇題(共有5個小題,共50分)
-
29.工業上,以煤炭為原料,通入一定比例的空氣和水蒸氣,經過系列反應可以得到滿足不同需求的原料氣。
請回答:
(1)在C和O2的反應體系中:
反應1.C(s)+O2(g)=CO2(g)ΔH1=-394kJ?mol-1
反應2.2CO(g)+O2(g)=2CO2(g)ΔH2=-566kJ?mol-1
反應3.2C(s)+O2(g)=2CO(g)ΔH3
①ΔH3=。
②設y=ΔH-TΔS,反應1、2和3的y隨溫度的變化關系如圖1所示。圖中的線條b對應的是反應。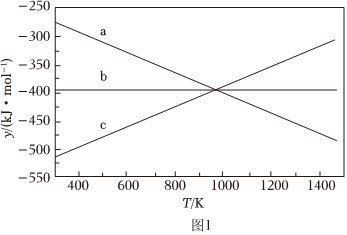
③一定壓強下,隨著溫度的升高,氣體中CO2與CO的物質的量之比。
A.不變
B.增大
C.減小
D.無法判斷
(2)一氧化碳變換反應:CO(g)+H2O(g)═CO2(g)+H2(g)ΔH=-41kJ?mol-1。
①一定溫度下,反應后測得各組分的平衡壓強(已知溫度相同時氣體壓強之比等于濃度之比):p(CO)=0.4MPa、p(H2O)=0.2MPa、p(CO2)=0.8MPa和p(H2)=0.8MPa,則反應的平衡常數K的數值為。
②維持與題①相同的溫度和總壓,提高水蒸氣的比例,使CO的平衡轉化率提高到80%,則原料氣中水蒸氣和CO的物質的量之比為。
③生產過程中,為了提高變換反應的速率,下列措施中不合適的是。
A.反應溫度愈高愈好
B.適當提高反應物壓強
C.選擇合適的催化劑
D.通入一定量的氮氣
④以固體催化劑M催化變換反應,反應歷程分兩步完成,能量-反應過程如圖2所示,寫出步驟Ⅱ的反應方程式。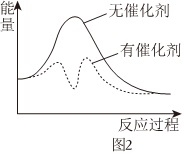
步驟Ⅰ:M+H2O=MO+H2;
步驟Ⅱ:;
從圖中可以看出使用催化劑能加快化學反應速率的原因是。組卷:8引用:1難度:0.7 -
30.鈣鈦礦(CaTiO3)型化合物是一類可用于生產太陽能電池、傳感器、固體電阻器等的功能材料.回答下列問題:
(1)基態Ti原子的價層電子排布式為。
(2)已知組成和結構相似的物質,物質的熔點隨著相對分子量的增大而增大。Ti的四鹵化物熔點如下表所示,解釋TiF4熔點出現反常的原因是。
(3)CaTiO3的晶胞如圖(a)所示,其組成元素鈣位于元素周期表中的化合物 TiF4 TiCl4 TiBr4 Ti4 熔點/℃ 377 -24.12 38.3 155 區(填s、p、d、ds),鈣和鎵的第一電離能大小順序是,圖示晶胞中Ti4+的配位數是。
(4)一種立方鈣鈦礦結構的金屬鹵化物光電材料的組成為Pb2+、I-和有機堿離子CH3,其晶胞如圖(b)所示。有機堿CH3NH+3中有配位鍵,提供空軌道的微粒是NH+3;圖(a)中的Ca2+與圖(b)中的空間位置相同,若晶胞參數(邊長)為anm,則晶體密度為g?cm-3(列出計算式)。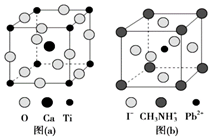 組卷:19引用:1難度:0.3
組卷:19引用:1難度:0.3


