人教版(2019)必修第二冊《6.2 化學反應的速率與限度》2020年同步練習卷(3)
發布:2024/11/12 19:0:1
一、選擇題(共13小題,每小題0分,滿分0分)
-
1.關于化學反應速率的說法正確的是( )
A.化學反應速率可表示可逆反應進行的程度 B.化學反應速率是指一定時間內,任何一種反應物濃度的減少或任何一種生成物濃度的增加 C.對于任何化學反應來說,反應速率越快,反應現象就越明顯 D.根據反應速率的大小可知化學反應進行的相對快慢 組卷:120引用:2難度:0.9 -
2.反應4A(s)+3B(g)=2C(g)+D(g),2 min內B的濃度減少0.6 mol?L-1,對此反應速率的描述正確的是( )
A.v(A)=0.4 mol?L-1?min-1 B.分別用B、C、D表示的反應速率的值之比為3:2:1 C.在2 min末的反應速率,用B表示為0.3 mol?L-1?min-1 D.在這2 min內B和C兩物質濃度都是逐漸減小的 組卷:156引用:9難度:0.6 -
3.下列有關化學反應速率的說法中正確的是( )
A.氫氣與氮氣能夠緩慢地反應生成氨氣,使用合適的催化劑可以提高化學反應速率 B.等質量的鋅粉和鋅片與相同體積、相同濃度的鹽酸反應,反應速率相等 C.用鐵片與硫酸制備氫氣時,濃硫酸可以加快產生氫氣的速率 D.增大反應CO2(g)+H2(g)═CO(g)+H2O(g)的壓強,反應速率不變 組卷:30引用:8難度:0.7 -
4.合成氨反應為:3H2+N2?2NH3,其反應速率可以分別用v(H2)、v(N2)、v(NH3)表示,反應達平衡時,下列關系式正確的是( )
A.3v(H2)正 =v(N2)逆 B.v(H2)生成= v(NH3)生成 C.v(N2)消耗 =2v(NH3)消耗 D.2v(H2)逆 =3v(NH3)正 組卷:366引用:4難度:0.9 -
5.下列哪種說法可以證明反應。N2+3H2?2NH3已達到平衡狀態( )
A.1個N≡N鍵斷裂的同時,有3個H-H鍵形成 B.1個N≡N鍵斷裂的同時,有3個H-H鍵斷裂 C.1個N≡N鍵斷裂的同時,有2個N-H鍵斷裂 D.1個N≡N鍵斷裂的同時,有6個N-H鍵形成 組卷:105引用:8難度:0.9
二、解答題(共3小題,滿分0分)
-
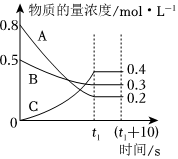 15.在一定條件下,A氣體與B氣體反應生成C氣體.反應過程中,反應物與生成物的濃度隨時間變化的曲線如圖.回答下列問題:
15.在一定條件下,A氣體與B氣體反應生成C氣體.反應過程中,反應物與生成物的濃度隨時間變化的曲線如圖.回答下列問題:
(1)該反應的化學方程式為.
(2)0~t1 s內A氣體的反應速率為.
(3)反應后與反應前的壓強之比為.
(4)(t1+10)s時,A氣體的體積分數為,此時v(A)正v(B)逆(填“>”、“<”或“=”).
(5)關于該反應的說法正確的是.
a.到達t1時刻該反應已停止
b.在t1時刻之前B氣體的消耗速率大于它的生成速率
c.在t1時刻C氣體的正反應速率等于逆反應速率.組卷:32引用:3難度:0.5 -
16.某同學在用稀硫酸與鋅制取氫氣的實驗中,發現加入少量硫酸銅溶液可加快氫氣的生成速率。請回答下列問題:
(1)上述實驗中發生反應的化學方程式有。
(2)硫酸銅溶液可以加快氫氣生成速率的原因是。
(3)要加快上述實驗中氣體產生的速率,還可采取的措施有(答兩種)。
(4)為了進一步研究硫酸銅的量對氫氣生成速率的影響,該同學設計了如下一系列實驗。將表中所給的混合溶液分別加入6個盛有過量Zn粒的反應瓶中,收集產生的氣體,記錄獲得相同體積的氣體所需時間。
①請完成此實驗設計,其中:V1=實驗混合溶液 A B C D E F 4mol?L-1H2SO4/mL 30 V1 V2 V3 V4 V5 飽和CuSO4溶液/mL 0 0.5 2.5 5 V6 20 H2O/mL V7 V8 V9 V10 10 0 ,V6=,V9=。
②該同學最后得出的結論為當加入少量CuSO4溶液時,生成氫氣的速率會大大提高,但當加入的CuSO4溶液超過一定量時,生成氫氣的速率反而會下降。請分析氫氣生成速率下降的主要原因。組卷:23引用:1難度:0.6


