2020-2021學年貴州省遵義市高二(下)期末化學試卷
發(fā)布:2025/1/1 22:30:2
一、選擇題(本題包含14個小題,每小題3分,共42分,每小題只有一個選項符合題意,請將正確選項填涂到對應的答題卡上。)
-
1.下列說法中不正確的是( )
A.需要加熱才能發(fā)生的反應不一定是吸熱反應 B.輪船底部鑲嵌鋅塊,可以防止船體被腐蝕 C.鋼鐵腐蝕的負極反應為:Fe-3e-=Fe3+ D.常溫時,向純水中加入酸或堿一定會影響水的電離程度 組卷:1引用:1難度:0.7 -
2.用鋅片與稀硫酸反應制取氫氣時.下列措施使氫氣生成速率變化最小的是( )
A.加入少量硫酸銅晶體 B.不用稀硫酸而用濃硫酸 C.用鋅粉代替鋅片 D.加少量BaCl2晶體 組卷:10引用:2難度:0.7 -
3.用如圖所示的兩個裝置進行電化學實驗,下列說法中正確的是( )
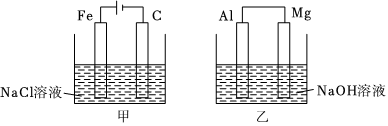
A.甲裝置中鐵作陽極,乙裝置中鎂作負極 B.兩裝置放出的氣體成分相同 C.甲、乙燒杯中均有沉淀生成 D.反應一段時間后,兩燒杯中溶液的pH都明顯減小 組卷:12引用:2難度:0.5 -
4.“氯水是淺黃綠色的液體”,且H+、Cl-、ClO-的水溶液均為無色,下列說法中正確的是( )
A.氯水中的反應可表示為:Cl2+H2O?2H++Cl-+ClO- B.將氯水滴入KI溶液中,溶液變?yōu)樽攸S色 C.氯水的漂白性是Cl2的氧化性所致 D.氯水在實驗室中可以長期保存 組卷:2引用:1難度:0.8 -
5.一定條件下,氫氣與氧氣反應的能量變化如圖所示,下列說法中正確的是( )

A.該反應的反應熱△H=(c-a)kJ/mol B.該反應為吸熱反應 C.斷裂2molH-H和1molO=O放出(b-a)kJ的能量 D.H2燃燒熱的熱化學方程式為:H2(g)+ O2(g)═H2O(g)△H=12kJ/mol(c-a)2組卷:49引用:9難度:0.6 -
6.下列有關(guān)化學及應速率的說法中錯誤的是( )
A.決定化學反應速率的主要因素是反應物本身的性質(zhì) B.同一化學反應,用不同物質(zhì)的濃度變化所表示的化學反應速率的數(shù)值不一定相同 C.某些反應選用適當?shù)拇呋瘎芙档头磻杌罨埽梢越档头磻璧臏囟?/label> D.對于反應4A(g)+B(g)═2C(g)單位時間內(nèi)的化學反應速率有4ν(A)=ν(B) 組卷:1引用:1難度:0.5 -
7.一定溫度下容積不變的密閉容器中,對于可逆反應2A(g)+B(g)?2C(g) ΔH<0,下列說法中正確的是( )
A.達到化學平衡時,ν(正)=ν(逆)=0 B.達到化學平衡后,減小體系壓強,ν(逆)增大,ν(正)減小,平衡逆向移動 C.當體系壓強不隨時間變化時,C的物質(zhì)的量濃度保持不變 D.△H不變時,反應達到化學平衡狀態(tài) 組卷:4引用:1難度:0.5
【選修5:有機化學基礎(chǔ)】
-
20.化學上常用燃燒法確定有機物的組成,這種方法是在電爐加熱下用純氧氧化管內(nèi)樣品,根據(jù)產(chǎn)物的質(zhì)量確定有機物的組成。本實驗是通過A、B裝置的質(zhì)量改變,確定有機物 M的組成。回答下列問題:
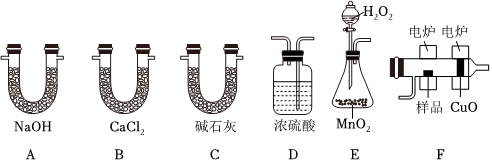
(1)裝置的連接順序(從左到右)是(填序號,裝置不能重復使用)。
(2)C裝置的作用是。
(3)E裝置中反應的化學方程式為。
(4)F裝置(燃燒管)中CuO的作用是。
(5)本實驗中,F(xiàn)裝置反應完全后繼續(xù)通入一段時間O2的目的是。
(6)若實驗中所取純樣品M只含C、H、O三種元素中的兩種或三種,M的相對分子質(zhì)量小于150,準確稱取2.44gM,經(jīng)充分反應后,A管質(zhì)量增加6.16g,B管質(zhì)量增加1.08g。
①該樣品M的實驗式為。
②能否確定M的分子式(填“能”或“不能”)。組卷:3引用:1難度:0.5 -
21.某天然有機物A遇碘水變藍,在酶作用下水解生成B,1molB水解可生成2molC:D是可再生能源,同時D的溶液是常用的飲料之一,且D的質(zhì)譜圖(圖一)和核磁共振氫譜圖(圖二)如下所示;E的核磁共振氫譜有4組峰且峰面積之比為3:1:1:1;F是一種高分子材料。它們之間的轉(zhuǎn)化關(guān)系如圖所示,回答下列問題:
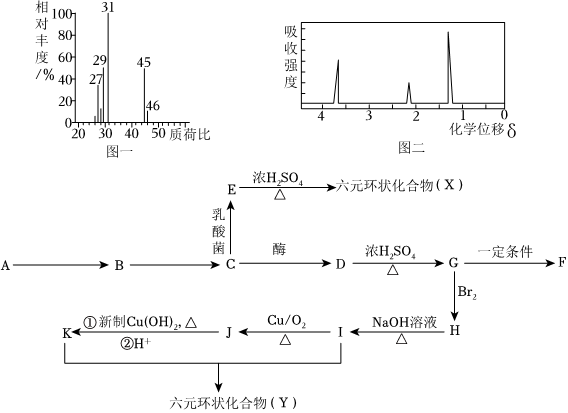
(1)B的名稱是,E中官能團的名稱是。
(2)X的結(jié)構(gòu)簡式為。
(3)H→I的化學方程式為,反應類型是。
(4)I與K生成高分子化合物的化學方程式為。
(5)已知某芳香烴的質(zhì)譜圖中最大質(zhì)荷比與Y的相對分子質(zhì)量的數(shù)值相等,則該芳香烴滿足下列條件的同分異構(gòu)體有種;
①同一碳原子上不能連兩個碳碳雙鍵
③只含苯環(huán),不含其他環(huán)狀結(jié)構(gòu)
寫出其中核磁共振氫譜有4組峰且峰面積之比為 1:2:2:3的結(jié)構(gòu)簡式。
(6)寫出由E制備 的線路圖(其他試劑任選) 。組卷:9引用:1難度:0.5
的線路圖(其他試劑任選) 。組卷:9引用:1難度:0.5


