2022-2023學年甘肅省天水市秦安一中高一(上)期中化學試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(60分)。
-
1.下列科研成果不是由我國發(fā)明或創(chuàng)造的是( )
A.世界上第一個由人工合成的、具有生理活性的蛋白質(zhì)--結(jié)晶牛胰島素 B.黑火藥和造紙 C.發(fā)現(xiàn)元素周期律 D.青蒿素的合成 組卷:8引用:2難度:0.9 -
2.2017年7月,清華大學寧存政教授課題組在硅基納米激光器和光放大器研究上獲得重大突破,對世界科技具有重要意義。下列分散系中分散質(zhì)的微粒直徑與納米級(1~100nm)粒子具有相同數(shù)量級的是( )
A.溶液 B.膠體 C.懸濁液 D.乳濁液 組卷:17引用:3難度:0.8 -
3.我國女科學家屠呦呦發(fā)現(xiàn)青蒿素(青蒿素的化學式:C15H22O5),它是一種用于治療瘧疾的藥物,曾經(jīng)挽救了數(shù)百萬人的生命,2015年獲得諾貝爾生理與醫(yī)學獎,成為我國獲得諾貝爾科學獎的第一人。下列關(guān)于青蒿素的敘述錯的是( )
A.青蒿素的一個分子中的含有42個原子 B.青蒿素是一種有機物 C.青蒿素的摩爾質(zhì)量為282 D.青蒿素中碳元素的質(zhì)量分數(shù)約為63.8% 組卷:17引用:4難度:0.8 -
4.碳酸鈉的物質(zhì)類別是( )
A.酸 B.堿 C.鹽 D.酸性氧化物 組卷:66引用:3難度:0.8 -
5.下列物質(zhì)中屬于堿性氧化物的是( )
A.Na2O B.SO2 C.NH3 D.KOH 組卷:90引用:3難度:0.7 -
6.下列物質(zhì)能使干燥的藍色石蕊試紙先變紅后褪色的是( )
①氯氣 ②液氯 ③新制氯水 ④氯氣的四氯化碳溶液 ⑤鹽酸 ⑥鹽酸與少量漂白粉的混合溶液.A.①②③ B.①②③⑥ C.③⑥ D.③④⑥ 組卷:277引用:11難度:0.7 -
7.最新研究發(fā)現(xiàn),人體內(nèi)自身產(chǎn)生的NO能促進全身血液循環(huán),預防動脈粥樣硬化,恢復血管柔軟性和彈性。下列有關(guān)NO的敘述中,正確的是( )
A.NO能溶于水,不能用排水法收集 B.NO暴露在空氣中,氣體由無色變?yōu)榧t棕色,發(fā)生的是物理變化 C.“雷雨發(fā)莊稼”的諺語涉及到NO,生成NO的過程屬于自然固氮 D.由信息知人可吸入大量NO,有利于身體健康 組卷:28引用:3難度:0.7 -
8.Na在空氣中加熱的產(chǎn)物是( )
A.Na2O B.Na2O2 C.NaOH D.NaHCO3 組卷:84引用:3難度:0.5
二、填空題(40分)。
-
23.某小組同學設(shè)計實驗實現(xiàn)幾種價態(tài)硫元素的轉(zhuǎn)化。
任務(wù)Ⅰ:從以下試劑中選擇合適的試劑實現(xiàn)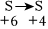 的轉(zhuǎn)化。
的轉(zhuǎn)化。
試劑清單:①濃H2SO4 ②稀H2SO4 ③酸性KMnO4溶液 ④Na2SO3溶液
⑤Cu ⑥品紅
(1)寫出實現(xiàn)轉(zhuǎn)化的化學方程式
(2)設(shè)計實驗,證明實現(xiàn)了該轉(zhuǎn)化(寫出操作和現(xiàn)象)。
Ⅱ.實現(xiàn)硫元素在0、+2、+4價之間的轉(zhuǎn)化。
查閱資料:+2價硫在酸性條件下不穩(wěn)定,易發(fā)生自身氧化還原反應(yīng)。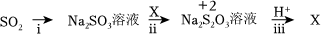
(3)i中加入的物質(zhì)是,該轉(zhuǎn)化利用的是SO2的性質(zhì)。
(4)寫出iii的離子方程式。組卷:54引用:2難度:0.7 -
24.我國化學家侯德榜發(fā)明的“聯(lián)合制堿法”為世界制堿工業(yè)做出了巨大貢獻。如圖為聯(lián)合制堿法的主要過程(部分物質(zhì)已略去)。
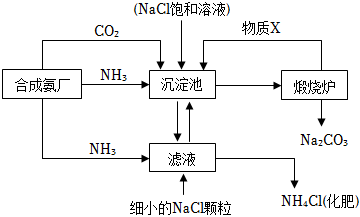
資料:ⅰ.沉淀池中的反應(yīng)為NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl
ⅱ.溶解度
(1)煅燒爐中反應(yīng)的化學方程式是物質(zhì) NaCl NH4HCO3 NaHCO3 NH4Cl 20℃溶解度/g 36.0 21.7 9.6 37.2 ,物質(zhì)X是(填化學式)。
(2)下列說法正確的是(填字母)。
A.沉淀池中有NaHCO3析出,因為一定條件下NaHCO3的溶解度最小
B.濾液中主要含有NaCl、Na2CO3和NH4Cl
C.設(shè)計循環(huán)的目的是提高原料的利用率
(3)工業(yè)可用純堿代替燒堿生產(chǎn)某些化工產(chǎn)品,如用飽和純堿溶液與Cl2反應(yīng)可制得一種在生產(chǎn)生活中常用于漂白、消毒的物質(zhì),同時有NaHCO3生成,該反應(yīng)的化學方程式是。
(4)某純堿樣品中含雜質(zhì)NaCl,取質(zhì)量為ag的樣品,加入足量的稀鹽酸,充分反應(yīng)后,加熱、蒸干、灼燒,得到bg固體物質(zhì),則此樣品中Na2CO3的質(zhì)量分數(shù)為。組卷:170引用:8難度:0.7


