2021-2022學年寧夏銀川二中高一(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(每小題只有一個選項符合題意,每題2分,共40分)
-
1.在元素周期表中位于金屬元素和非金屬元素交界處最容易找到的材料是( )
A.制催化劑的材料 B.耐高溫、耐腐蝕的合金材料 C.制農藥的材料 D.半導體材料 組卷:359引用:122難度:0.9 -
2.元素周期表是一座開放的“元素大廈”,“元素大廈”尚未客滿。若發現120號元素,請在“元素大廈”中安排好它的“房間”( )
A.第7周期0族 B.第7周期第ⅠA族 C.第8周期第ⅡA族 D.第8周期第ⅠA族 組卷:2引用:1難度:0.7 -
3.已知
I、13153Cs、13755Cs具有放射性,下列有關說法正確的是( )13455A.137是銫元素的相對原子質量 B. I放出射線是一個化學變化13753C. I與13153Cs的中子數相同13455D. Cs、13755Cs互為同位素13455組卷:3引用:1難度:0.7 -
4.原子核外電子的運動規律是元素周期律的基礎,下列說法錯誤的是( )
A.同一原子中,離核較遠的電子受到的吸引力較小 B.原子核外電子排布時L層未排滿,則M層無電子 C.同一周期中,隨著核電荷數的增加,元素的最高化合價一定增大 D.第四周期中,ⅡA與ⅢA族元素原子的核電荷數相差11 組卷:38引用:4難度:0.5 -
5.下列為元素周期表中的一部分,表中數字為原子序數,M的原子序數為37的是( )
A. 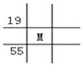
B. 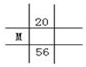
C. 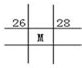
D. 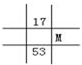 組卷:308引用:43難度:0.9
組卷:308引用:43難度:0.9 -
6.利用焰色反應的原理既可制作五彩繽紛的節日煙花,亦可定性鑒別某些金屬鹽。灼燒食鹽樣品時,鈉的焰色為( )
A.黃色 B.紅色 C.紫色 D.綠色 組卷:97引用:4難度:0.8 -
7.鉀和鈉的性質相似,下列說法中能最好的解釋這個事實的是( )
A.都是金屬 B.原子半徑相差不大 C.最高化合價相同 D.最外層電子數相同 組卷:33引用:3難度:0.7 -
8.已知1~18號元素的離子aW3+、bX+、cY2-、dZ-都具有相同的電子層結構,下列關系正確的是( )
A.單質的還原性:X>W B.原子序數:c>b C.氫化物的穩定性:H2Y>HZ D.離子半徑:X<W 組卷:7引用:3難度:0.7 -
9.原子電子層數相同的X、Y、Z三種元素,若最高價氧化物水化物酸性強弱為 H3XO4<H2YO4<HZO4,則下列判斷正確的是( )
A.非金屬性強弱為X>Y>Z B.氣態氫化物的穩定性為:H3X>H2Y>HZ C.原子半徑為X<Y<Z D.陰離子的還原性為X3->Y2->Z- 組卷:20引用:3難度:0.7
三、填空題(共65分)
-
28.某研究性學習小組查閱資料得知,漂白粉與硫酸溶液反應可制取氯氣,化學方程式為:Ca(ClO)2+CaCl2+2H2SO4
2CaSO4+2Cl2↑+2H2O,他們設計如下實驗制取氯氣并驗證其性質。請回答下列問題:△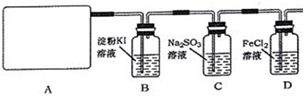
(1)每生成1molCl2,上述化學反應中轉移的電子個數為(NA表示阿伏加德羅常數)。
(2)該實驗中A部分的裝置是(填寫裝置的序號)。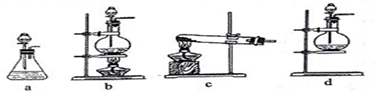
(3)裝置B中的現象是。
(4)請寫出裝置D中反應的離子方程式。
(5)此實驗設計存在的明顯缺陷是,改進方法是。
(6)請幫助他們設計一個實驗,證明洗氣瓶C中的亞硫酸鈉已被氧化(簡述實驗步驟):。
(7)氯氣是活潑的非金屬單質,具有很強的性(填“氧化”或“還原”)。組卷:7引用:1難度:0.7 -
29.某同學利用鐵與硫酸的反應,探究影響反應速率的因素(實驗所用鐵的質量相等且鐵塊的形狀相同,硫酸均過量),實驗設計如表:
回答下列問題:實驗編號 硫酸濃度/(mol?L-1) 硫酸體積/mL 鐵的狀態 溫度/K 1 1.00 40 塊狀 293 2 2.00 40 塊狀 293 3 2.00 40 粉末 293 4 2.00 40 塊狀 313
(1)若四組實驗均以收集到448mL(標準狀況)氫氣為標準,則上述實驗中還需要測定的數據是。
(2)實驗1和2是探究對該反應速率的影響;實驗和是探究溫度對該反應速率的影響。
(3)根據實驗測得的在不同時間t產生氫氣體積V的數據,繪制得到圖甲,則曲線c對應的實驗組別可能是。根據實驗數據,該同學發現對于每一組實驗,產生氫氣的速率υ隨時間t變化情況如圖乙所示,其中t1~t2速率變化的主要原因是。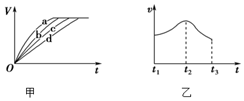
(4)若上述實驗所用硫酸體積均為250mL,實驗3反應進行2min時收集到448mL(標準狀況)氫氣,該時間段內以硫酸的濃度變化表示的平均反應速率v(H2SO4)=(反應后溶液體積不變)。
(5)實驗4如果反應太激烈,為了減緩反應速率而又不影響產生氫氣的量,下列措施你認為可行的是(填編號)。
A.加蒸餾水
B.減小壓強
C.加入CH3COONa
D.加CuSO4固體
(6)進行實驗3時,若將稀硫酸改為40mL4.0mol?L-1鹽酸(其他條件不變),發現放出氣泡的速率,鹽酸明顯比硫酸快。你認為可能的原因是(忽略溫度對反應速率的影響)。組卷:15引用:3難度:0.6


