2021-2022學年山東省青島市萊西一中普通班高一(上)月考化學試卷(12月份)
發布:2024/4/20 14:35:0
一、選擇題:(本題共10小題,每小題2分,共20分.每小題只有一個選項符合題目要求.)
-
1.中華文化源遠流長、博大精深,下列傳統文化中蘊含的化學知識或原理不正確的是( )
A.《肘后備急方》中記載:“青蒿一握,以水二升漬,絞取汁,盡服之……”,提取青蒿素屬于化學變化 B.《夢溪筆談》中:“石穴中水,所滴者皆為鐘乳”,該現象未涉及氧化還原反應 C.《抱樸子?金丹篇》記載:“凡草木燒之即燼,而丹砂(硫化汞)燒之成水銀,積變又還成丹砂”,該過程涉及的反應都是氧化還原反應 D.《夢溪筆談》中“方家以磁石磨針鋒,則能指南”中的磁石主要成分為Fe3O4 組卷:69引用:2難度:0.7 -
2.下列有關硫及其化合物性質的說法中,正確的是( )
A.銅粉和硫粉混合加熱可制得CuS B.久置酸雨酸性增強,原因是水的揮發 C.SO2通入石蕊試液中,溶液顏色先變紅,再褪色 D.亞硫酸鈉暴露在空氣中容易被氧化成硫酸鈉 組卷:61引用:3難度:0.8 -
3.下列各組離子能在溶液中大量共存的是( )
A.K+、Mg2+、CO32-、Cl- B.Na+、K+、CO32-、Cl- C.Na+、Ca2+、HCO3-、OH- D.Fe2+、H+、SO42-、ClO- 組卷:3引用:1難度:0.7 -
4.下列敘述不正確的是( )
A.工業生產中常用生石灰來吸收廢氣中的二氧化硫 B.二氧化硫的水溶液能使紫色石蕊試液變紅,說明二氧化硫能與水反應生成酸 C.二氧化硫能使有色物質顏色消失,說明二氧化硫具有氧化性 D.二氧化硫能使酸性高錳酸鉀溶液褪色,說明二氧化硫具有還原性 組卷:10引用:3難度:0.9 -
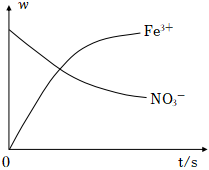 5.某反應過程中存在Fe2+、NO3-、Fe3+、NH4+、H+和H2O六種粒子,測得Fe3+、NO3-的質量分數(w)隨時間變化的曲線如圖所示,下列判斷錯誤的是( )
5.某反應過程中存在Fe2+、NO3-、Fe3+、NH4+、H+和H2O六種粒子,測得Fe3+、NO3-的質量分數(w)隨時間變化的曲線如圖所示,下列判斷錯誤的是( )A.NO3-被還原,發生還原反應 B.還原性:Fe2+>NH4+ C.Fe2+被氧化為Fe3+ D.還原劑與氧化劑的物質的量之比為1:8 組卷:35引用:2難度:0.7 -
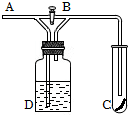 6.如圖所示,在A處通入未經干燥的氯氣。當關閉B閥時,C處的紅布條看不到明顯現象;當打開B閥后,C處的紅布條逐漸褪色。則D瓶中盛放的溶液可能是( )
6.如圖所示,在A處通入未經干燥的氯氣。當關閉B閥時,C處的紅布條看不到明顯現象;當打開B閥后,C處的紅布條逐漸褪色。則D瓶中盛放的溶液可能是( )
①NaOH溶液
②H2O
③濃硫酸
④飽和NaCl溶液A.①③ B.①④ C.②③ D.②④ 組卷:8引用:3難度:0.7 -
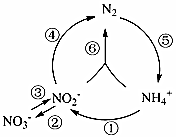 7.自然界中氮元素部分循環如圖所示,下列說法錯誤的是( )
7.自然界中氮元素部分循環如圖所示,下列說法錯誤的是( )A.反應①~⑥均屬于氧化還原反應 B.反應①②⑤均屬于氮的固定 C.反應⑥的離子方程式為NH4++NO2-═N2↑+2H2O D.向水體中大量排放NH4+及NO3-能引起水質惡化 組卷:157引用:1難度:0.5
三、非選擇題:(本題共7小題,共60分.)
-
21.某研究小組用如圖裝置進行SO2與FeCl3溶液反應的相關實驗(夾持裝置略去)。
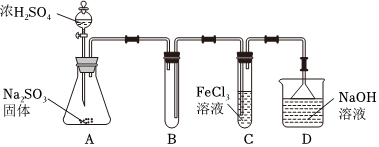
(1)通入足量SO2時C中觀察到的現象為。
(2)根據以上現象,該小組同學認為SO2與FeCl3溶液發生氧化還原反應。
①寫出SO2與FeCl3溶液反應的離子方程式:。
②寫出D溶液吸收尾氣的離子方程式:。
③該小組同學向C試管反應后的溶液中加入硝酸酸化的BaCl2溶液,若出現白色沉淀,即可證明反應生成了。該做法SO2-4(填“合理”或“不合理”),理由是。
(3)裝置B的作用是。
(4)為了驗證SO2具有還原性,實驗中可以代替FeCl3的試劑有(填序號)。
A.濃硫酸
B.酸性KMnO4溶液
C.NaCl 溶液
D.氯水
E.品紅溶液組卷:20引用:2難度:0.7 -
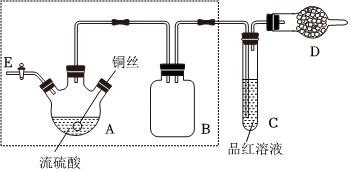 22.某同學對教材中銅與濃硫酸的實驗作了如下改進。實驗裝置如圖所示(加熱和夾持裝置已略去)。
22.某同學對教材中銅與濃硫酸的實驗作了如下改進。實驗裝置如圖所示(加熱和夾持裝置已略去)。
實驗步驟:
①組裝儀器,檢查裝置氣密性;
②加入試劑,關閉旋塞E,加熱A,觀察C中溶液顏色變化;
③將銅絲上提離開液面,停止加熱。
(1)檢查虛線框內裝置氣密性的方法是。
(2)儀器B的作用是,儀器D中所盛藥品是。
(3)證明該反應有SO2生成的現象為。
(4)實驗后,拆除裝置前,為避免有害氣體的泄漏,應當采取的操作是。
(5)實驗后儀器A中有白色固體產生,將儀器A中固液混合物緩慢轉移至盛有少量水的燒杯中,可觀察到的現象是。不可直接向儀器A中加水的原因是。組卷:17引用:1難度:0.6


