2021-2022學年上海二中(合格班)高二(下)期末化學試卷
發布:2025/1/7 23:0:2
一、選擇題(共80分,每題只有1個選項,每題2分)
-
1.
Po的中子數為( )21084A.84 B.210 C.126 D.294 組卷:39引用:1難度:0.8 -
2.提出原子結構的行星模型的科學家是( )
A.道爾頓 B.湯姆孫 C.盧瑟福 D.倫琴 組卷:18引用:5難度:0.6 -
3.有機物中均含有的元素是( )
A.碳 B.硫 C.氧 D.氮 組卷:53引用:2難度:0.8 -
4.
H、11H、21H、H+、H2是( )31A.氫的五種同位素 B.五種氫元素 C.氫的五種同素異形體 D.氫元素的五種不同粒子 組卷:144引用:30難度:0.7 -
5.下列微粒中與OH-具有相同質子數和電子數的是( )
A.Na+ B.Ne C.Cl- D.F- 組卷:55引用:2難度:0.7 -
6.下列各組微粒中,具有相同的電子層數和最外層電子數的是( )
A.He和H B.F-和Mg2+ C.Cl-和Na+ D.Al3+和Ar 組卷:41引用:1難度:0.7 -
7.下列各組的量不隨原子序數的遞增呈現周期性變化的是( )
A.原子核外電子數 B.化合價 C.原子半徑 D.原子最外層電子數 組卷:17引用:2難度:0.7 -
8.在元素周期表中位于金屬和非金屬元素的交界處,容易找到的元素是( )
A.制備催化劑的元素 B.耐高溫的合金元素 C.制備農藥的元素 D.用于半導體材料的元素 組卷:22引用:5難度:0.9 -
9.主族元素R的最高價氧化物的化學式為R2O5,則它的氣態氫化物的化學式是( )
A.RH4 B.RH3 C.H2R D.HR 組卷:20引用:4難度:0.7 -
10.迄今為止,下列各族元素中生成化合物種類最多的是( )
A.ⅡA族 B.ⅢA族 C.ⅣA族 D.ⅤA族 組卷:34引用:1難度:0.5 -
11.A和B均為短周期元素,它們的離子A-和B2+具有相同的核外電子層結構。下面說法正確的是( )
A.原子序數A>B B.核外電子數為A>B C.原子半徑A>B D.離子半徑 A->B2+ 組卷:48引用:11難度:0.9 -
12.X、Y是同周期的非金屬元素,若X的原子半徑小于Y的原子半徑,則下列說法中正確的是( )
A.X的非金屬性比Y強 B.X原子最外層電子數比Y少 C.Y單質的氧化性大于X D.Y的氣態氫化物的穩定性大于X的氣態氫化物 組卷:55引用:1難度:0.6 -
13.下列關于離子鍵的敘述正確的是( )
A.原子間強烈的相互作用 B.陰、陽離子間強烈的吸引作用 C.陰、陽離子間強烈的排斥作用 D.陰、陽離子間強烈的靜電作用 組卷:28引用:1難度:0.7 -
14.下列物質的電子式正確的是( )
A.氯化鈣 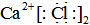
B.硫化氫 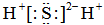
C.氯氣: 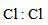
D.甲烷: 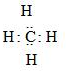 組卷:81引用:1難度:0.8
組卷:81引用:1難度:0.8
二、非選擇題
-
41.乙醇汽油可作為汽車的燃料,是目前世界上可再生能源的發展重點.乙醇是一種重要的工業原料,可由乙烯為原料制得,完成下列填空.
(1)乙醇中所含的官能團的名稱為.
(2)乙烯的空間構型為形.
(3)寫出乙烯與水反應制備乙醇的方程式:;該反應類型為反應.
實驗室可用乙醇和乙酸為原料制備乙酸乙酯,實驗裝置如圖所示.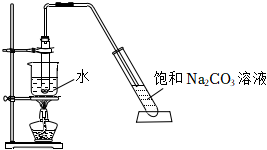
(4)寫出制取乙酸乙酯的方程式:.
(5)該實驗中飽和Na2CO3作用是.組卷:9引用:1難度:0.7 -
42.下表為元素周期表中的一部分.
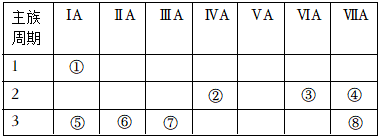
(1)元素⑥所對應離子的結構示意圖.元素①③⑤所形成化合物的電子式.
(2)元素②在周期表中的位置是.
(3)元素④、⑦、⑧原子所對應離子的半徑按由大到小的順序排列為(用離子符號表示).
(4)上述元素中金屬性最強的是(填元素符號),最高價氧化物對應水化物的酸性最強的物質為(填化學式).組卷:11引用:1難度:0.5


