2022年內(nèi)蒙古呼倫貝爾市部分學(xué)校高考化學(xué)質(zhì)檢試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題:本題共7小題,每小題6分,共78分。在每小題給出的四個(gè)選項(xiàng)中,只有一項(xiàng)是符合題目要求的。
-
1.化學(xué)與生活、生產(chǎn)密切相關(guān),下列有關(guān)說法不正確的是( )
A.2022北京冬奧會(huì)上頒獎(jiǎng)禮服的衣服內(nèi)膽里添加的石墨烯發(fā)熱材料屬于新型有機(jī)高分子材料 B.開發(fā)利用新能源,減少化石燃料的燃燒,可以有效減少CO2的排放,實(shí)現(xiàn)“碳達(dá)峰、碳中和”的目標(biāo) C.鈦合金具有高比強(qiáng)度、耐腐蝕和耐低溫等性能,故可應(yīng)用于航空航天領(lǐng)域 D.燃煤時(shí)添加石灰石,可以減少SO2等有害氣體的排放 組卷:12引用:1難度:0.9 -
2.設(shè)NA為阿伏加德羅常數(shù)的數(shù)值,下列說法正確的是( )
A.向沸水中滴加含0.1 mol氯化鐵的飽和溶液,制得的Fe(OH)3膠體粒子數(shù)目是0.1NA B.標(biāo)準(zhǔn)狀況下,22.4 L的CH2Cl2所含的分子總數(shù)為NA C.4.0 g H218O所含質(zhì)子數(shù)為2NA D.1 mol?L-1 Na2CO3溶液中含有的CO32-數(shù)目小于NA 組卷:13引用:1難度:0.6 -
3.短周期主族元素X、Y、W、Z、R的原子序數(shù)依次增大。其中X、Z同主族,Z的單質(zhì)是制造太陽能電池的常用材料,W3+與Y2-具有相同的核外電子數(shù),R是同周期中原子半徑最小的元素。下列說法正確的是( )
A.Y2-的半徑大于W3+的半徑 B.Y、Z形成的二元化合物為離子化合物 C.Z的最高價(jià)氧化物對應(yīng)的水化物的酸性比X的強(qiáng) D.Z的氣態(tài)簡單氫化物的穩(wěn)定性比R的強(qiáng) 組卷:6引用:1難度:0.6 -
4.下列實(shí)驗(yàn)現(xiàn)象和結(jié)論都正確的是( )
選項(xiàng) 實(shí)驗(yàn)操作 現(xiàn)象 結(jié)論 A 將SO2通入酸性高錳酸鉀溶液 高錳酸鉀溶液紫色褪色 SO2具有漂白性 B 向某溶液中滴加KSCN溶液 溶液顯紅色 原溶液中有Fe3+ C 將稀鹽酸滴入碳酸鈉溶液中產(chǎn)生的氣體直接通入硅酸鈉溶液 有白色沉淀生成 證明非金屬性
Cl>C>SiD 滴加稀NaOH溶液,將濕潤的紅色石蕊試紙置于試管口 試紙不變藍(lán) 原溶液中無NH4+ A.A B.B C.C D.D 組卷:11引用:1難度:0.7
三、【化學(xué)——選修3:物質(zhì)結(jié)構(gòu)與性質(zhì)】
-
11.(NH4)3[Fe(SCN)6]、[Fe(TCNE)(NCCH3)2][FeCl4]、K4[Fe(CN)6]?3H2O等鐵的配合物用途非常廣泛。回答下列問題:

(1)基態(tài)Fe原子價(jià)層電子的電子排布圖(軌道表達(dá)式)為。
(2)Fe與Ca位于同一周期且最外層電子構(gòu)型相同,鐵的熔點(diǎn)和沸點(diǎn)均比鈣的高,其原因是。
(3)圖一中配合物(NH4)3[Fe(SCN)6]中的H、S、N的電負(fù)性從大到小的順序是。
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配體為CH3CN和TCNE。
①CH3CN中碳原子的雜化方式是和。
②TCNE中第一電離能較大的是(填元素符號(hào)),分子中所有原子(填“在”或“不在”)同一平面,分子中σ 鍵與π鍵的數(shù)目之比是。
(5)K4[Fe(CN)6]?3H2O是食鹽的抗結(jié)劑,強(qiáng)熱分解有Fe3C生成,F(xiàn)e3C 的晶胞結(jié)構(gòu)如圖二所示:Fe3C的密度為(列出計(jì)算式)g?cm-3。組卷:17引用:3難度:0.7
四、【化學(xué)——選修5:有機(jī)化學(xué)基礎(chǔ)】
-
12.藥物中間體 Q、醫(yī)用材料 PVA 的合成路線如圖。
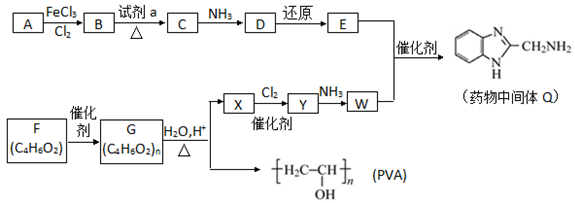
已知:-NH2+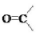 →
→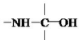
(1)A 的分子式是 C6H6,A→B 的反應(yīng)類型是。
(2)B→C 是硝化反應(yīng),試劑 a 是。
(3)C→D 為取代反應(yīng),其化學(xué)方程式是。
(4)F 含有的官能團(tuán)是。
(5)F 的含有碳碳雙鍵和酯基的同分異構(gòu)體有種(含順反異構(gòu)體,不含 F),其中核磁共振氫譜有 3 組吸收峰,且能發(fā)生銀鏡反應(yīng)的結(jié)構(gòu)簡式是。
(6)G→X 的化學(xué)方程式是。
(7)W 能發(fā)生聚合反應(yīng),形成的高分子結(jié)構(gòu)簡式是。
(8)將下列 E+W→Q 的流程圖補(bǔ)充完整(在虛線框內(nèi)寫出物質(zhì)的結(jié)構(gòu)簡式):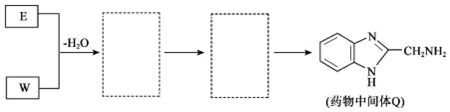 組卷:13引用:2難度:0.4
組卷:13引用:2難度:0.4


