2021-2022學年廣西玉林市博白中學高二(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共7小題,每小題6分,共78分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.下列化學用語書寫正確的是( )
A.基態Mg原子的核外電子排布圖: 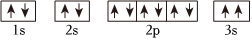
B.過氧化氫電子式: 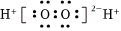
C.As原子的簡化電子排布式為[Ar]4s24p3 D.原子核內有10個中子的氧原子: O188組卷:19引用:3難度:0.6 -
2.下列關于晶體的敘述中,正確的是( )
A.原子晶體中,共價鍵的鍵能越大,熔、沸點越高 B.分子晶體中,分子間的作用力越大,該分子越穩定 C.分子晶體中,共價鍵的鍵能越大,熔、沸點越高 D.某晶體溶于水后,可電離出自由移動的離子,該晶體一定是離子晶體 組卷:464引用:21難度:0.7 -
3.下列各項敘述中,正確的是( )
A.鎂原子由1s22s22p63s2→1s22s22p63p2時,原子釋放能量,由基態轉化成激發態 B.價電子排布為5s25p1的元素位于第五周期第ⅠA族,是S區元素 C.所有原子任一能層的S電子云輪廓圖都是球形,但球的半徑大小不同 D.24Cr原子的電子排布式是:1s22s22p63s23p63d44s2 組卷:185引用:23難度:0.9
三、[化學—選修3:物質結構與性質](共1小題,滿分15分)
-
 9.A、B、C、D、E代表前四周期原子序數依次增大的五種元素。A、D同主族且有兩種常見化合物DA2和DA3;工業上電解熔融C2A3制取單質C;B、E除最外層均只有2個電子外,其余各層全充滿,E位于元素周期表的ds區。回答下列問題:
9.A、B、C、D、E代表前四周期原子序數依次增大的五種元素。A、D同主族且有兩種常見化合物DA2和DA3;工業上電解熔融C2A3制取單質C;B、E除最外層均只有2個電子外,其余各層全充滿,E位于元素周期表的ds區。回答下列問題:
(1)B、C中第一電離能較大的是,基態D原子價電子的軌道表達式為。
(2)DA2分子的VSEPR模型是。H2A比H2D熔沸點高得多的原因是。
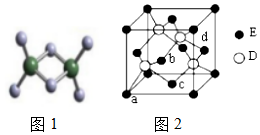
(3)實驗測得C與氯元素形成化合物的實際組成為C2Cl6,其球棍模型如圖1所示。已知C2Cl6 在加熱時易升華,與過量的NaOH溶液反應可生成Na[C(OH)4]。
①C2Cl6屬于晶體(填晶體類型),其中C原子的雜化軌道類型為雜化。
②[C(OH)4]-中存在的化學鍵有。
(4)工業上制備B的單質是電解熔融B的氯化物,而不是電解BA,原因是。
(5)B、C的氟化物晶格能分別是2957kJ?mol-1、5492kJ?mol-1,二者相差很大的原因是。
(6)D與E所形成化合物晶體的晶胞如圖2所示。
①在該晶胞中,E的配位數為。
②已知該晶胞的密度為ρ g/cm3,則其中兩個D原子之間的距離為pm(列出計算式即可)。組卷:13引用:3難度:0.5
四、[化學——選修5:有機化學基礎](共1小題,滿分15分)
-
10.阿帕魯胺是一種治療癌癥的藥物,其合成路線如圖。
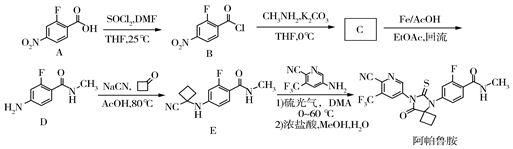
已知:
回答下列問題:
(1)A生成B的反應類型為。A中含氧官能團的名稱為。
(2)C的結構簡式為。
(3)B生成C反應中,K2CO3的作用是。
(4)寫出D生成E的化學方程式:。
(5)X為D的芳香族同分異構體,寫出滿足下列條件的X的任意兩種結構簡式、。
①含有酰胺基(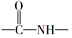 );
);
②核磁共振氫譜有5組峰,峰面積之比為3:2:2:1:1;
③苯環上有兩個取代基,其中一個為F原子。
(6)以甲苯為原料可合成化合物A。已知: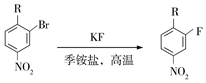 ,寫出制備化合物A時中間產物X、Y、Z的結構簡式:、、。
,寫出制備化合物A時中間產物X、Y、Z的結構簡式:、、。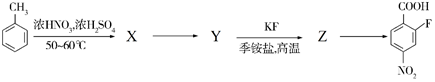 組卷:7引用:1難度:0.5
組卷:7引用:1難度:0.5


