2012-2013學年上海市松江二中高三(下)開學化學試卷(2月份)
發布:2024/4/20 14:35:0
一、選擇題(本題共10分,每小題2分,每題只有一個正確選項)
-
1.下列問題處理的過程中主要發生化學變化的是( )
A.通過水解將“地溝油”制成肥皂 B.用多孔吸附劑清除海面上泄漏的原油 C.把放射性核廢料深埋于地下巖層 D.用蒸餾方法從食鹽水中獲得純凈水 組卷:28引用:6難度:0.9 -
2.下列化學用語表示正確的是( )
A.CO2分子的球棍模型: 
B.COCl2的電子式: 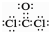
C.質子數為6、質量數為14的原子: N146D.熔融狀態下硫酸氫鉀的電離方程式:KHSO4(熔融)→K++H++SO4- 組卷:13引用:1難度:0.9 -
3.干冰氣化時,下列所述內容發生變化的是( )
A.分子內共價鍵 B.分子大小 C.分子間的作用力 D.分子內共價鍵的鍵長 組卷:9引用:3難度:0.9 -
4.下列有關物質的性質與其應用不相對應的是( )
A.常溫下濃硫酸能使鋁發生鈍化,可在常溫下用鋁制容器貯藏貯運濃硫酸 B.氯氣具有強氧化性,因此可用于漂白有色布料 C.NH3能與Cl2生成NH4Cl,可用濃氨水檢驗輸送氯氣的管道是否有泄漏 D.氫氟酸能與二氧化硅反應,因此可用于刻蝕玻璃 組卷:5引用:1難度:0.9 -
5.化學規律中經常會有特例,下列有關規律的描述正確的是( )
A.分子晶體中一定含有共價鍵 B.常溫時pH=7的溶液一定是中性溶液 C.放熱反應在常溫下一定能發生 D.只含有極性鍵的分子一定是極性分子 組卷:23引用:3難度:0.9
二、選擇題(本題共36分,每小題3分,只有一個正確選項.)
-
6.“類推”的思維方式在化學學習與研究中經常采用.下列類推思維中正確的是( )
A.NaOH飽和溶液導電能力強,則Ca(OH)2飽和溶液導電能力也強 B.CaC2能水解:CaC2+2H2O→Ca(OH)2+HC≡CH,則Mg2C2也能水解:Mg2C2+4H2O→2Mg(OH)2+CH3-C≡CH C.加熱時Cu與O2反應生成CuO,則加熱時Cu與S反應生成CuS D.BaCl2溶液中通入SO2無沉淀產生,則Ba(NO3)2溶液中通入SO2也無沉淀產生 組卷:116引用:4難度:0.5 -
7.已知:乙醇可被強氧化劑氧化為乙酸.BrCH2CH=CHCH2Br可經三步反應制取HOOCCHClCH2COOH,發生反應的類型依次是( )
A.水解反應、加成反應、氧化反應 B.加成反應、水解反應、氧化反應 C.水解反應、氧化反應、加成反應 D.加成反應、氧化反應、水解反應 組卷:126引用:10難度:0.9 -
8.在壓強為2.20×104kPa、溫度達到374℃時,水成為“超臨界狀態”,此時水可與CO2等含碳化合物反應生成有機物,這就是“水熱反應”,生物質在地下高溫高壓條件下通過水熱反應可生成石油、煤等礦物能源.下列說法錯誤的是( )
A.火力發電廠可望利用廢熱,通過水熱反應將二氧化碳轉變為能源物質 B.“水熱反應”是一種復雜的物理化學變化 C.超臨界水與普通水的組成不相同 D.隨著科技的進步,通過“水熱反應”獲取能源有望實現地球上碳資源的和諧循環 組卷:95引用:4難度:0.7 -
9.反應①、②分別是從海藻灰和某種礦石中提取碘的主要反應:
①2NaI+MnO2+3H2SO4═2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3═2Na2SO4+3NaHSO4+H2O+I2
下列說法正確的是( )A.兩個反應中均為硫元素被氧化 B.碘元素在反應①中被還原,在反應②中被氧化 C.氧化性:MnO2> >SO2-4>I2IO-3D.反應①、②中生成等量的I2時轉移電子數比為1:5 組卷:432引用:54難度:0.7 -
10.下列離子能在溶液中大量共存,當將溶液的pH調節至1時就會出現渾濁的是( )
A.Fe2+、Fe3+、 、NH+4NO-3B.S2-、K+、I-、 SO2-3C.Na+、I-、 、CO2-3NO-3D.Al3+、 、OH-、Na+HCO-3組卷:6引用:3難度:0.7
四、解答題(共8小題,滿分84分)
-
29.某化合物A的結構簡式為:
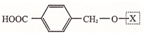 ,為了研究X的結構,將化合物A在一定條件下水解只得到B(分子式為C8H8O3)和C(分子式為C7H 6O3).C遇FeCl3水溶液顯紫色,與NaHCO3溶液反應有CO2產生.
,為了研究X的結構,將化合物A在一定條件下水解只得到B(分子式為C8H8O3)和C(分子式為C7H 6O3).C遇FeCl3水溶液顯紫色,與NaHCO3溶液反應有CO2產生.
請回答下列問題:
(1)化合物A中有三個含氧官能團,它們的名稱分別是羧基、羥基和.
(2)化合物B能發生的反應類型有.
a.水解反應 b.加成反應 c.縮聚反應 d.消去反應
化合物C能經下列反應得到G(分子式為C8H6O2,分子內含有五元環);
已知:(Ⅰ)RCOOHRCH2OH還原
(Ⅱ)R-BrR-COOH①NaCN②H+
(3)確認化合物C的結構簡式為.
(4)F→G反應的化學方程式為.
(5)化合物E有多種同分異構體,1H核磁共振譜圖表明,其中某些同分異構體含有苯環,且苯環上有兩種不同化學環境的氫,符合上述條件的E的同分異構體有種(不含E).
(6)寫出以苯乙烯(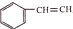 )為主要原料
)為主要原料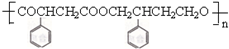 制備合成路線流程圖(無機試劑任選).合成路線流程圖示例如下:CH3CH2OHH2C=CH2濃硫酸170℃Br2
制備合成路線流程圖(無機試劑任選).合成路線流程圖示例如下:CH3CH2OHH2C=CH2濃硫酸170℃Br2 .組卷:4引用:1難度:0.5
.組卷:4引用:1難度:0.5 -
30.防治環境污染是當前環保工作的重要研究內容之一.二氧化硫和氮氧化物是大氣的主要污染物.
(1)將1.5mol SO2用氫氧化鈉溶液、石灰及氧氣處理后,假設硫元素不損失,理論上可得到g石膏(CaSO4?2H2O).
(2)用CH4消除NOx污染的化學方程式為:CH4+4NO→2N2+CO2+2H2O;CH4+2NO2→N2+CO2+2H2O
現有11.2L NO2、NO的混合氣體NOx,將其還原為N2,需要4.48L 的CH4,則混合氣體中NO2、NO的物質的量分別為.(體積都已換算為標準狀況)
(3)①常溫下用氧缺位鐵酸鋅ZnFe2Oy可以消除NOx污染,使NOx轉變為N2,同時ZnFe2Oy轉變為ZnFe2O4.若2mol ZnFe2Oy與足量NO2可生成0.5mol N2,則y=.
②氧缺位鐵酸鋅ZnFe2Oz化學式的氧化物形式為aZnO?bFeO?cFe2O3.已知1mol ZnFe2Oz最多能使4.0L(標況)NO1.4轉化為N2.則上述氧化物形式的化學式可具體表示為.
(4)低溫臭氧氧化脫硫脫硝技術可以同時吸收煙氣中的氮氧化物和二氧化硫,反應原理是將NOx氧化成N2O5,通過洗滌形成硝酸鹽,二氧化硫形成硫酸鹽.其主要反應如下:
①NO+O3→NO2+O2
②2NO2+O3→N2O5+O2
③N2O5+2NH3+H2O→2NH4NO3
④SO2+O3+2NH3+H2O→(NH4)2SO4+O2
某熱電廠煙氣中平均含NOx4.5‰、SO2 9.0‰(體積分數),壓縮空氣經臭氧發生器變成臭氧空氣,其中O3濃度為90L/m3,臭氧空氣與加濕氨氣和煙氣混合反應.若流量比為y,請通過計算列出y與x的關系式.V(臭氧空氣)V(煙氣)組卷:2引用:1難度:0.3


