2016-2017學年廣西南寧市賓陽中學高一(下)開學化學試卷(2月份)
發布:2024/4/20 14:35:0
一、選擇題(每小題只有一個正確選項,每題3分,共54分)
-
1.下列敘述錯誤的是( )
A.氧化鐵常用作紅色油漆和涂料 B.過氧化鈉可用于呼吸面具作為氧氣的來源 C.光導纖維的主要成分是硅酸鹽 D.常溫下可用鐵制或鋁制容器盛裝濃硫酸 組卷:26引用:4難度:0.9 -
2.Fe、FeO、Fe3O4的混合物中,加入100mL 2mol/L的鹽酸,恰好使混合物完全溶解,放出44.8mL(標準狀況)的氣體,所得溶液中加入KSCN溶液無血紅色出現,若用足量的CO在高溫下還原相同質量的此混合物,能得到鐵( )
A.2.8 g B.5.6 g C.11.2 g D.無法確定 組卷:49引用:2難度:0.9 -
3.將SO2和SO3兩種氣體的混合物通入BaCl2溶液,其結果是( )
A.只生成BaSO3沉淀,SO3從溶液中逸出 B.兩種氣體都被吸收,并有BaSO4沉淀生成 C.生成BaSO3和BaSO4兩種沉淀 D.只有BaSO4沉淀,SO2通入溶液中無沉淀生成 組卷:19引用:1難度:0.8 -
4.下列離子的檢驗方法合理的是( )
A.向某溶液中加入NaOH溶液,得紅褐色沉淀,說明溶液中含有Fe3+ B.向某溶液中滴入KSCN溶液呈紅色,說明不含Fe2+ C.向某溶液中通入Cl2,然后再加入KSCN溶液變紅色,說明原溶液中含有Fe2+ D.向某溶液中加入NaOH溶液得白色沉淀,又觀察到顏色逐漸變為紅褐色,說明該溶液中只含有Fe2+,不含有Mg2+ 組卷:98引用:7難度:0.5 -
5.某溫度下,將Cl2通入NaOH溶液中,反應得到NaCl、NaClO、NaClO3的混合液,經測定NaClO與NaClO3的物質的量之比為1:3,則Cl2與NaOH溶液反應時被還原的氯元素與被氧化的氯元素的物質的量之比為( )
A.3:11 B.11:3 C.1:4 D.4:1 組卷:57引用:6難度:0.9 -
6.下列有關鈉的物理性質的敘述中正確的是( )
①銀白色金屬;
②質軟,可以用小刀切割;
③熔點低于100℃;
④密度比水小;
⑤熱和電的良導體.A.①②④ B.①②③④ C.①③④ D.①②③④⑤ 組卷:2150引用:9難度:0.9 -
7.將鈉、鎂、鋁各0.3mol分別放入100mL 2mol?L-1的鹽酸中,同溫同壓下產生氣體的體積比是( )
A.1:1:1 B.3:2:2 C.1:2:3 D.6:3:2 組卷:73引用:3難度:0.7
二、填空題(共46分)
-
21.已知:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O.某強酸性溶液X含有Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-中的一種或幾種(不考慮水的電離和離子水解),取該溶液進行實驗,實驗內容如下:
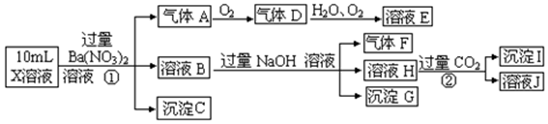
請回答下列問題:
(1)溶液X中除H+外肯定含有的離子是,無法確定是否含有的離子是
(2)沉淀G的化學式為,通常可以利用KClO在堿性條件下氧化G來制備一種新型、高效、多功能水處理劑K2FeO4.請寫出制備過程中的離子方程式
(3)寫出生成氣體F的離子方程式:
(4)經檢驗證實X中不含有(1)中無法確定的陽離子.若測定A、F、I均為0.01 mol,10 mL X溶液中
n(H+)=0.04 mol,沉淀C的物質的量為0.06mol,則上述(1)中無法確定的陰離子(填“存
在”或“不存在”),若不存在請說明理由,若存在請寫出其物質的量濃度.組卷:33引用:1難度:0.3 -
22.KClO3和濃鹽酸在一定溫度下反應會生成黃綠色的易爆物二氧化氯。其變化可表述為:
2KClO3+4HCl(濃)═2KCl+2ClO2↑+Cl2↑+2H2O
(1)該反應的氧化劑和還原劑之比是
(2)濃鹽酸在反應中顯示出來的性質是(填寫編號)。
①還原性 ②氧化性 ③酸性
(3)若產生標準狀況下體積為6.72L的氣體,則轉移的電子的物質的量為。組卷:84引用:1難度:0.5


