2021-2022學(xué)年湖南大學(xué)附中高二(上)期中化學(xué)試卷
發(fā)布:2024/12/10 7:0:1
一、選擇題:本題共10小題,每小題3分,共30分。在每小題給出的四個(gè)選項(xiàng)中,只有一項(xiàng)是符合題目要求的。
-
1.屬于離子化合物,且水溶液呈酸性的是( )
A.NH4Cl B.NaCl C.CH3COONa D.H2SO4 組卷:25引用:5難度:0.7 -
2.用鐵片與稀硫酸反應(yīng)制取氫氣時(shí),下列措施不能使氫氣生成速率加快的是( )
A.對(duì)該反應(yīng)體系適當(dāng)加熱 B.將稀硫酸改為98%的濃硫酸 C.滴加少量CuSO4溶液 D.鐵片改用鐵粉 組卷:25引用:3難度:0.9 -
 3.研究表明以MoS2為催化劑,在不同電解質(zhì)溶液中可實(shí)現(xiàn)常溫電催化合成氨,其反應(yīng)歷程與相對(duì)能量關(guān)系如圖所示(*表示具有活性的分子)。下列說(shuō)法不正確的是( )
3.研究表明以MoS2為催化劑,在不同電解質(zhì)溶液中可實(shí)現(xiàn)常溫電催化合成氨,其反應(yīng)歷程與相對(duì)能量關(guān)系如圖所示(*表示具有活性的分子)。下列說(shuō)法不正確的是( )A.兩種電解質(zhì)溶液環(huán)境下N2→2NH3的焓變相同 B.在Li2SO4溶液中MoS2對(duì)N2的活化效果好 C.N2的氫化是N≡N鍵斷裂與N—H鍵形成的過(guò)程 D.在Na2SO4溶液環(huán)境中決定合成氨反應(yīng)速率的步驟為*N2H2→*N2H3 組卷:17引用:3難度:0.5 -
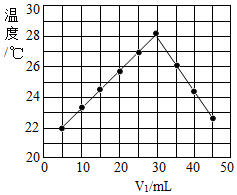 4.將V1 mL 1.0mol/L HCl溶液和V2 mL未知濃度的NaOH溶液混合均勻后測(cè)量并記錄溶液溫度,結(jié)果如圖所示(實(shí)驗(yàn)中始終保持V1+V2=50mL).下列敘述正確的是( )
4.將V1 mL 1.0mol/L HCl溶液和V2 mL未知濃度的NaOH溶液混合均勻后測(cè)量并記錄溶液溫度,結(jié)果如圖所示(實(shí)驗(yàn)中始終保持V1+V2=50mL).下列敘述正確的是( )A.做該實(shí)驗(yàn)時(shí)環(huán)境溫度為22℃ B.該實(shí)驗(yàn)表明化學(xué)能可以轉(zhuǎn)化為熱能 C.NaOH溶液的濃度約是1.00 mol/L D.該實(shí)驗(yàn)表明有水生成的反應(yīng)都是放熱反應(yīng) 組卷:182引用:46難度:0.7 -
5.用CuCl2?2H2O晶體制取無(wú)水CuCl2的實(shí)驗(yàn)裝置如圖所示,下列說(shuō)法不正確的是( )

A.先滴入濃硫酸,再點(diǎn)燃c處酒精燈 B.通入HCl可以抑制CuCl2的水解 C.裝置d中上層為苯,下層為NaOH溶液 D.硬質(zhì)玻璃管內(nèi)部右側(cè)會(huì)出現(xiàn)白霧 組卷:11引用:2難度:0.5 -
6.常溫下,濃度均為0.1mol/L的4種溶液pH如表:下列說(shuō)法正確的是( )
溶質(zhì) Na2CO3 NaHCO3 NaClO NaHSO3 pH 11.6 9.7 10.3 4.0 A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的濃度 B.四種溶液中,水的電離程度最大的是NaClO C.常溫下,相同物質(zhì)的量濃度的H2SO3、H2CO3、HClO,pH最大的是H2SO3 D.NaHSO3溶液中離子濃度大小順序?yàn)閏(Na+)>c(H+)>c(HSO3-)>c(SO32-)>c(OH-) 組卷:29引用:2難度:0.7
三、非選擇題:本題共4小題,共54分。考生根據(jù)要求作答。
-
17.綠色電源“直接二甲醚(CH3OCH3)燃料電池”的工作原理如圖1所示:

(1)H+的移動(dòng)方向?yàn)橛?(填“A”或“B”,下同)電極到電極。寫出A電極的電極反應(yīng)式:。
(2)SO2和NOx是主要大氣污染物,利用圖2裝置可同時(shí)吸收SO2和NO。
①a是直流電源的極。
②已知電解池的陰極室中溶液的pH在4~7之間,陰極的電極反應(yīng)為。
③用離子方程式表示吸收NO的原理。
(3)工業(yè)上,在強(qiáng)堿性條件下用電解法除去廢水中的CN-,裝置如圖3所示。依次發(fā)生的反應(yīng)有:
i.CN--2e-+2OH-═CNO-+H2O
ii.2Cl--2e-═Cl2↑
iii.3Cl2+2CNO-+8OH-═N2+6Cl-+2CO32-+4H2O
①除去1molCN-,外電路中至少需要轉(zhuǎn)移mol電子。
②為了使電解池連續(xù)工作,需要不斷補(bǔ)充。組卷:26引用:2難度:0.5 -
18.某小組研究FeCl3與Na2S的反應(yīng),設(shè)計(jì)了如下實(shí)驗(yàn):
Ⅰ.探究黑色沉淀的成分

實(shí)驗(yàn)a 實(shí)驗(yàn)b 實(shí)驗(yàn)c FeCl3
體積5 mL 10 mL 30 mL 實(shí)驗(yàn)
現(xiàn)象產(chǎn)生黑色渾濁,混合液pH=11.7 黑色渾濁度增大,混合液pH=6.8 黑色渾濁比實(shí)驗(yàn)b明顯減少,觀察到大量黃色渾濁物,混合液pH=3.7
查閱資料:Fe2S3(黑色)在空氣中能夠穩(wěn)定存在,F(xiàn)eS(黑色)在空氣中易變質(zhì)為Fe(OH)3
設(shè)計(jì)實(shí)驗(yàn):分別取實(shí)驗(yàn)a、b、c中沉淀放置于空氣中12小時(shí),a中沉淀無(wú)明顯變化。b、c中黑色沉淀部分變?yōu)榧t褐色。
(1)①同學(xué)甲認(rèn)為實(shí)驗(yàn)a中黑色沉淀為Fe2S3,實(shí)驗(yàn)b、c的黑色沉淀物中既有Fe2S3又有FeS,依據(jù)的實(shí)驗(yàn)現(xiàn)象是。
②同學(xué)乙認(rèn)為實(shí)驗(yàn)b的黑色沉淀物中有FeS則一定混有S,理由是。
③設(shè)計(jì)實(shí)驗(yàn)檢驗(yàn)b的黑色沉淀物中混有硫。
已知:硫在酒精溶液中的溶解度隨乙醇質(zhì)量分?jǐn)?shù)的增大而增大。
實(shí)驗(yàn)證明了b中黑色沉淀混有S,試劑a是,觀察到的現(xiàn)象為。
Ⅱ.探究實(shí)驗(yàn)a中Fe3+與S2-沒有發(fā)生氧化還原反應(yīng)的原因
經(jīng)查閱資料,可能的原因有兩種:
原因1:pH影響了Fe3+與S2-的性質(zhì),二者不能發(fā)生氧化還原反應(yīng)。
原因2:沉淀反應(yīng)先于氧化還原反應(yīng)發(fā)生,導(dǎo)致反應(yīng)物濃度下降,二者不能發(fā)生氧化還原反應(yīng)。
設(shè)計(jì)實(shí)驗(yàn):電極材料為石墨
(2)①試劑X和Y分別是、。
②甲認(rèn)為若右側(cè)溶液變渾濁,說(shuō)明Fe3+與S2-發(fā)生了氧化還原反應(yīng)。是否合理?說(shuō)明理由。
③乙進(jìn)一步實(shí)驗(yàn)證明該裝置中Fe3+與S2-沒有發(fā)生氧化還原反應(yīng),實(shí)驗(yàn)操作及現(xiàn)象是。
④由此得出的實(shí)驗(yàn)結(jié)論是。
Ⅲ.探究實(shí)驗(yàn)c隨著FeCl3溶液的增加,黑色沉淀溶解的原因
(3)①用離子方程式解釋實(shí)驗(yàn)1中的現(xiàn)象
實(shí)驗(yàn)1實(shí)驗(yàn)2 
固體溶解,聞到微量臭雞蛋氣味,溶液出現(xiàn)淡黃色渾濁。 、(寫離子方程式)。
、(寫離子方程式)。
②結(jié)合化學(xué)平衡等反應(yīng)原理及規(guī)律解釋實(shí)驗(yàn)2中現(xiàn)象相同與不同的原因。組卷:188引用:6難度:0.3


