2021-2022學年遼寧省沈陽二中高一(上)段考化學試卷(10月份)
發布:2024/11/12 19:0:1
一、選擇題(共15小題,每小題3分,滿分45分)
-
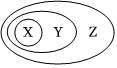 1.如圖表示了一些物質或概念之間的從屬或包含關系,不正確的是( )
1.如圖表示了一些物質或概念之間的從屬或包含關系,不正確的是( )X Y Z A CuSO4?5H2O 鹽 純凈物 B 膠體 分散系 混合物 C 堿性氧化物 氧化物 化合物 D 置換反應 氧化還原反應 離子反應 A.A B.B C.C D.D 組卷:40引用:6難度:0.9 -
2.證據推理是邏輯推理能力在化學學科中的重要表現形式,化學學科核心素養要培養證據推理的能力,下列推理正確的是( )
A.在同一化合物中,金屬元素顯正價,所以非金屬元素一定顯負價 B.Cu2+的氧化性比H+強,所以CuCl2和稀鹽酸的混合液中加入少量鐵屑時,可能沒有氣泡冒出 C.酸能使紫色石蕊溶液變紅,通入CO2后的紫色石蕊溶液變紅,所以CO2是酸 D.混合物都不是電解質,所以冰水混合物也不是電解質 組卷:46引用:6難度:0.8 -
3.下列說法正確的有幾項( )
①需要通電才可以進行的有:電離、電泳、電鍍、電解
②堿性氧化物均為金屬氧化物,酸性氧化物一定是非金屬氧化物
③葡萄糖溶液用一束強光照射可以發生丁達爾現象
④電解質溶液中自由移動離子數目越多導電能力一定越強
⑤把飽和三氯化鐵溶液滴入沸水中并充分攪拌可以制得氫氧化鐵膠體
⑥Na2O、CuO、FeO屬于堿性氧化物
⑦有單質參加的化合反應一定是氧化還原反應
⑧堿石灰、漂白粉、冰水混合物、明礬KAl(SO4)2?12H2O均為混合物
⑨金屬元素由化合態變成游離態一定是被還原A.1項 B.2項 C.3項 D.4項 組卷:52引用:2難度:0.6 -
 4.美國科學家用某有機分子和球形籠狀分子C60制成了“納米車”(如圖所示),每輛“納米車”是由一個有機分子和4個C60分子構成,直徑約6到9納米。下列說法正確的是( )
4.美國科學家用某有機分子和球形籠狀分子C60制成了“納米車”(如圖所示),每輛“納米車”是由一個有機分子和4個C60分子構成,直徑約6到9納米。下列說法正確的是( )A.用激光筆照射該物質分散在蒸餾水中形成的分散系,光線通過時出現明亮的光路 B.人們用肉眼可以清晰看到“納米車”的運動 C.C60是一種新型的化合物 D.C60與石墨不是同素異形體 組卷:18引用:5難度:0.8 -
5.某工業廢水中僅含下表離子中的5種:
某同學欲探究廢水的組成,進行了如下實驗:陽離子 K+、Cu2+、Fe3+、Ca2+、Fe2+ 陰離子 Cl-、 、CO2-3、NO-3、SO2-4SiO2-3
Ⅰ.取廢水少許加入足量鹽酸,無白色沉淀析出,但生成能使澄清石灰水變渾濁的無色無味氣體
Ⅱ.向Ⅰ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
下列推斷不正確的是( )A.溶液中一定含有的離子是K+、Cl-、 、CO2-3、NO-3SO2-4B.Ⅰ中加入鹽酸生成無色氣體的離子方程式是 +2H+═CO2↑+H2OCO2-3C.原溶液中的K+、Cl-、 存在與否無法確定NO-3D.Ⅱ中產生白色沉淀的離子方程式是Ba2++ ═BaSO4↓SO2-4組卷:79引用:5難度:0.7 -
6.下列說法正確的是( )
A.NaHCO3的電離方程式是NaHCO3═Na++H++ CO2-3B.向硫酸中通入少量氨氣,硫酸溶液的導電能力會明顯增強 C.膠體和其它分散系的本質區別是分散質粒子大小為1~100nm D.氧化還原反應的本質是元素化合價的變化 組卷:7引用:1難度:0.6
二、解答題
-
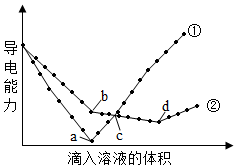 18.在兩份相同的Ba(OH)2溶液中,分別滴入相同濃度的H2SO4、NaHSO4溶液,其導電能力隨滴入溶液體積變化的曲線如圖所示。
18.在兩份相同的Ba(OH)2溶液中,分別滴入相同濃度的H2SO4、NaHSO4溶液,其導電能力隨滴入溶液體積變化的曲線如圖所示。
(1)圖中①、②代表滴加哪種溶液的變化曲線①。(填化學式)
(2)b點溶液中大量存在的離子是。
(3)a、d兩點對應的溶液均顯。(填“酸性”、“中性”、“堿性”)
(4)曲線①中的a點導電能力最弱的原因是。(用化學方程式表示)
(5)c點兩溶液中氫離子濃度①②。(填大于、小于或等于)
(6)曲線②中的c點顯(填“酸性”、“中性”、“堿性”)。
(7)曲線②中的b、d兩點對應所加溶液的體積比為。組卷:27引用:1難度:0.9 -
19.甘肅馬家窯遺址出土的青銅刀是我國最早冶煉的青銅器,由于時間久遠,其表面有一層“綠銹”,“綠銹”俗稱“銅綠”,是銅和空氣中的水蒸氣、CO2、O2作用產生的,化學式為Cu2(OH)2CO3,“銅綠”能跟酸反應生成銅鹽,CO2和H2O。
(1)物質分類標準看,“銅綠”屬于(填字母)。
A.酸
B.堿
C.鹽
D.氧化物
(2)銅器表面有時會生成銅綠,這層銅綠可用化學方法除去,試寫出用鹽酸除去銅綠而不損傷器物的反應的離子方程式。
(3)古代人們高溫灼孔雀石[Cu2(OH)2?CuCO3]和木炭的混合物得到一種紫紅色的金屬銅,其化學反應式為CuO+CCu+CO2↑,該反應屬于△(填序號)。
A.化合反應
B.置換反應
C.氧化還原反應
D.非氧化還原反應
(4)氧化亞銅(Cu2O)是一種鮮紅色粉末狀固體,幾乎不溶于水,可在酸酸性溶液中發生反應,與硫酸、鹽酸反應如下:Cu2O+H2SO4═CuSO4+Cu+H2O,該反應中氧化產物為。
(5)Cu2O+4HCl═2HCuCl2+H2O該反應(填“是”或“不是”)氧化還原反應。
(6)氧化還原反應中實際上包含氧化和還原兩個過程,下面是一個發生還原過程的反應式:+4H++3e-═NO↑+2H2O,將少量Cu2O放入稀硝酸中能使上述還原過程發生。NO-3
①上述反應中生成3個NO分子的同時,轉移電子數目為個。
②已知Cu2O被氧化為Cu(NO3)2,寫出Cu2O與稀硝酸反應的化學方程式,并標出電子轉移的方向和數目:。組卷:10引用:1難度:0.7


