2016-2017學(xué)年山東省棗莊市滕州市善國中學(xué)高三(上)第四周同步化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題
-
1.化學(xué)與生活密切相關(guān),下列有關(guān)說法錯誤的是( )
A.用灼燒的方法可以區(qū)分蠶絲和人造纖維 B.食用油反復(fù)加熱會產(chǎn)生稠環(huán)芳香烴等有害物質(zhì) C.加熱能殺死流感病毒是因為蛋白質(zhì)受熱變性 D.醫(yī)用消毒酒精中乙醇的濃度為95% 組卷:1905引用:35難度:0.9 -
 2.常溫下S2Cl2是橙黃色液體,其分子結(jié)構(gòu)如圖所示.少量泄漏會產(chǎn)生窒息性氣味,遇水易水解,并產(chǎn)生酸性懸濁液.下列關(guān)于S2Cl2的說法錯誤的是( )
2.常溫下S2Cl2是橙黃色液體,其分子結(jié)構(gòu)如圖所示.少量泄漏會產(chǎn)生窒息性氣味,遇水易水解,并產(chǎn)生酸性懸濁液.下列關(guān)于S2Cl2的說法錯誤的是( )A.為非極性分子 B.分子中既含有極性鍵又含有非極性鍵 C.與S2Br2結(jié)構(gòu)相似,熔沸點S2Br2>S2Cl2 D.與水反應(yīng)的化學(xué)方程式可能為2S2Cl2+2H2O→SO2↑+3S↓+4HCl 組卷:213引用:16難度:0.7 -
3.某物質(zhì)的實驗式為PtCl4?2NH3,其水溶液不導(dǎo)電,加入AgNO3溶液反應(yīng)也不產(chǎn)生沉淀,以強堿處理并沒有NH3放出,則關(guān)于此化合物的說法中正確的是( )
A.配合物中中心原子的電荷數(shù)和配位數(shù)均為6 B.該配合物可能是平面正方形結(jié)構(gòu) C.Cl-和NH3分子均與Pt4+配位 D.配合物中Cl-與Pt4+配位,而NH3分子不配位 組卷:160引用:34難度:0.7 -
4.NA代表阿伏加德羅常數(shù).下列說法正確的是( )
A.8.0gCuO和Cu2S的混合物含銅原子個數(shù)為0.2NA B.標(biāo)準(zhǔn)狀況下,11.2 L乙醇蒸氣含共價鍵數(shù)目為4NA C.1mol K與O2完全反應(yīng)生成K2O、K2O2、KO3的混合物,轉(zhuǎn)移電子數(shù)為NA D.1L 0.2 mol?L-1 NH4ClO4溶液中含NH4+數(shù)目為0.2NA 組卷:14引用:3難度:0.9 -
5.下列離子方程式書寫正確的是( )
A.向NaHSO4溶液中滴Ba(OH)2溶液,恰好使 沉淀完全:2H++SO2-4+Ba2++OH-═H2O+BaSO4↓SO2-4B.向FeI2溶液中通入少量氯氣:2Fe2++Cl2═2Fe3++2Cl- C.加熱可增強純堿溶液去污力: +2H2O?H2CO3+2OH-CO2-3D.過量CO2通入Ca(ClO)2溶液中:ClO-+CO2+H2O═ +HClOHCO-3組卷:37引用:5難度:0.7 -
6.可以大量共存的離子組是( )
A.Na+、Fe2+、NO3-、Cl- B.K+、HCO3-、SO42-、OH- C.ClO-、Cl-、Na+、H+ D.Ba2+、K+、SO42-、H+ 組卷:44引用:9難度:0.7 -
7.下列指定反應(yīng)的離子方程式正確的是( )
A.MnO2與濃鹽酸混合加熱:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O△B.(NH4)2Fe(SO4)2溶液中加入過量的NaOH溶液:Fe2++2OH-=Fe(OH)2↓ C.Ba(HCO3)2溶液中加入稀硫酸:Ba2++SO =BaSO4↓2-4D.H2C2O4(弱酸)溶液中加入酸性KMnO4溶液:2MnO +5H2C2O4=2Mn2++10CO2↑+2H2O+6OH--4組卷:5引用:3難度:0.9 -
8.在Zn+HNO3→Zn(NO3)2+NH4NO3+H2O的反應(yīng)中,如果2mol Zn完全起反應(yīng),則被還原的HNO3的物質(zhì)的量是( )
A.0.5mol B.1mol C.2mol D.5mol 組卷:7引用:2難度:0.7 -
9.一定條件下硝酸銨受熱分解的化學(xué)方程式為:5NH4NO3═2HNO3+4N2↑+9H2O,在反應(yīng)中被氧化與被還原的氮原子數(shù)之比為( )
A.1:1 B.5:4 C.5:3 D.3:5 組卷:224引用:128難度:0.7 -
10.在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1mol的混合溶液中加入0.1mol鐵粉,充分?jǐn)嚢韬箬F完全反應(yīng),同時析出0.1mol Ag.則下列結(jié)論中不正確的是( )
A.向反應(yīng)后的溶液中繼續(xù)加入少量鐵粉,鐵粉可以繼續(xù)溶解 B.氧化性:Ag+>Fe3+>Cu2+>Zn2+ C.反應(yīng)后溶液的質(zhì)量減輕 D.反應(yīng)后溶液中Cu2+與Fe2+的物質(zhì)的量之比為1:1 組卷:59引用:12難度:0.7
三、實驗題
-
29.活性氧化鋅常用作橡膠制品的硫化活性劑。工業(yè)上用粗氧化鋅(含少量CuO、FeO、MnO、Fe2O3等)生產(chǎn)活性氧化鋅,生產(chǎn)工藝流程如圖:

根據(jù)上表提供的信息,回答下列問題:Fe(OH)2 Fe( OH)3 Cu(OH)2 Zn(OH)2 Mn(OH)2 開始沉淀的pH 7.5 2.2 5.2 6.4 8.6 沉淀完全的pH 9.0 3.2 6.7 8.0 10.1
(1)“廢渣1”的主要成分是。
(2)完成“反應(yīng)器2”中反應(yīng)之一的離子方程式:MnO-4+Mn2++=MnO2↓+H+
(3)蘸取“反應(yīng)器2”中的溶液點在試紙上,如果觀察到試紙變藍(lán),說明KMnO4過量。
(4)“廢渣2”分離出的MnO2可用于制取MnO,已知:
2MnO2(s)+C(s)═2MnO(s)+CO2(g)△H=-174.6kJ?mol-1
C(s)+CO2(g)═2CO(g)△H=+283.0kJ?mol-1
試寫出MnO2(s)與CO(g)反應(yīng)制取MnO(s)的熱化學(xué)方程式:。
(5)“反應(yīng)器3”中加入鋅粉的作用是。
(6)“反應(yīng)器4”得到的廢液中,含有的主要離子除了Na+外,還有。
(7)從“反應(yīng)器4”中經(jīng)過濾等操作得到堿式碳酸鋅。取堿式碳酸鋅3.41g,在400~450℃下加熱至恒重,得到ZnO 2.43g和標(biāo)準(zhǔn)狀況下CO2 0.224L,堿式碳酸鋅的化學(xué)式。組卷:2引用:1難度:0.4 -
30.某同學(xué)設(shè)計如圖所示的實驗方案:
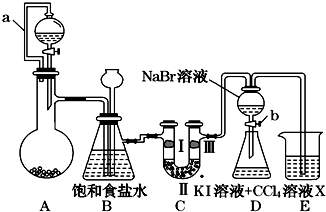
(1)A裝置的分液漏斗里盛裝濃鹽酸,燒瓶里固體為重鉻酸鉀(K2Cr2O7),還原產(chǎn)物是CrCl3,寫出A中離子方程式:.
(2)本實驗?zāi)康氖?!--BA-->,B裝置有幾個作用,分別是除去氯氣中的氯化氫、.拆去a導(dǎo)管的后果可能是.
(3)裝置C的功能是探究有氧化性的物質(zhì)是否一定有漂白性,下列最佳試劑組合是.
(4)證明溴的非金屬性比碘強的實驗操作和現(xiàn)象是① ② ③ ④ Ⅰ 濕潤的紅紙條 干燥的紅紙條 干燥的紅紙條 濕潤的紅紙條 Ⅱ 堿石灰 濃硫酸 硅膠 氯化鈉 Ⅲ 濕潤的紅紙條 干燥的紅紙條 干燥的白紙條 干燥的紅紙條 .
(5)D裝置進行實驗時存在明顯不足,它是,合適的溶液X是(從①氫氧化鈉溶液②亞硫酸鈉溶液③亞硫酸氫鈉溶液④氯化亞鐵溶液⑤硫氫化鈉溶液⑥碳酸氫鈉溶液中選擇).組卷:276引用:5難度:0.5


