2019-2020學年新疆烏魯木齊八中高一(上)第二次月考化學試卷
發布:2024/4/20 14:35:0
一、選擇題(共21小題,每題2分,共42分。每小題只有一個選項符合題意)
-
1.下列說法中不正確的是( )
①將硫酸鋇放入水中不能導電,硫酸鋇是非電解質;
②氨溶于水得到氨水溶液能導電,氨水是電解質;
③固態氯化氫不導電,液態氮化氫可以導電;
④硫酸氫鈉電離出的陽離子有H+,硫酸氫鈉是酸:
⑤電解質放在水中一定能導電,非電解質放在水中一定不導電。A.僅①④ B.僅①④⑤ C.僅②③ D.①②③④⑤ 組卷:27引用:4難度:0.6 -
2.下列關于氧化還原反應的敘述,正確的是( )
A.有一種元素被氧化,肯定有另一種元素被還原 B.在反應中不一定所有元素的化合價都發生變化 C.置換反應和復分解反應不可能是氧化還原反應 D.化合反應和置換反應一定是氧化還原反應 組卷:1引用:1難度:0.7 -
3.下列分類標準不正確的是( )
A.化學反應分為:氧化還原反應、非氧化還原反應(標準:是否有電子的轉移) B.分散系分為:溶液、膠體、濁液(標準:能否產生丁達爾效應) C.純凈物分為:單質、化合物(標準:組成物質的元素種數) D.化合物分為:電解質、非電解質(標準:溶于水或熔融狀態能否導電的化合物) 組卷:212引用:20難度:0.7 -
4.下列括號中的分離方法運用得當的是( )
A.植物油和自來水(蒸餾) B.水溶液中的食鹽和碘(分液) C.BaSO4和CaCl2(溶解、過濾、蒸發) D.自來水中的雜質(萃取) 組卷:2引用:1難度:0.8 -
5.在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-離子完全沉淀;如加入足量強堿并加熱可得到c mol NH3,(已知NH4++OH-
NH3↑+H2O)則原溶液中的Al3+的物質的量濃度(mol?L-1)為( )△A. 2b-c2aB. 2b-caC. 2b-c3aD. 2b-c6a組卷:123引用:105難度:0.7 -
6.有關化學實驗的下列操作中,一般情況下不能相互接觸的是( )
A.過濾操作中,玻璃棒與三層濾紙 B.過濾操作中,漏斗頸與燒杯內壁 C.分液操作中,分液漏斗頸與燒杯內壁 D.用膠頭滴管向試管滴液體時,滴管尖端與試管內壁 組卷:150引用:62難度:0.9 -
7.某無色溶液能與Al反應放出H2,下列離子一定能在該溶液中大量共存的是( )
A.H+、 、NH+4、Fe2+NO-3B.Na+、 、K+、Cl-SO2-4C.Ba2+、OH-、 、AlO-2SO2-3D.Al3+、Mg2+、 、ClO-SiO2-3組卷:6引用:5難度:0.9 -
8.常溫常壓下,2.2g CO2氣體的摩爾質量是( )
A.0.05 g/mol B.0.5 mol C.44 g D.44 g/mol 組卷:13引用:6難度:0.9 -
9.將2.3g金屬鈉放入100g水中,完全反應后溶液中溶質的質量分數為( )
A. 4100+2.3×100%B. 2.3100+4-1.8×100%C. 4100+4×100%D. 4100+2.3-0.1×100%組卷:411引用:10難度:0.7
二、非選擇題,共58分。
-
27.如圖所示,一密閉容器被無摩擦、可滑動的兩隔板a和b分成甲、乙兩室.標準狀況下,在乙室中充入0.6molHCl,甲室中充入NH3、H2的混合氣體,靜止時活塞位置下圖.已知甲、乙兩室中氣體的質量之差為10.9g.
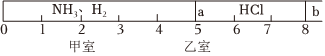
請回答下列問題:
(1)甲室中氣體的物質的量為mol.
(2)甲室中氣體的質量為g.
(3)甲室中NH3、H2的物質的量之比為,質量比為.
(4)經過查資料知道HCl+NH3=NH4Cl(NH4Cl常溫下是固體),如果將板a去掉,當HCl與NH3完全反應后,活塞b將靜置于刻度“”處(填數字).組卷:81引用:7難度:0.5 -
28.(1)向mg鎂和鋁的混合物中加入適量的稀硫酸,恰好完全反應生成標準狀況下的氣體bL。向反應后的溶液中加入c mol/L氫氧化鉀溶液V mL,使金屬離子剛好沉淀完全,得到的沉淀質量為n g。再將得到的沉淀灼燒至質量不再改變為止,得到固體p g。則下列關系不正確的是
。
A.p=m+b1.4
B.p=m+2Vc125
C.n=m+17Vc1000
D.n=m+17b11.2
(2)一定體積的KMnO4溶液恰好能氧化一定質量的KHC2O4?H2C2O4?2H2O。若用0.1000mol?L-1的NaOH溶液中和相同質量的KHC2O4?H2C2O4?2H2O,所需NaOH溶液的體積恰好為KMnO4溶液的3倍,則KMnO4溶液的濃度(mol?L-1)為。
提示:①H2C2O4是二元弱酸
②10KHC2O4?H2C2O4+8KMnO4+17H2SO4═8MnSO4+9K2SO4+40CO2↑+32H2O組卷:5引用:1難度:0.4


