2021-2022學年廣西玉林市五校聯考高二(上)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題共7小題,每小題0分。在每小題給出的四個選項中,只有一項是符合題目要求的)
-
1.化學與生產、生活密切相關。下列有關物質的用途、性質都正確且有相關性的是( )
選項 用途 性質 A 液氨作制冷劑 NH3分解生成N2和H2的反應是吸熱反應 B NH4Fe(SO4)2?12H2O常作凈水劑 NH4Fe(SO4)2?12H2O具有氧化性 C 漂粉精可以作環境消毒劑 漂粉精溶液中ClO-和HClO都有強氧化性 D Al2O3常作耐高溫材料 Al2O3既能與強酸反應,又能與強堿反應 A.A B.B C.C D.D 組卷:114引用:6難度:0.6 -
2.NA是阿伏加德羅常數的值。下列說法正確的是( )
A.常溫下1L0.1mol?L-1Na2CO3溶液中含0.1NA個 CO2-3B.0.1molNa2O2與足量水反應轉移0.1NA個電子 C.0.1molCH4與Cl2在光照下反應生成的CH3Cl分子數為0.1NA D.標準狀況下,22.4LNO2中含NA個分子 組卷:5引用:2難度:0.6 -
3.下列說法正確的是( )
A.常溫下,加水稀釋0.1mol?L-1醋酸溶液,溶液中所有離子濃度均減少 B.升高溫度和增大濃度都可以提高反應體系內活化分子百分數 C.常溫下,反應C(s)+CO2(g)=2CO(g)不能自發進行,則該反應的ΔH>0 D.在稀溶液中:H+(aq)+OH-(aq)=H2O(1)ΔH=-57.3kJ?mol-1,若將含1molCH3COOH與含1molNaOH的溶液混合,放出的熱量等于57.3kJ 組卷:3引用:2難度:0.5
二、必考題(共129分)
-
10.二氧化氯(ClO2)是一種黃綠色氣體,易溶于水,在混合氣體中的體積分數大于10%就可能發生爆炸,在工業上常用作水處理劑、漂白劑。回答下列問題:
(1)在處理廢水時,ClO2可將廢水中的CN-氧化成CO2和N2,寫出該反應的離子方程式:。
(2)某小組按照文獻中制備ClO2的方法設計了如圖所示的實驗裝置用于制備ClO2。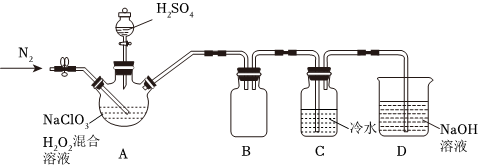
①通入氮氣的主要作用有2個,一是可以起到攪拌作用,二是。
②裝置B的作用是。
③當看到裝置C中導管液面上升時應進行的操作是。
(3)測定裝置C中ClO2溶液的濃度:取10mLC中溶液于錐形瓶中,加入足量的KI溶液和H2SO4酸化,然后加入作指示劑,用0.1000mol?L-1的Na2S2O3標準液滴定錐形瓶中的溶液(I2+2S2=2I-+S4O2-3),當看到O2-6現象時,測得標準液消耗的體積為20.00mL,通過計算可知C中ClO2溶液的濃度為mol?L-1。
(4)下列操作使測定結果偏高的是。
A.滴定前平視,滴定終點俯視讀數
B.盛放Na2S2O3標準溶液的滴定管未用標準液潤洗
C.硫酸酸化的KI溶液在空氣中靜置時間過長
D.滴定前正常,滴定后滴定管尖嘴內有氣泡組卷:5引用:3難度:0.5 -
11.(1)21世紀是鈦的世界,納米材料二氧化鈦(TiO2)具有很高的化學活性,可做性能優良的催化劑。工業上二氧化鈦的制備是:
I.將干燥后的金紅石(主要成分TiO2,主要雜質SiO2)與碳粉混合裝入氯化爐中,在高溫下通入Cl2反應制得混有SiCl4雜質的TiCl4。資料卡片 物質 熔點 沸點 SiCl4 -70℃ 57.6℃ TiCl4 -25℃ 136℃
II.將SiCl4分離,得到純凈的TiCl4,所采取的操作名稱是
III.用TiCl4制備TiO2?xH2O的化學方程式為,制備時需要,促進水解趨于完全。
IV.TiO2?xH2O高溫分解得到TiO2.如在實驗室中進行,則需在(填儀器名稱)中加熱。
(2)亞硫酰氯(SOCl2)是一種液態化合物,沸點為77℃,在農藥制藥等領域用途廣泛。SOCl2遇水劇烈反應,液面上有白霧形成,并有帶刺激性氣味的氣體逸出,該氣體可使品紅溶液褪色。
根據上述實驗,寫出SOCl2與水反應的化學方程式
AlCl3溶液蒸干灼燒得不到無水AlCl3,而用SOCl2與AlCl3?6H2O混合共熱,可得無水AlCl3,其原因是組卷:6引用:2難度:0.5


