人教版(2019)選擇性必修1《第七單元 鹽類的水解及沉淀溶解平衡》2023年單元測試卷(A卷)
發布:2024/8/16 13:0:1
一、選擇題
-
1.我國古代染坊常用某種“堿劑”來精煉絲綢,該“堿劑”的主要成分是一種鹽,能促進蠶絲表層絲膠蛋白雜質水解而除去。這種“堿劑”的主要成分可能是( )
A.食鹽 B.燒堿 C.純堿 D.膽礬 組卷:38引用:5難度:0.6 -
2.磷酸鈣可制作糖漿澄清劑、塑料穩定劑等。已知常溫下,在含有Ca3( PO4)2的懸濁液中c(Ca2+)=2.0×10-6mol?L-1,c(PO43-)=2.0×10-6mol?L-1,則常溫下Ca3(PO4)2的Ksp為( )
A.2.0×10-29 B.3.2×10-29 C.6.3×10-18 D.5.1×10-27 組卷:18引用:2難度:0.7 -
3.下列溶液的酸堿性及對應的解釋均正確的是( )
選項 溶液 酸堿性 解釋 A Fe2(SO4)3溶液 酸性 Fe3++3H2O?Fe(OH)3↓+3H+ B Na2S溶液 堿性 S2-+2H2O?H2S+2OH- C NH4Cl溶液 堿性 NH4++H2O?NH3?H2O+H+ D NaHCO3溶液 堿性 HCO3-+H2O?H2CO3+OH- A.A B.B C.C D.D 組卷:15引用:2難度:0.6 -
4.滴有酚酞試液的下列溶液,經如下操作后溶液顏色變深的是( )
A.碳酸鈉溶液中滴入鹽酸 B.水中加入鈉 C.氨水中加入少量NH4Cl 固體 D.醋酸溶液微熱 組卷:7引用:1難度:0.9 -
5.化學與生產、生活密切相關.下列應用與鹽類水解無關的是( )
A.常用熱的純堿溶液清洗餐具上的油污 B.“84”消毒液能漂白有色物質 C.常用消石灰改良酸性土壤 D.明礬、硫酸鐵常用于凈水 組卷:9引用:1難度:0.9 -
6.工業上可通過如圖所示流程回收鉛酸蓄電池中的鉛,下列有關說法不正確的是( )
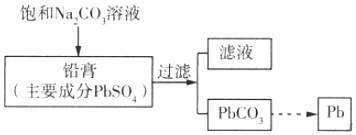
A.PbSO4在水中存在沉淀溶解平衡:PbSO2(s)?Pb2+(aq)+SO42-(aq) B.生成PbCO3的離子方程式為PbSO4 (s)+CO32-(aq)═PbCO3(s)+SO42-(aq) C.pH:濾液<飽和Na2CO3溶液 D.濾液中Pb2+濃度為0 組卷:15引用:2難度:0.5
三、解答題
-
19.常溫下,幾種物質的溶度積常數見下表:
(1)某酸性CuCl2溶液中含少量的FeCl3,為制得純凈CuCl2溶液,宜加入物質 Cu(OH)2 Fe(OH)3 CuCl CuI Ksp 2.2×10-20 2.6×10-39 1.7×10-7 1.3×10-12 ,將溶液調至pH=4,使Fe3+轉化為Fe(OH)3沉淀,此時溶液中的c(Fe3+)=mol?L-1。
(2)上述溶液過濾后,將所得濾液經過、(按操作順序填寫實驗步驟的名稱),再經過濾,可得到CuCl2?2H2O晶體。
(3)某學習小組用“間接碘量法”測定含有CuCl2?2H2O晶體的試樣(不含能與I-發生反應的氧化性雜質)的純度,過程如下:取0.800g試樣溶于水,加入適當過量的KI固體,充分反應,生成白色沉淀。用0.100 0mol?L-1Na2S2O3標準溶液滴定,到達滴定終點時,消耗Na2S2O3標準溶液40.00mL(已知:I2+2S2O32-═S4O62-+2I- )。
①可選用作滴定指示劑,滴定終點的現象是。
②CuCl2溶液與KI反應的離子方程式為。
③含有CuCl2?2H2O晶體的試樣的純度是。組卷:79引用:3難度:0.5 -
20.某化工廠廢水(pH=2.0,ρ≈1g?mL-1)中含有Ag+、Pb2+等重金屬離子,其濃度各約為0.01mol?L-1.排放前擬用沉淀法除去這兩種離子,查找有關數據如表:
(1)你認為往廢水中投入難溶電解質 AgI PbI2 AgOH Pb(OH)2 Ag2S PbS Ksp 8.3×10-17 7.1×10-9 5.6×10-8 1.2×10-15 6.3×10-50 3.4×10-28 (填序號),Ag+、Pb2+沉淀效果最好。
a.KI b.NaOH c.Na2S
(2)常溫下,如果用NaOH處理上述廢水,使溶液的pH=9.0,處理后的廢水中c(Pb2+)=。
(3)如果用食鹽處理只含Ag+的廢水,測得處理后的廢水(ρ≈1g?mL-1)中NaCl的質量分數為0.117%.若排放標準要求為c(Ag+)低于1.0×10-8mol?L-1,已知Ksp(AgCl)=1.8×10-10mol?L-2,問該工廠處理后的廢水中c(Ag+)=,是否符合排放標準(填“是”或“否”)。組卷:74引用:2難度:0.4


