新人教版九年級下冊《第11章 鹽 化肥》2021年單元測試卷(重慶八中)
發布:2024/4/20 14:35:0
一、選擇題(本題包括16個小題,每題2分,共32分)每小題只有一個選項符合題意。
-
1.下面有關鹽的用途是利用其化學性質的是( )
A.小蘇打治療胃酸過多 B.大理石做華表 C.硫酸鋇做鋇餐 D.食鹽配制生理鹽水 組卷:55引用:1難度:0.8 -
2.小明想施用鉀肥.使作物生長茁壯、莖桿粗硬、增加抗倒伏能力,他應該選用( )
A.磷酸二氫鈣 B.硝酸銨 C.碳酸鉀 D.硝酸鉀 組卷:7引用:2難度:0.9 -
3.下列物質的名稱、俗名與化學式完全對應的是( )
A.氯化鈉、食鹽、NaCl2 B.碳酸氫鈉、純堿、NaHCO3 C.氫氧化鈉、苛性鈉、NaOH D.氫氧化鈣、消石灰、CaO 組卷:9引用:2難度:0.6 -
4.下列實驗操作正確的是( )
A. 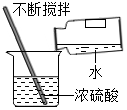
稀釋濃硫酸B. 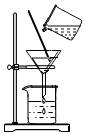
C. 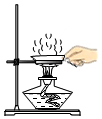
D. 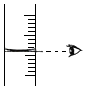 組卷:17引用:1難度:0.7
組卷:17引用:1難度:0.7 -
5.下列物質分類正確的一組是( )
A.混合物:空氣、冰水共存物、天然氣 B.氧化物:干冰、雙氧水、赤鐵礦 C.堿:燒堿、生石灰、氨水 D.鹽:純堿、小蘇打、高錳酸鉀 組卷:6引用:1難度:0.6 -
6.亞硝酸鈉(NaNO2)常作為食品添加劑在肉制品中使用,其主要作用是保持肉制品的亮紅色澤,抑菌和增強風味,但過量或長期食用對人體健康會造成危害。亞硝酸鈉中氮元素的化合價為( )
A.-3 B.+1 C.+3 D.+5 組卷:60引用:2難度:0.5 -
7.下列各組固體物質,只用水無法鑒別的是( )
A.FeSO4和Na2SO4 B.NaCl和KCl C.Na2CO3和CaCO3 D.NaOH和NH4NO3 組卷:140引用:4難度:0.6 -
8.下列化學方程式正確的是( )
A.Cu+2AgCl═CuCl2+2Ag B.2Fe+6HCl═2FeCl3+2H2↑ C.CaCl2+H2O+CO2═CaCO3↓+2HCl D.2AgNO3+BaCl2═2AgCl↓+Ba(NO3)2 組卷:19引用:3難度:0.6
三、實驗題(本大題包括2個題,共11分)
-
23.某化學小組同學完成鹽的性質實驗后,處理廢液時將過量的碳酸鈉溶液與硫酸銅溶液混合,發現產生了藍色沉淀,小組同學在老師的指導下對該沉淀的成分進行了探究。
【提出問題】過量的碳酸鈉溶液與硫酸銅溶液混合產生的沉淀是什么?
【作出猜想】①甲同學猜想該沉淀為CuCO3.理由是:(用化學方程式表示)。
②乙同學猜想該沉淀為Cu(OH)2.理由:碳酸鈉溶液呈(填“酸”或“堿”)性。
③根據甲、乙同學的猜想,丙同學認為該沉淀為CuCO3和Cu(OH)2。
【查閱資料】①Cu(OH)2、CuCO3受熱易分解,均生成兩種氧化物。
②Cu(OH)2的分解溫度為66℃~68℃;CuCO3的分解溫度為200℃~220℃。
③無水CuSO4為白色固體,遇水變藍。
【進行實驗】
(1)固體的獲取將反應后的固液混合物經 過濾、洗滌、低溫烘干后得藍色固體。
討論:①低溫烘干的原因:,②判斷固體已洗凈的方法和現象是。
(2)固體成分的定性探究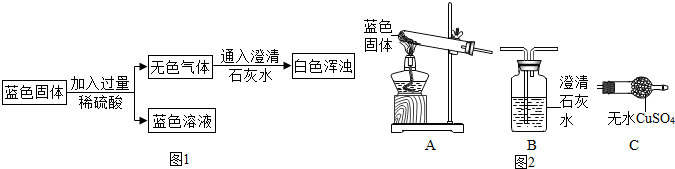
①甲同學用如圖1方案進行實驗,根據所得到的現象。甲同學認為他的猜想是正確的。
②乙同學利用如圖2裝置進行實驗。
乙同學通過實驗得出丙同學的猜想成立,其實驗時裝置的正確連接順序為(填字母序號)。
(3)固體成分的定量測定
丙同學對固體進行熱分解,獲得相關數據,繪成固體質量變化與分解溫度關系圖,如圖3所示。該固體中Cu(OH)2與CuCO3的質量比為。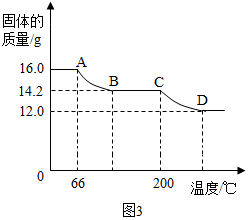
【實驗反思】
結合上述實驗,下列說法正確的是(填數字序號)。
①甲同學的實驗不能證明其猜想成立
②甲同學實驗過程中所得藍色溶液的溶質為CuSO4
③乙同學實驗過程中,觀察到C中白色固體變藍,B中澄清石灰水變渾濁
④丙同學實驗中C點所得固體為CuCO3。組卷:102引用:3難度:0.5
四、計算題(本大題包括1個題,共6分)
-
24.工業上侯氏制堿法制得的純堿產品中常含有少量的氯化鈉雜質,化驗員要對每批次的純堿產品進行檢驗.在實驗室中取27g純堿樣品,平均分成五份依次加入到盛有100g稀鹽酸的錐形瓶中(錐形瓶的質量為60g),每次充分反應后都進行稱量,得到的實驗數據如表:
(1)第一次加入純堿樣品充分反應后,生成二氧化碳的質量是第一次 第二次 第三次 第四次 第五次 加入純堿樣品的質量/g 5.4 5.4 5.4 5.4 5.4 電子天平的示數/g 163.2 166.4 169.6 175 180.4 g.
(2)第次加入純堿樣品后恰好與100g稀鹽酸完全反應,此時共反應純堿樣品g.
(3)計算純堿樣品中碳酸鈉的質量分數是多少?(計算結果精確到0.1%)組卷:53引用:3難度:0.5


