2022-2023學年湖南省長沙市雅禮中學高二(上)入學化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題共12小題,每小題3分,共36分;在每小題給出的四個選項中,只有一項是符合題目要求的)
-
1.下列生活用品中主要由合成纖維制造的是( )
A.尼龍繩 B.宣紙 C.羊絨衫 D.棉襯衣 組卷:1670引用:43難度:0.9 -
2.化學無處不在,與化學有關的說法不正確的是( )
A.侯氏制堿法的工藝過程中應用了物質溶解度的差異 B.可用蘸濃鹽酸的棉棒檢驗輸送氨氣的管道是否漏氣 C.碘是人體必需微量元素,所以要多吃富含高碘酸的食物 D.二氧化氮的排放會導致光化學煙霧和酸雨的產生 組卷:9引用:1難度:0.6 -
3.飄塵是物質燃燒時產生的粒狀漂浮物,顆粒很小,不易沉降。它與空氣中的SO2和O2接觸時,SO2會部分轉化為SO3,使空氣的酸度增加,環境污染更為嚴重。其中飄塵所起的作用可能是( )
A.氧化劑 B.還原劑 C.催化劑 D.載體 組卷:398引用:22難度:0.9 -
4.高純度晶硅是典型的無機非金屬材料,又稱“半導體”材料。它的發現和使用曾引起計算機的一場“革命”。它可以按下列方法制備:下列說法不正確的是( )

A.步驟①的化學方程式為:SiO2+C Si+CO2↑高溫B.步驟①中每生成1mol Si,轉移4mol電子 C.高純硅是制造太陽能電池的常用材料,二氧化硅是制造光導纖維的基本原料 D.SiHCl3(沸點33.0℃)中含有少量的SiCl4(沸點67.6℃),通過蒸餾(或分餾)可提純SiHCl3 組卷:92引用:3難度:0.9 -
5.用下列兩種途徑制取H2SO4,某些反應條件和產物已省略,下列有關說法不正確的是( )
途徑①:SH2SO4濃HNO3
途徑②:SSO2O2SO3O2H2SO4.H2OA.途徑②與途徑①相比較更能體現“綠色化學”的理念,因為途徑②比途徑①的污染相對較小且原子利用率較高 B.由途徑①和②分別制取1 mol H2SO4,理論上各消耗1 mol S,各轉移6 mol電子 C.途徑①反應中體現了濃HNO3的強氧化性和酸性 D.途徑②的第二步反應在實際生產中可以通過增大O2的濃度來提高SO2的轉化率 組卷:130引用:2難度:0.7 -
6.NA為阿伏加德羅常數的值。下列說法正確的是( )
A.18gD2O和18gH2O中含有的質子數均為10NA B.1molBrCl與H2O完全反應生成氯化氫和次溴酸,轉移的電子數為NA C.過氧化鈉與水反應時,生成0.1mol氧氣轉移的電子數為0.2NA D.密閉容器中2molNO與1molO2充分反應,產物的分子數為2NA 組卷:64引用:1難度:0.7
三、填空題(此題包括4小題,共48分)
-
19.氨在工農業生產中應用廣泛,可由N2、H2合成NH3。
(1)天然氣蒸汽轉化法是前獲取原料氣中H2的主流方法。CH4經過兩步反應完全轉化為H2和CO2,其能量變化示意圖如圖: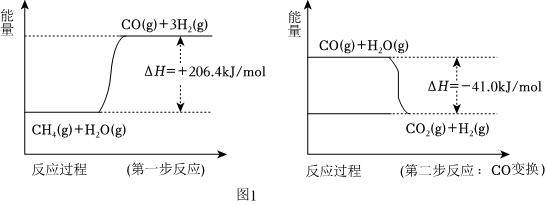
結合圖象,寫出CH4通過蒸汽轉化為CO2和H2的熱化學方程式。
(2)利用透氧膜,一步即獲得N2、H2,工作原理如圖2所示(空氣中N2與O2的物質的量之比按4:1計)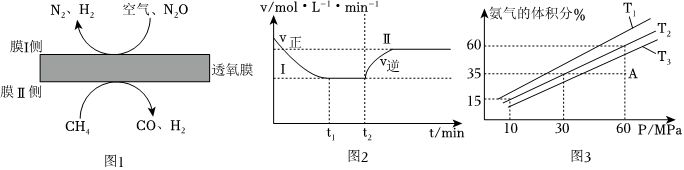
①起還原作用的物質是。
②膜I側所得氣體=2,CH4、H2O、O2反應的化學方程式是n(H2)n(N2)。
(3)甲小組模擬工業合成氨在一恒溫恒容的密閉容器中發生如下反應:N2(g)+3H2(g)?2NH3(g)△H<0.t1時刻到達平衡后,在t2時刻改變某一條件,其反應過程如圖3所示,下列說法正確的是
A.Ⅰ、Ⅱ兩過程到達平衡時,平衡常數:KⅠ<KⅡ
B.Ⅰ、Ⅱ兩過程到達平衡時,NH3的體積分數:Ⅰ<Ⅱ
C.Ⅰ、Ⅱ兩過程到達平衡的標志:混合氣體密度不再發生變化
D.t2時刻改變的條件可以是向密閉容器中加N2和H2混合氣
(4)乙小組模擬不同條件下的合成氨反應,向容器充入9.0mol N2 和23.0mol H2,圖4為不同溫度下平衡混合物中氨氣的體積分數與總壓強(P )的關系圖。
①T1、T2、T3由大到小的排序為。
②在T2、60MPa條件下,比較A點v正v逆(填“>”、“<”或“=”),理由是。
③計算T2、60Mpa平衡體系的平衡常數Kp=。(用平衡分壓代替平衡濃度計算,分壓=總壓x物質的量分數)組卷:25引用:3難度:0.6 -
20.近期發現,H2S是繼NO、CO之后的第三個生命體系氣體信號分子,它具有參與調節神經信號傳遞、舒張血管減輕高血壓的功能。H2S與CO2在高溫下發生反應:H2S(g)+CO2(g)?COS(g)+H2O(g)。在溫度為610K時,將0.10molCO2與0.40molH2S充入2.5L的空鋼瓶中,反應平衡后水的物質的量分數為0.02。
(1)H2S的平衡轉化率α1=,反應平衡常數K=;
(2)在620K下重復實驗,平衡后水的物質的量分數為0.03,H2S的轉化率α2NH4+,該反應的ΔH0(填“>”、“<”或“=”);
(3)向反應器中再分別充入下列氣體,能使H2S轉化率增大的是(填標號)。
a.H2S
b.CO2
c.COS
d.N2組卷:263引用:1難度:0.7


