2021-2022學年遼寧省沈陽市鐵西區九年級(上)期末化學試卷
發布:2024/12/13 6:0:2
一、選擇題(共15分)(本部分包括13道小題,1-11小題,每題1分;12、13小題,每題2分。每小題只有一個最符合題目要求的選項)
-
1.下列物質的性質中屬于化學性質的是( )
A.導電性 B.可燃性 C.延展性 D.揮發性 組卷:224引用:104難度:0.9 -
2.下列儀器能夠在酒精燈火焰上直接加熱的是( )
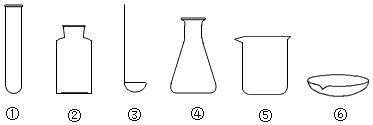
A.①③④ B.①③⑥ C.①②⑤ D.②④⑥ 組卷:1408引用:17難度:0.7 -
3.下列各物質中屬于混合物的是( )
A.空氣 B.氮氣 C.氧氣 D.二氧化碳 組卷:42引用:6難度:0.9 -
4.下列關于氧氣性質的說法錯誤的是( )
A.紅磷可以在氧氣中燃燒,產生大量白煙 B.發生氧化反應時總會發光、放熱 C.鐵絲能在氧氣中燃燒,火星四射 D.自然界中發生的燃燒、動植物的呼吸、金屬的銹蝕都是氧化反應 組卷:41引用:1難度:0.8 -
5.一壺水燒開后,壺蓋被頂開,這是因為( )
A.水分子運動速度快,撞開壺蓋 B.水分解成氫氣和氧氣 C.水由液態變成氣態,分子間隔增大,體積膨脹 D.水分子分成氫原子和氧原子后粒子數目增多 組卷:98引用:71難度:0.9 -
6.下列說法正確的是( )
A.魚類可以在水中暢游說明水中含有氧元素 B.地殼中、人體中以及海水中含量最多的元素都是氧元素 C.含有氧元素的化合物就是氧化物 D.某物質中除了氧元素以外只含一種元素,則它一定是氧化物 組卷:34引用:1難度:0.8
二、非選擇題(共50分)
-
18.金屬鐵是世界上年產量最高的金屬,也是應用最廣泛的金屬。
(1)某煉鐵廠用于高爐煉鐵的主要原料是赤鐵礦石、焦炭、空氣等,主要反應過程如圖所示:
寫出①的化學式;②的化學方程式。
(2)工業上用含氧化鐵80%的赤鐵礦1200t為原料煉鐵,得到含雜質4%的生鐵。據此填寫下列框圖中有關物質的質量。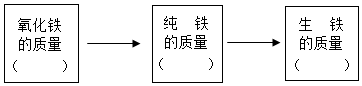 組卷:140引用:1難度:0.3
組卷:140引用:1難度:0.3 -
19.定性研究和定量研究是學習化學的重要手段。請根據實驗要求回答問題:
實驗一:圖1是氫氣還原氧化銅的實驗裝置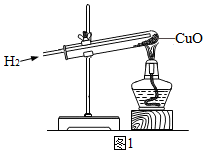
(1)該實驗觀察到的實驗現象有。實驗結束時的正確操作及原因是。
實驗二:圖2是用純凈的一氧化碳還原氧化鐵的實驗裝置。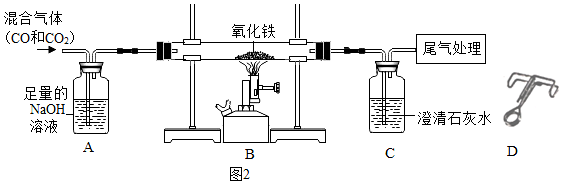
(2)根據實驗要求,推測NaOH溶液的作用是。
(3)實驗裝置B、C處發生反應的化學方程式為、。
(4)實驗結束時應繼續通入混合氣體至裝置冷卻到室溫,這樣做的目的是。但也有同學認為可以事先在裝置中放置D中的止水夾(數量不限),實現停止加熱時就可以停止通入混合氣體。具體的操作是撤掉酒精噴燈,迅速,將裝置冷卻至室溫后再拆開整套裝置。
實驗三:進行定量實驗
過氧化鈣(CaO2)是一種重要的化工產品,可用來改善地表水質、治理赤潮。過氧化鈣產品中常含有氧化鈣雜質。某小組設計如下實驗測定過氧化鈣產品的純度,實驗裝置如圖3。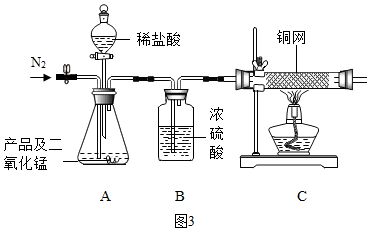
【資料在線】
①CaO2是一種白色固體,能與鹽酸反應:CaO2+2HCl═CaCl2+H2O2
②CaO是一種白色固體,能與鹽酸反應:CaO+2HCl═CaCl2+H2O
③MnO2與稀鹽酸不反應。
【實驗步驟】
①連接儀器并檢查裝置氣密性。
②稱取過氧化鈣產品及MnO2共12g。
③緩慢通入N2一段時間后,加熱銅網至紅熱。
④緩慢滴入過量稀鹽酸,直至A中樣品完全反應。
⑤緩慢通入N2一段時間后停止加熱,待C中銅網冷卻后,停止通入N2。
⑥將錐形瓶中的剩余物過濾、洗滌、干燥,得到濾渣2g。
回答下列問題
(5)A中MnO2的作用是,質量是。
(6)實驗前先緩慢通入一段時間的N2,作用是。樣品完全反應后,繼續緩慢通入N2的目的是。
(7)裝置B的作用有:除去氣體中的水蒸氣、。
(8)實驗測得C裝置中銅網增重1.8g,增重的質量是的質量。由此可以計算出H2O2的質量為g,產品中過氧化鈣的質量分數為。組卷:131引用:1難度:0.3


