2021-2022學年山東省泰安市新泰一中高一(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(1-15單選,每題2分,每題只有一個答案正確;16-20每題有1-2個答案正確,全對得4分,少選得2分,錯選不得分)
-
1.下列現象或做法與化學反應速率無關的是( )
A.“冰墩墩”制作材料生產過程中添加抗老化助劑 B.水果箱中放置乙烯利 C.饅頭制作過程中用酵頭發酵 D.新冠病毒可能通過氣溶膠加速傳播 組卷:84引用:3難度:0.5 -
2.壽山石是中華瑰寶,傳統“四大印章石”之一。某地采掘的壽山石化學式為X2Y4Z10(ZF)2。已知X、Y、Z、F均為短周期元素,X元素原子的最外層電子數等于其電子層數,且其單質能與強堿反應生成F2,YF4與F2Z2含有相同的電子數。下列說法錯誤的是( )
A.Y元素最高價氧化物對應的水化物為弱酸 B.X單質的導電能力強于Y單質 C.Z和F可形成不止一種化合物 D.F2Z2中既含有離子鍵,又含有共價鍵 組卷:21引用:3難度:0.6 -
3.下列說法正確的是( )
A.硫酸氫鉀在熔融狀態下離子鍵、共價鍵均被破壞,形成定向移動的離子,從而導電 B.HCl、HBr、HI的分子間的作用力依次增大,熱穩定性也依次增強 C.N2和Cl2兩種分子中,每個原子的最外層都具有8電子穩定結構 D.在O2、CO2、SiO2和NaOH中,都存在共價鍵,它們均由分子直接構成 組卷:18引用:1難度:0.8 -
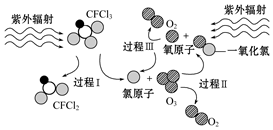 4.如圖為氟利昂(CFCl3)破壞臭氧層的反應過程示意圖,下列說法不正確的是( )
4.如圖為氟利昂(CFCl3)破壞臭氧層的反應過程示意圖,下列說法不正確的是( )A.過程Ⅰ中斷裂共價鍵C-Cl鍵 B.過程Ⅱ可表示為O3+Cl═ClO+O2 C.過程Ⅲ中O+O═O2是吸熱過程 D.上述過程說明氟利昂中氯原子是破壞O3的催化劑 組卷:20引用:2難度:0.7 -
5.下列說法正確的是( )
A.非金屬單質中一定含有共價鍵,不含離子鍵 B.含有氫、氧元素的化合物一定是共價化合物 C.僅由非金屬元素組成的化合物可能是離子化合物 D.熔點較高或很高的化合物一定不是共價化合物 組卷:19引用:1難度:0.7 -
6.一定條件下,容積固定的密閉容器中,對于可逆反應X(g)+3Y(g)?2Z(g),若X、Y、Z的起始濃度分別為c1、c2、c3(均不為零),達到化學平衡狀態時,X、Y、Z的濃度分別為0.1mol?L-1、0.3mol?L-1、0.08mol?L-1,則下列判斷不合理的是( )
A.c1:c2=1:3 B.達到化學平衡狀態時,Y和Z的生成速率之比為2:3 C.達到化學平衡狀態時,容器內的壓強不再變化 D.c1的取值范圍為0<c1<0.14mol?L-1 組卷:118引用:1難度:0.5 -
7.德國化學家F.Haber利用N2和H2在催化劑表面合成氨氣而獲得諾貝爾獎,該反應的微觀歷程及能量變化的示意圖如下,用
 、
、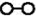 、
、 分別表示N2、H2、NH3,下列說法正確的是( )
分別表示N2、H2、NH3,下列說法正確的是( )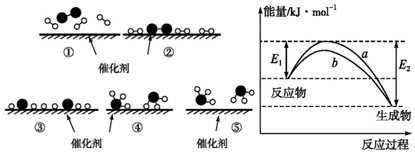
A.合成氨反應中,反應物斷鍵吸收的能量大于生成物形成新鍵釋放的能量 B.催化劑在吸附N2、H2時,催化劑與氣體之間的作用力為化學鍵 C.在該過程中,N2、H2斷鍵形成氮原子和氫原子 D.使用催化劑,合成氨反應放出的熱量減少 組卷:42引用:2難度:0.5 -
8.我國最近在太陽能光電催化-化學耦合分解硫化氫研究中獲得新進展,相關裝置如圖所示,下列說法正確的是( )
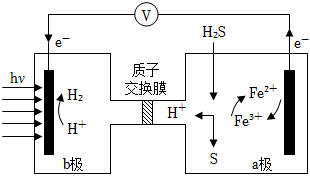
A.該制氫工藝中光能最終轉化為化學能 B.該裝置工作時,H+由b極區流向a極區 C.a極上發生的電極反應為Fe3++e-=Fe2+ D.a極區需不斷補充含Fe3+和Fe2+的溶液 組卷:285引用:20難度:0.7 -
9.反應NH4Cl+NaNO2═NaCl+N2↑+2H2O放熱且產生氣體,可用于冬天石油開采。下列表示反應中相關微粒的化學用語正確的是( )
A.中子數為18的氯原子 Cl3517B.N2的結構式::N??N: C.Na+的結構示意圖 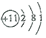
D.H2O的電子式:H-O-H 組卷:19引用:2難度:0.6
二、非選擇題
-
26.天然氣既是高效潔凈的能源,又是重要的化工原料,在生產、生活中用途廣泛。
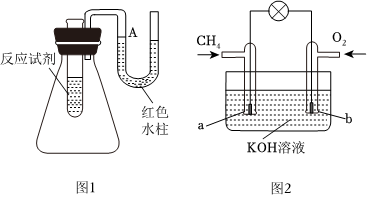
(1)如圖1是一個簡易測量物質反應是吸熱還是放熱的實驗裝置,利用此裝置可以很方便地測得某反應是放熱反應還是吸熱反應。將鋁片加入小試管內,然后注入足量的鹽酸,請根據要求完成下列問題:U形導管中液面A(填“上升”或“下降”),
說明此反應是(填“放熱”或“吸熱”)反應。
(2)甲烷可以消除氮氧化物污染。如:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)。
①下列措施能夠使該反應速率加快的是。
a.使用催化劑
b.降低溫度
c.及時分離水
d.把容器的體積縮小一倍
e.充入NO2
f.恒容下,充入Ar惰性氣體
②若上述反應在恒容密閉容器中進行,下列敘述能說明該反應已達平衡狀態的是。
a.正反應速率和逆反應速率相等
b.正反應速率最大,逆反應速率為0
c.容器內氣體的壓強不再變化
d.混合氣體的質量不再變化
e.c(NO2)=2c(N2)
f.單位時間內生成1mol CO2同時生成2 mol NO2
(3)甲烷可直接應用于燃料電池,該電池采用KOH溶液為電解質,其工作原理如圖2所示:
①外電路電子移動方向:(填“a極到b極”或“b極到a極”)。
②a電極的電極方程式為。組卷:48引用:3難度:0.5 -
27.某課外興趣小組實驗探究影響化學反應速率的因素.
為更精確地研究濃度對反應速率的影響,小組同學利用壓強傳感器等數字化實驗設備,探究鎂與不同濃度硫酸的反應速率,兩組實驗所用藥品如下:
實驗結果如圖所示.序號 鎂條的質量/g 硫酸 物質的量濃度(mol?L-1) 體積/mL Ⅰ 0.01 1.0 2 Ⅱ 0.01 0.5 2 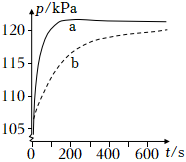
①實驗Ⅰ對應圖中曲線(填字母);圖中曲線上的斜率越大,說明反應速率越(填“快”、“慢”“無法確定”).
②分析實驗Ⅱ對應曲線可知,反應開始階段,反應速率不斷加快,原因是;隨著反應的不斷進行,化學反應速率減慢,原因是.組卷:3引用:1難度:0.6


