2022年廣東省粵西地區(qū)中考化學二模試卷
發(fā)布:2024/10/31 18:30:3
一、選擇題(本大題包括15小題,每小題3分,共45分。在每小題列出的四個選頂中,只有一個是正確的,請將答愿卡上對應題目所選的選項涂黑)
-
1.下列過程中發(fā)生了化學變化的是( )
A.摩擦生熱 B.光合作用 C.酒精揮發(fā) D.海水曬鹽 組卷:18引用:1難度:0.9 -
2.規(guī)范的操作方法是實驗安全和成功的保證。下列圖示的實驗操作正確的是( )
A. 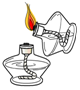
點燃酒精燈B. 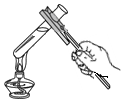
加熱液體C. 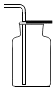
收集氫氣D. 
稀釋濃硫酸組卷:129引用:8難度:0.7 -
3.生活、工作場所常見到一些警示圖標。下列圖標放置地點錯誤的是( )
A. 
運輸濃硫酸的槽罐車B. 
存放酒精的試劑柜C. 
面粉加工廠D. 
城市居民住宅區(qū)組卷:224引用:14難度:0.7 -
4.下列物質(zhì)的分類正確的是( )
A.復合肥:硝酸鉀、磷酸二氫銨、磷酸二氫鉀 B.合金:黃銅、青銅、氧化銅 C.無機非金屬材料:陶瓷、水泥、玻璃鋼 D.堿:火堿、純堿、小蘇打 組卷:199引用:4難度:0.8 -
5.“碳達峰”是指我國承諾在2030年前,二氧化碳的排放不再增長;“碳中和”是指到2060年,采取各種方式抵消自身產(chǎn)生的二氧化碳排放量,實現(xiàn)二氧化碳“零排放”。下列措施不利于“碳達峰”和“碳中和”的是( )
A.鼓勵民眾植樹造林 B.加大煤和石油的使用 C.培育氫燃料電池汽車產(chǎn)業(yè) D.循環(huán)利用CO2制造合成燃料、尿素等物質(zhì) 組卷:283引用:19難度:0.8 -
6.下列有關化學發(fā)展簡史的敘述不正確的是( )
A.張青蓮為相對原子質(zhì)量的測定做出了卓越貢獻 B.道爾頓采用定量的方法研究了空氣的組成 C.門捷列夫發(fā)現(xiàn)了元素周期律 D.我國古代四大發(fā)明中的火藥、造紙屬于化學方面取得的成就 組卷:109引用:9難度:0.8 -
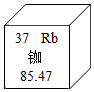 7.“北斗”三號衛(wèi)星導航系統(tǒng)應用了星載氫原子鐘和銣原子鐘。銣在元素周期表中的信息如圖所示,下列有關銣的說法錯誤的是( )
7.“北斗”三號衛(wèi)星導航系統(tǒng)應用了星載氫原子鐘和銣原子鐘。銣在元素周期表中的信息如圖所示,下列有關銣的說法錯誤的是( )A.屬于金屬元素 B.Rb+核外電子數(shù)為36 C.原子核內(nèi)有37個質(zhì)子 D.相對原子質(zhì)量為85.47g 組卷:369引用:12難度:0.6
四、(本大題包括1小題,共10分)
-
20.某化學興趣小組用除鐵銹后的廢液(主要含F(xiàn)eCl3、FeCl2、HCl)制備FeSO4?7H2O,其流程如圖:
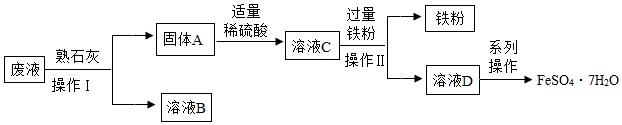
【查閱資料】鐵能與硫酸鐵反應,生成硫酸亞鐵。化學方程式:Fe+Fe2(SO4)3═3FeSO4。
(1)寫出熟石灰與廢液中的某物質(zhì)發(fā)生中和反應的化學方程式。
(2)操作Ⅰ的名稱是,所得固體A需洗滌,具體的操作是:取最后一次洗滌后的濾液,向其中滴加,無明顯現(xiàn)象,則表示固體已洗凈,所得溶液B的溶質(zhì)一定有(填化學式)。
(3)向洗滌后的固體A中加入稀硫酸,發(fā)生的化學反應方程式為(寫一個即可)。
(4)操作Ⅱ加入過量鐵粉的作用是。
(5)已知硫酸亞鐵的溶解度和析出晶體的組成如下表:
根據(jù)上表,硫酸亞鐵晶體(FeSO4?7H2O)冷卻結(jié)晶溫度最高不超過溫度/℃ 0 10 30 40 50 60 64 70 80 90 溶解度/g 15.6 20.5 33.0 40.4 48.8 55.0 55.3 50.6 43.7 37.2 析出晶體 FeSO4?7H2O FeSO4?4H2O FeSO4?H2O ℃。
(6)得到的FeSO4?7H2O晶體應該用洗滌(填序號)。
a.水
b.飽和硫酸亞鐵溶液
c.稀硫酸組卷:52引用:2難度:0.4
五、(本大題包括1小題,共10分)
-
21.硫酸是化學實驗室中常用的試劑,也是重要的化工原料。試回答下列問題:
(1)濃硫酸具有強烈的腐蝕性。如果不慎將濃硫酸沾到皮膚上,應立即用大量的水沖洗,然后涂上3%~5%的(填“碳酸氫鈉”“氫氧化鈉”“硼酸”之一)溶液,以防灼傷皮膚。
(2)用硫單質(zhì)制取硫酸的轉(zhuǎn)化流程示意圖如圖:
在S、SO2、SO3、H2SO4四種物質(zhì)中,硫元素的化合價表現(xiàn)為+4價的物質(zhì)是(填化學式)。寫出上述轉(zhuǎn)化流程步驟③中所發(fā)生反應的化學方程式:。
(3)現(xiàn)取100g稀硫酸倒入燒杯中,慢慢向燒杯中加入溶質(zhì)質(zhì)量分數(shù)為10%的BaCl2溶液,反應過程中產(chǎn)生沉淀的質(zhì)量與所加入BaCl2溶液的質(zhì)量關系如圖所示。試回答:
①當加入BaCl2溶液200g時(即圖中A點),燒杯中溶液里大量存在的酸根離子是(填離子符號)。
②當加入BaCl2溶液416g時(即圖中B點),恰好完全反應,試通過計算求產(chǎn)生沉淀的總質(zhì)量。(計算結(jié)果精確至0.1g)組卷:287引用:4難度:0.5


