2021-2022學年云南省德宏州瑞麗市高二(上)期末化學試卷
發布:2024/4/20 14:35:0
一、單選題(共20小題,每題3分)
-
1.以下對核外電子運動狀態的描述正確的是( )
A.電子的運動與行星相似,圍繞原子核在固定的軌道上高速旋轉 B.能量低的電子只能在s軌道上運動,能量高的電子總是在f軌道上運動 C.能層序數越大,s原子軌道的半徑越大 D.在同一能級上運動的電子,其運動狀態肯定相同 組卷:22引用:1難度:0.6 -
2.下列與金屬腐蝕有關的說法,正確的是( )
A. 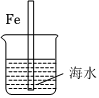
如圖,圖中,插入海水中的鐵棒,越靠近底端腐蝕越嚴重B. 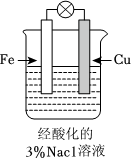
如圖,圖中,插入溶液中的鐵棒容易溶解,主要是發生電化學腐蝕C. 
如圖,圖中,燃氣灶的中心部位容易生銹,主要是由于高溫下鐵發生電化學腐蝕D. 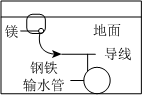
如圖,圖中,用犧牲鎂塊的方法來防止地下鋼鐵管道的腐蝕,鎂塊相當于原電池的負極組卷:26引用:10難度:0.7 -
 3.25℃時,取濃度均為0.1000mol?L-1的醋酸溶液和氨水各20.00mL,分別用0.1000mol?L-1NaOH溶液、0.1000mol?L-1鹽酸進行中和滴定,滴定過程中pH隨滴加溶液的體積變化關系如圖所示。下列說法不正確的是( )
3.25℃時,取濃度均為0.1000mol?L-1的醋酸溶液和氨水各20.00mL,分別用0.1000mol?L-1NaOH溶液、0.1000mol?L-1鹽酸進行中和滴定,滴定過程中pH隨滴加溶液的體積變化關系如圖所示。下列說法不正確的是( )A.根據滴定曲線可得,25℃時Ka(CH3COOH)≈Kb(NH3?H2O)≈10-5 B.當NaOH溶液和鹽酸滴加至20.00mL時,曲線Ⅰ和Ⅱ剛好相交 C.曲線Ⅰ表示的滴定過程一般選擇甲基橙作指示劑 D.在逐滴加入NaOH溶液或鹽酸至40.00mL的過程中,水的電離程度先增大后減小 組卷:24引用:1難度:0.5 -
4.pH=5和pH=3的兩種鹽酸以體積比1:2混合,則混合溶液的pH約為( )
A.3.2 B.4.0 C.4.2 D.5.0 組卷:74引用:3難度:0.4 -
 5.用如圖所示的實驗裝置進行實驗X及Y時,每隔半分鐘分別測定放出氣體的體積.下列選項中可正確表示實驗X及Y的結果是( )
5.用如圖所示的實驗裝置進行實驗X及Y時,每隔半分鐘分別測定放出氣體的體積.下列選項中可正確表示實驗X及Y的結果是( )實驗 所用的酸 X 25mL 0.2mol/L Y 50mL 0.1mol/L A. 
B. 
C. 
D.  組卷:90引用:12難度:0.7
組卷:90引用:12難度:0.7 -
 6.將二氧化碳轉化為燃料是目前的研究熱點,2017年《科學》雜志報道的一種將CO2轉化為烴和醇的裝置如圖所示。下列說法正確的是( )
6.將二氧化碳轉化為燃料是目前的研究熱點,2017年《科學》雜志報道的一種將CO2轉化為烴和醇的裝置如圖所示。下列說法正確的是( )A.圖中能量轉化的方式只有1種 B.裝置工作時,H+向X極區移動,Y極周圍溶液的pH 增大 C.X 極上得到CH3OH 的電極反應式為2CO2+4H2O+12e-═2CH3OH+3O2 D.若X極生成1mol C2H4 和1mol CH3OH,電路中流過18 mol 電子 組卷:551引用:6難度:0.3 -
 7.如題圖所示,將緊緊纏繞不同金屬的鐵釘放入培養皿中,再加入含有適量酚酞和NaCl的瓊脂熱溶液,冷卻后形成瓊膠(離子在瓊膠內可以移動),下列敘述正確的是( )
7.如題圖所示,將緊緊纏繞不同金屬的鐵釘放入培養皿中,再加入含有適量酚酞和NaCl的瓊脂熱溶液,冷卻后形成瓊膠(離子在瓊膠內可以移動),下列敘述正確的是( )A.a中鐵釘附近呈現紅色 B.b中鐵釘上發生還原反應 C.a中銅絲上發生氧化反應 D.b中鋁條附近有氣泡產生 組卷:1166引用:29難度:0.7 -
8.用石墨作電極,電解1mol?L-1下列物質的溶液,則電解前后溶液的pH保持不變的是( )
A.硫酸 B.氫氧化鈉 C.硫酸鈉 D.氯化鈉 組卷:20引用:3難度:0.6
二、非選擇題
-
23.工業上利用廢鎳催化劑(主要成分為Ni,還含有一定量的Zn、Fe、SiO2、CaO等)制備草酸鎳晶體的流程如圖:

(1)請寫出一種能提高“酸浸”速率的措施:;濾渣Ⅰ的成分是CaSO4和(填化學式)。
(2)除鐵時,控制不同的條件可以得到不同的濾渣Ⅱ。已知濾渣Ⅱ的成分與溫度、pH的關系如圖乙所示:
①若控制溫度為40℃、pH=8,則濾渣Ⅱ的主要成分為(填化學式)。
②若控制溫度為80℃、pH=2,可得到黃鐵礬鈉[Na2Fe6(SO4(OH)12),]沉淀(圖中陰影部分),寫出生成黃鐵礬鈉的離子方程式:。
(3)已知除鐵后所得100mL溶液中c(ca2+)=0.01mol?L-1,加入100mLNH4F溶液,使Ca2+恰好沉淀完全即溶液中c(Ca2+)=1×10-5mol?L-1,則所加溶液的c(NH4F)=mol?L-1[已知Ksp(CaF2)=5.29×10-9]。
(4)加入有機萃取劑的作用是。組卷:3引用:3難度:0.7 -
 24.某校化學研究性學習小組欲設計實驗驗證Fe、Cu的金屬活動性,他們提出了以下兩種方案。請你幫助他們完成有關實驗項目:
24.某校化學研究性學習小組欲設計實驗驗證Fe、Cu的金屬活動性,他們提出了以下兩種方案。請你幫助他們完成有關實驗項目:
方案I:有人提出將大小相等的鐵片和銅片,分別同時放入稀硫酸(或稀鹽酸)中,觀察產生氣泡的快慢,據此確定它們的活動性。該原理的離子方程式為。
方案II:有人利用Fe、Cu作電極設計成原電池,以確定它們的活動性。試在下面的方框內畫出原電池的裝置圖,標出原電池的電極材料和電解質溶液,并寫出電極反應式。
正極反應式:,負極反應式:。
方案III;結合你所學的知識,幫助他們再設計一個驗證Fe、Cu活動性的簡單實驗方案(與方案1、II不能雷同),用離子方程式表示其反應原理:。組卷:18引用:4難度:0.6


