2021-2022學年重慶市天星橋中學高二(上)第二次月考化學試卷
發布:2024/11/22 4:0:1
一、單選題(本大題共22小題,共44.0分)
-
1.下列反應為熵增的吸熱反應的是( )
A.4Fe(OH)2(s)+O2(g)+2H2O(l)=4Fe(OH)3(s) B.NH4HCO3(s)+CH3COOH(l)=CO2(g)+CH3COONH4(aq)+H2O(l) C.2H2(g)+O2(g)=2H2O(l) D.2Al(s)+Fe2O3(s)=Al2O3(s)+2Fe(s) 組卷:2引用:1難度:0.7 -
2.下列有關化學反應速率的說法正確的是( )
A.凡是能量達到活化能的分子發生的碰撞均為有效碰撞 B.增大反應物濃度能加快正反應的反應速率,降低逆反應的反應速率 C.溫度升高使化學反應速率加快的主要原因是增加了反應物分子之間的碰撞次數 D.決定化學反應速率的根本因素是參加反應的各物質的性質 組卷:26引用:7難度:0.9 -
3.在一定條件下,對于密閉容器中進行的反應:P(g)+Q(g)?R(g)+S (s)下列說法中可以充分說明這一反應已經達到化學平衡狀態的是( )
A.P、Q、R、S的濃度相等 B.P、Q、R、S在密閉容器中共存 C.P、Q、R、S的濃度不再變化 D.用P的濃度表示的化學反應速率與用Q的濃度表示的化學反應速率相等 組卷:71引用:33難度:0.9 -
4.一定條件下,體積為2L的密閉容器中,1mol X和3mol Y進行反應:X(g)+3Y(g)?2Z(g),經12s達到平衡,生成0.6mol Z.下列說法正確的是( )
A.以X濃度變化表示的反應速率為 mol(L?s)18B.12s后將容器體積擴大為10L,Z的平衡濃度變為原來的 15C.若增大X的濃度,則物質Y的轉化率減小 D.若該反應的△H<0,升高溫度,平衡常數K減小 組卷:35引用:12難度:0.7 -
5.對可逆反應4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列敘述正確的是( )
A.達到化學平衡時,4υ正(O2)=5υ逆(NO) B.若單位時間內生成x mol NO的同時,消耗x mol NH3,則反應達到平衡狀態 C.達到化學平衡時,若增加容器體積,則正反應速率減少,逆反應速率增大 D.化學反應速率關系是:2υ正(NH3)=3υ正(H2O) 組卷:964引用:156難度:0.7 -
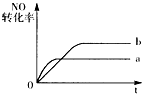 6.在容積不變的密閉容器中,一定條件下進行如下反應:
6.在容積不變的密閉容器中,一定條件下進行如下反應:
NO(g)+CO(g)=N2(g)+CO2(g)△H=-373.2kJ/mol.12
如圖曲線a表示該反應過程中,NO的轉化率與反應時間的關系.若改變起始條件,使反應過程按照曲線b進行,可采取的措施是( )A.加催化劑 B.向密閉容器中加入氬氣 C.降低溫度 D.增大反應物中NO的濃度 組卷:107引用:10難度:0.7 -
7.下列事實可以用勒夏特列原理解釋的是( )
A.高錳酸鉀(KMnO4)溶液加水稀釋后顏色變淺 B.使用催化劑,提高合成氨的生產效率 C.新制的氯水在光照條件下顏色變淺 D.H2、I2、HI平衡混合氣體加壓后顏色變深 組卷:6引用:2難度:0.7 -
8.對可逆反應N2(g)+3H2(g)?2NH3(g)△H<0,下列圖象正確的是( )
A. 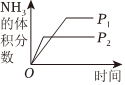
B. 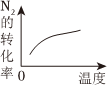
C. 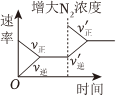
D. 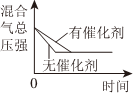 組卷:45引用:8難度:0.7
組卷:45引用:8難度:0.7 -
9.下列有關pH=11的氨水和pH=11的碳酸鈉溶液中水的電離程度的比較正確的是( )
A.前者大于后者 B.前者等于后者 C.前者小于后者 D.無法確定 組卷:16引用:2難度:0.7
二、填空題(本大題共6小題,共46分)
-
28.(1)化學是一門以實驗為基礎的學科,化學實驗是化學學習的重要內容.根據你掌握的知識判斷,下列實驗操作的描述中,正確的是
.(填寫下列各項序號)
A.從試劑瓶中取出的任何藥品,若有剩余不能再放回原試劑瓶
B.用稀鹽酸洗滌盛放過石灰水的試劑瓶
C.配制硫酸溶液時,可先在量筒中加入一定體積的水,再在攪拌下慢慢加入濃硫酸
D.各放一張質量相同的濾紙于天平的兩托盤上,將NaOH固體放在左盤紙上稱量
E.Na2CO3溶液不能保存在帶有玻璃塞的試劑瓶中
F.將用水潤濕的pH試紙,浸入稀鹽酸溶液,測定溶液的pH
(2)化學實驗中,不正確的操作會對實驗結果的準確性造成一定的影響,請用“>”、“<”或“一”填寫下列空白:
①實驗時未用標準液潤洗滴定管,則測得錐形瓶中待測液的濃度實際濃度.
②用托盤天平稱取10.4g氯化鈉,若將砝碼和氯化鈉的位置放顛倒了,所稱取氯化鈉的質量為10.4g.
③用容量瓶配制500mL 0.1mol?L-1.NaOH溶液,定容時仰視刻度線,所得溶液的物質的量濃度0.1mol?L-1.組卷:36引用:2難度:0.5
三、實驗題(本大題共1小題,共10.0分)
-
 29.實驗室中有一未知濃度的稀鹽酸,某學生測定鹽酸的濃度在實驗室中進行實驗.請完成下列填空:
29.實驗室中有一未知濃度的稀鹽酸,某學生測定鹽酸的濃度在實驗室中進行實驗.請完成下列填空:
(1)配制100ml 0.10mol?L-1NaOH標準溶液,計算需稱量g氫氧化鈉固體.
(2)取20.00mL待測鹽酸溶液放入錐形瓶中,并滴加2~3滴酚酞作指示劑,用自己配制的標準液NaOH溶液進行滴定.重復上述滴定操作2~3次,記錄數據如下:
①滴定達到終點的標志是實驗編號 NaOH溶液的濃度 滴定完成時,NaOH溶液滴入的體積/mL 待測鹽酸的體積/mL 1 0.10 22.62 20.00 2 0.10 22.72 20.00 3 0.10 22.80 20.00 .
②根據上述數據,可計算出該鹽酸的濃度約為(保留兩位有效數字).
③排去堿式滴定管中氣泡的方法應采用如圖所示操作中的,然后輕輕擠壓玻璃球使尖嘴部分充滿堿液.
④在上述實驗中,下列操作(其他操作正確)會造成測定結果偏高的有:.
A、滴定終點讀數時俯視讀數
B、酸式滴定管使用前,水洗后未用待測鹽酸溶液潤洗
C、錐形瓶水洗后未干燥
D、稱量NaOH固體中混有Na2CO3固體
E、配制好的NaOH標準溶液保存不當,部分與空氣中的CO2反應生成了Na2CO3
F、堿式滴定管尖嘴部分有氣泡,滴定后消失.組卷:23引用:2難度:0.5


