2022-2023學年福建省福州市三校高二(上)期中化學試卷
發布:2024/11/13 22:0:1
一、選擇題(本大題共16小題,每小題3分,每題只有一個選項符合題意,共48分)
-
1.下列措施不符合節能減排的是( )
A.在屋頂安裝太陽能熱水器為居民提供生活用熱水 B.大力發展火力發電,解決電力緊張問題 C.用石灰對煤燃燒后形成的煙氣脫硫,并回收石膏 D.用雜草生活垃圾等有機廢棄物在沼氣池中發酵產生沼氣,作家庭燃氣 組卷:15引用:2難度:0.6 -
2.一定量的鐵片與足量稀硫酸反應制取氫氣時,下列措施能使氫氣生成速率增大且生成氫氣總量不變的是( )
A.降低溫度 B.不用稀硫酸,改用98%濃硫酸 C.滴加少量CuSO4溶液 D.不用鐵片,改用等量的鐵粉 組卷:23引用:3難度:0.7 -
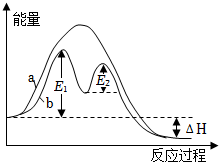 3.某反應過程能量變化如圖所示,下列說法正確的是( )
3.某反應過程能量變化如圖所示,下列說法正確的是( )A.反應過程a有催化劑參與 B.該反應的焓變△H>0 C.使用催化劑,能改變該反應的活化能 D.有催化劑條件下,反應的活化能等于E1+E2 組卷:29引用:4難度:0.7 -
4.下列說法中錯誤的是( )
A.凡是放熱反應而且熵增加的反應,就更易自發進行 B.對于同一物質在不同狀態時的熵值是:氣態>液態>固態 C.對同一反應來說,平衡常數K值越大,則正反應進行越完全 D.凡是能量較高的分子發生的碰撞均為有效碰撞 組卷:52引用:3難度:0.8 -
5.設C(s)+H2O(g)?CO(g)+H2(g)ΔH>0,反應速率為V1;2NO2(g)?N2O4(g)ΔH<0,反應速率為V2。對于上述反應,當溫度降低時,V1和V2的變化情況為( )
A.同時減小 B.同時增大 C.V1增大,V2減小 D.V1減小,V2增大 組卷:10引用:3難度:0.5 -
6.化學反應過程中既有物質的變化,又有能量的變化。關于下列熱化學方程式的說法中,正確的是( )
(1)2H2(g)+O2(g)=2H2O(g)△H1
(2)2H2(g)+O2(g)=2H2O(l)△H2A.△H1<△H2 B.△H1>△H2 C.△H1=△H2 D.不能判斷△H1與△H2的相對大小 組卷:30引用:2難度:0.5
二、簡答題(共52分)
-
19.(1)按要求完成下列問題:
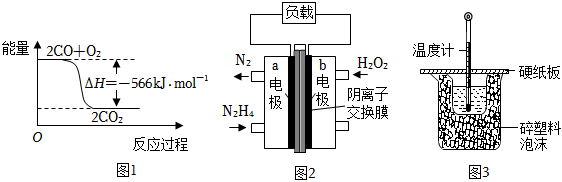
已知常溫下CO轉化成CO2的能量關系如圖1所示。寫出該反應的熱化學方程式:。
(2)N2H4和H2O2混合可作火箭推進劑,已知:0.5molN2H4(l)和足量氧氣反應生成N2(g)和H2O(l),放出310.6kJ的熱量;2H2O2(l)=O2(g)+2H2O(l)△H=-196.4kJ?mol-1。
①反應N2H4(l)+O2(g)=N2(g)+2H2O(l)的△H=kJ?mol-1。
②N2H4(l)和H2O2(l)反應生成N2(g)和H2O(l)的熱化學方程式為。
將上述反應設計成原電池如圖2所示,KOH溶液作為電解質溶液。
③a極電極反應式為。
(3)實驗室用50mL0.50mol?L-1鹽酸與50mL某濃度的NaOH溶液在如圖3所示裝置中反應,通過測定反應過程中所放出的熱量可計算中和熱。
①該裝置缺少一種玻璃儀器,該儀器的名稱為。
②實驗室提供了0.50mol?L-1和0.55mol?L-1兩種濃度的NaOH溶液,應最好選擇mol?L-1的NaOH溶液進行實驗。
③在測定中和反應的反應熱的實驗中,下列敘述正確的是。
A.測定中和反應的反應熱時,酸堿中和之后應讀取體系達到的最高溫度
B.中和反應的試驗中,應快速將NaOH溶液一次倒入盛鹽酸的小燒杯中
C.可以用氫氧化鉀代替氫氧化鈉,濃硫酸代替稀鹽酸
D.在測定中和反應的反應熱實驗中,每完成一次反應熱熱測定,至少需要讀三次溫度。組卷:15引用:1難度:0.7 -
20.如圖所示,某同學設計了一個燃料電池并探究氯堿工業原理等相關問題,其中乙裝置中X為陽離子交換膜。請按要求回答相關問題:
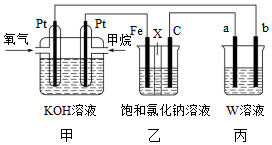
(1)甲中甲烷燃料電池的負極反應式為。
(2)乙中石墨電極(C)作極。
(3)若甲中消耗2.24 L(標況)氧氣,乙裝置中鐵電極上生成的氣體為(填化學式),其體積(標況)為L。
(4)若丙中是AgNO3溶液,a、b電極為石墨,一段時間后,溶液的pH(填“變大”“變小”或“不變”),寫出丙中反應的化學方程式。組卷:37引用:2難度:0.5


