2021-2022學年山東省威海市高二(上)期末化學試卷
發布:2024/12/16 15:0:2
一、選擇題:本題共10小題,每小題2分,共20分.每小題只有一個選項符合題意.
-
1.下列關于晶體的說法錯誤的是( )
A.分子晶體中分子間作用力越大,分子越穩定 B.溫度越高,金屬晶體的導電性越弱 C.離子晶體中一定含有離子鍵,共價晶體中一定含有共價鍵 D.在SiO2晶體中,由Si、O構成的最小單元環中共有12個原子 組卷:40引用:1難度:0.6 -
2.下列化學用語表達錯誤的是( )
A. 的空間結構模型:SO2-3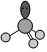
B.Ca2+的離子結構示意圖: 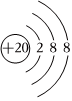
C.鐵原子最外層原子軌道示意圖: 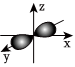
D.銅原子價電子排布式:3d104s1 組卷:17引用:2難度:0.7 -
3.下列有關比較中,順序排列錯誤的是( )
A.微粒的半徑:Al3+<Na+<Cl- B.共價晶體的硬度:SiC<晶體硅<金剛石 C.物質的沸點:H2O>HF>AsH3 D.離子晶體的熔點:MgO>NaCl>KCl 組卷:55引用:3難度:0.6 -
4.華人科學家吳健雄用
Co放射源進行實驗驗證了楊振寧和李政道的重要發現。6027Co的衰變方程為:6027Co=6027X+-1e-+AZ,其中ve是反中微子,其電荷數為0,電子和反中微子的靜止質量均為0。下列說法正確的是( )veA. Co的中子數為606027B.Co與X質量數相同,互為同位素 C.衰變產物X為 Ni6028D.X的核外電子空間運動狀態為28種 組卷:4引用:1難度:0.8 -
5.下列說法正確的是( )
A.任何溫度下,純水都顯中性且pH為7 B.常溫下,pH相同的CH3COONa、NaHCO3、NaClO溶液,其濃度逐漸增大 C.常溫下,pH=3的CH3COOH溶液和pH=11的Ba(OH)2溶液等體積混合后顯堿性 D.侯氏制堿法先將精制的飽和食鹽水氨化,再碳酸化,以獲得更多的NaHCO3沉淀 組卷:10引用:2難度:0.7 -
6.下列說法正確的是( )
A.元素周期表中周期序數等于核外電子層數,族序數等于最外層電子數 B.某基態原子3d軌道電子排布 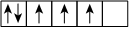 違背了洪特規則
違背了洪特規則C.在所有元素中,電負性和第一電離能最強的均為氟元素 D.運用玻爾原子結構模型可以解釋鈉原子光譜中有靠得很近的兩條黃色譜線 組卷:23引用:1難度:0.7 -
7.碘及其化合物廣泛用于醫藥、染料等方面。中國海洋大學提出一種從海帶中提取碘的方法,其流程如圖。下列說法錯誤的是( )
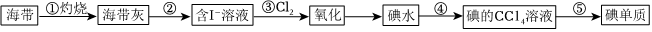
A.操作①的目的是分解除去其中的有機化合物 B.操作②用到的玻璃儀器有漏斗、燒杯、玻璃棒 C.操作④的名稱為萃取分液,CCl4可以用苯、酒精等代替 D.操作⑤可以為蒸餾 組卷:39引用:6難度:0.6
三、非選擇題:本題共6小題,共60分.
-
20.含砷廢水常見于采礦、半導體等工業,部分砷的化合物有毒,因此需除去廢水中的砷.
天然水體中砷元素主要以As(Ⅲ)和As(Ⅴ)存在.在H3AsO4水溶液中,各種微粒的物質的量分數與溶液pH的關系如圖1所示.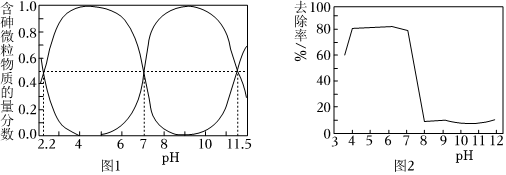
(1)當天然水體的pH為4時,水體中所含As(Ⅴ)的主要微粒是.
(2)將NaOH溶液滴入H3AsO4溶液中,當pH達到8時,所發生反應的離子方程式為.此時,溶液中含砷離子濃度由大到小的順序為.
(3)25℃時,向H3AsO4溶液中加入NaOH溶液至中性,此時溶液中=c(AsO43-)c(H3AsO4).組卷:13引用:1難度:0.6 -
21.利用高鐵酸鹽處理含砷廢水.在一定pH范圍內,高鐵酸鹽被還原成Fe(OH)3膠體,而吸附含砷化合物.不同pH對K2FeO4除砷影響如圖2所示.
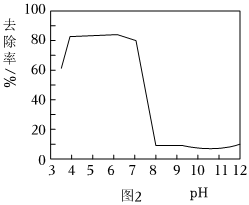
已知:溶液的pH對膠體粒子表面所帶電荷有影響.pH<7.1時,膠體粒子表面帶正電荷,pH越低,表面所帶正電荷越多.pH=7.1時,膠體粒子表面不帶電荷;pH>7.1時,膠體粒子表面帶負電荷,pH越高,表面所帶負電荷越多.
(1)結合圖1和圖2分析,除砷過程中控制廢水pH約為適宜,pH過低或過高,砷的去除率都會下降.pH過低,主要以Fe3+形式存在,不易形成Fe(OH)3膠體.pH過高,一是K2FeO4氧化性減弱,產生Fe(OH)3膠體的量少;二是;三是pH過高,生成Fe(OH)3沉淀而不是Fe(OH)3膠體.
(2)pH<1時,K2FeO4氧化H3AsO3的離子方程式為.組卷:7引用:1難度:0.7


