2023-2024學年浙江省杭州市夏衍中學九年級(上)期中科學試卷
發布:2024/10/24 3:0:1
一、選擇題(每小題3分,共45分,每小題只有一個選項符合題意)
-
1.一些食物的pH范圍如下,其中呈堿性的是( )
A.檸檬汁(2.0-3.0) B.牛奶(6.3-6.6) C.番茄汁(4.0-4.4) D.雞蛋清(7.6-8.0) 組卷:10引用:2難度:0.5 -
2.以下化學實驗現象的描述正確的是( )
A.鎂條在空氣中燃燒,火星四射,生成黑色固體 B.生銹鐵釘放入少量的稀鹽酸中,溶液呈現黃色 C.打開濃硫酸的試劑瓶塞,瓶口出現大量的白霧 D.向氫氧化鈉溶液中滴加少量紫色石蕊溶液,溶液變為紅色 組卷:2引用:1難度:0.5 -
3.圖是物質X溶于水發生解離后的微觀示意圖,其中能說明X是一種酸的是( )
A. 
B. 
C. 
D.  組卷:8引用:1難度:0.5
組卷:8引用:1難度:0.5 -
 4.用如圖所示裝置進行下列實驗:將①中溶液滴入②中,預測的現象與實際不相符的是( )
4.用如圖所示裝置進行下列實驗:將①中溶液滴入②中,預測的現象與實際不相符的是( )選項 ①中物質 ②中物質 預測②中的現象 A 稀鹽酸 碳酸鈣 產生氣泡 B 稀硫酸 氧化鐵 產生氣泡 C 氯化鋇溶液 硫酸鉀溶液 產生白色沉淀 D 氫氧化鈉溶液 硫酸銅溶液 產生白色沉淀 A.A B.B C.C D.D 組卷:8引用:1難度:0.5 -
 5.如圖是某地使用的“風光互補”景觀照明燈。它“頭頂”小風扇,“肩扛”光電池板,“腰挎”照明燈,“腳踩”蓄電池。下列解釋合理的是( )
5.如圖是某地使用的“風光互補”景觀照明燈。它“頭頂”小風扇,“肩扛”光電池板,“腰挎”照明燈,“腳踩”蓄電池。下列解釋合理的是( )A.光電池板是將電能轉化為光能 B.小風扇利用風力發電,將機械能轉化為電能 C.照明燈是將內能轉化為電能 D.蓄電池夜晚放電,將電能轉化為化學能 組卷:51引用:5難度:0.5 -
6.下列各圖中●和〇分別表示氫原子和氧原子,其中能表示保持H2O化學性質的微粒是( )
A. 
B. 
C. 
D.  組卷:820引用:3難度:0.5
組卷:820引用:3難度:0.5 -
7.如圖所示的四種運動中,重力勢能轉化為動能的是( )
A. 
運動員被蹦床彈起B. 
小球從B向C運動C. 
滾擺向上滾動D. 
衛星從遠地點向近地點運動組卷:9引用:1難度:0.5 -
8.如圖所示,OQ是水平地面,物體在水平拉力作用下從O勻速直線運動到Q,OP段拉力F1為300N,F1做的功為W1,功率為P1;PQ段拉力F2為200N,F2做的功為W2,功率為P2,則( )

A.W1>W2 B.W1<W2 C.P1>P2 D.P1<P2 組卷:131引用:4難度:0.5 -
9.“灰汁團”是寧波傳統小吃,制作過程中要用到大米和“灰汁”。“灰汁”制取方法如資料卡所示。下列說法錯誤的是( )
資料卡 傳統方法:稻草燒灰→加水溶解→靜置沉淀→過濾取汁 現代方法:將食用堿(純堿和小蘇打的混合物)與水按一定比例混合成汁 A.大米中含有的淀粉屬于有機物 B.稻草燃燒屬于物理變化 C.傳統方法制得的“灰汁”是混合物 D.現代方法制得的“灰汁”能使酚酞試液變紅色 組卷:134引用:9難度:0.5 -
10.將金屬M的粉末放入盛有硝酸銅溶液的燒杯中,充分反應后,溶液呈無色,繼續向燒杯中加入一定量的硝酸銀溶液,充分反應后過濾,得到濾渣和藍色濾液。根據上述實驗分析,下列說法錯誤的是( )
A.金屬活動性強弱順序:M>Cu>Ag B.濾渣中可能有金屬M C.濾液中至少含有兩種溶質 D.濾渣中一定有Ag 組卷:216引用:6難度:0.5 -
11.如圖所示,正常使用時屬于費力杠桿的是( )
A. 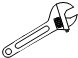
扳手B. 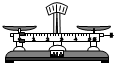
天平C. 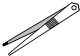
鑷子D. 
圓藝剪組卷:7引用:1難度:0.5
四、解答題(共45分)
-
34.我國提出爭取在2060年實現“碳中和”。為減少二氧化碳的排放,科學家提出用二氧化碳合成一種可降解的塑料[C4H6O3]n(相對分子質量為102n),一定條件下,反應可表示為:nCO2+nC3H6O═[C4H6O3]n。若制取204噸該塑料,理論上可以少排放多少噸二氧化碳?(寫出計算過程)
組卷:255引用:7難度:0.5 -
35.人類歷史發展的不同階段曾以不同金屬材料的使用作為標志。

(1)金、銀在自然界有單質形式存在,說明它們的化學性質都。
(2)在生產、生活實踐中,人類逐漸掌握了多種金屬的冶煉技術。
①比較兩種鐵礦石:磁鐵礦(主要成分為Fe3O4)和菱鐵礦(主要成分為FeCO3),從化學的角度分析“磁鐵礦作煉鐵原料更具優勢”,其原因是。
②近代工業上采用電解熔融氧化鋁(Al2O3)的方法冶煉鋁,Al2O3分解后得到兩種單質,該反應的化學方程式為。
(3)鎂鋁合金被譽為“21世紀綠色金屬結構材料”。一種鎂鋁合金Mg17Al12是特殊的儲氫材料,完全吸收氫氣后得到MgH2和Al,該反應的化學方程式為。
(4)鈦和鈦合金是21世紀重要的金屬材料。鈦合金制品放在海水中數年,取出后仍光亮如新,是因為其(填字母)非常好。
A.可塑性
B.機械性能
C.抗腐蝕性能
(5)鐵在潮濕的空氣中反應生成疏松的鐵銹。已知:Fe2O3+6HCl═2FeCl3+3H2O,2FeCl3+Fe═3FeCl2。
①鐵銹的主要成分是(填化學式),寫出一種防止鋼鐵生銹的方法:。
②將10g表面生銹的鐵釘(雜質已忽略)浸泡在100g含HCl 7.3%的稀鹽酸中充分反應,觀察到鐵銹已完全消失。反應停止后,取出光亮的鐵釘洗滌、干燥、稱量,質量為3.6g,則原生銹鐵釘中鐵元素的質量分數為。
(6)利用“活潑金屬”可以制得H2,可用作汽車能源。若推廣應用于汽車產業,則需綜合考慮的因素有(填字母)。
A.金屬原料的成本
B.生產過程中的能耗和污染
C.金屬的回收利用組卷:6引用:1難度:0.5


