2021年北京市海淀區高考化學二模試卷
發布:2024/12/6 3:30:2
一、本部分共14題,每題3分,共42分。在每題列出的四個選項中,選出最符合題目要求的一項。
-
1.下列安全標識不適合在加油站張貼的是( )
A. 
禁止吸煙B. 
熄火加油C. 
當心電離輻射D. 
當心火災組卷:36引用:3難度:0.6 -
2.下列化學用語正確的是( )
A.氨的電子式: 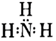
B.中子數為20的Cl的核素: Cl2017C.甲烷的球棍模型: 
D. 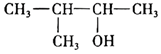 的系統命名:3-甲基-2-丁醇組卷:28引用:2難度:0.6
的系統命名:3-甲基-2-丁醇組卷:28引用:2難度:0.6 -
3.下列說法不正確的是( )
A.水泥、玻璃和陶瓷均屬于無機非金屬材料 B.麥芽糖在酸或酶的催化下可水解為葡萄糖 C.煤的干餾是實現煤綜合利用的主要途徑之一 D.利用油脂在堿性條件下的水解反應可獲得人造脂肪 組卷:61引用:2難度:0.8 -
 4.某品牌牙膏的成分含水、丙三醇、二氧化硅、苯甲酸鈉、十二烷基硫酸鈉和氟化鈉等。已知:牙釉質中含有羥基磷酸鈣[Ca5(PO4)3OH],是牙齒的保護層。在牙齒表面存在平衡:Ca5(PO4)3OH(s)?5Ca2+(aq)+3PO43-(aq)+OH-(aq);Ksp[Ca5(PO)3OH]>Ksp[Ca5(PO)3F]。下列說法不正確的是( )
4.某品牌牙膏的成分含水、丙三醇、二氧化硅、苯甲酸鈉、十二烷基硫酸鈉和氟化鈉等。已知:牙釉質中含有羥基磷酸鈣[Ca5(PO4)3OH],是牙齒的保護層。在牙齒表面存在平衡:Ca5(PO4)3OH(s)?5Ca2+(aq)+3PO43-(aq)+OH-(aq);Ksp[Ca5(PO)3OH]>Ksp[Ca5(PO)3F]。下列說法不正確的是( )A.若使牙膏呈弱酸性,更有利于保護牙釉質 B.丙三醇的俗稱是甘油 C.SiO2是摩擦劑,有助于去除牙齒表面的污垢 D.NaF能將Ca5(PO4)3OH轉化為更難溶的Ca5(PO4)3F,減少齲齒的發生 組卷:88引用:2難度:0.5 -
5.用下列儀器或裝置進行相應實驗,能達到實驗目的的是( )
A. 
蒸發結晶制備NaHCO3晶體B. 
分離苯和溴苯C. 
實驗室制取蒸餾水D. 
配制100mL 0.100mol/L NaCl溶液組卷:32引用:1難度:0.5 -
6.下列方程式與所給事實不相符的是( )
A.向KMnO4酸性溶液中滴加H2C2O4溶液,溶液褪色:2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O B.向沸水中滴加飽和FeCl3溶液,Fe(OH)3膠體:Fe3++3H2O Fe(OH)3↓+3H+△C.向銀氨溶液中滴加乙醛,水浴加熱,析出光亮銀鏡:CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O△D.Na2O2用作潛水艇供氧劑:2Na2O2+2H2O═4NaOH+O2↑;2Na2O2+2CO2═2Na2CO3+O2 組卷:107引用:3難度:0.5
二、本部分共5題,共58分。
-
18.具有十八面體結構的Ag3PO4晶體是一種高效光催化劑,可用于實現“碳中和”,也可用于降解有機污染物。
Ⅰ.配位-沉淀法制備Ag3PO4高效光催化劑
已知:ⅰ.Ag3PO4難溶于水,可溶于硝酸;
ⅱ.Ag3PO4沉淀的生成速率會影響其結構和形貌,從而影響其光催化性能;
ⅲ.銀氨溶液中存在:Ag(NH3)2+?Ag++2NH3
(1)配制銀氨溶液時的反應現象是。
(2)加入Na2HPO4溶液時,發生以下反應,請將離子方程式補充完整:Ag(NH3)2+++=NH3++。
(3)AgNO3和Na3PO4在溶液中反應也可制得Ag3PO4固體,但制得的Ag3PO4固體光催化性能極差。從速率角度解釋其原因:。
Ⅱ.Ag3PO4光催化劑的使用和再生
已知:Ag3PO4晶體在光照條件下發揮催化作用時,首先引發反應。a.Ag3PO4[Ag3PO4]⊕+e-可見光
(4)Ag3PO4光催化CO2制備甲醇可實現“碳中和”,a的后續反應:2H2O+4[Ag3PO4]⊕O3+4H++4Ag3PO4,CO2+6e-+6H+=CH3OH+H2O,則由CO2制備甲醇的總反應的化學方程式為可見光。
(5)Ag3PO4光催化降解RhB(代表有機污染物),RhB被氧化成CO2和H2O。a的后續反應O2+e-=,H2O+[Ag3PO4]⊕=H++?OH+Ag3PO4O-2
注:Ag3PO4在該催化過程中可能發生光腐蝕,生成單質銀,影響其光催化性能。
用Ag3PO4依次降解三份相同的廢水,測得3次降解過程中RhB的殘留率(c/co:即時濃度與起始濃度之比)隨時間變化的曲線如圖。
①下列說法正確的是(填字母序號)。
a.?OH和是降解RhB的重要氧化劑O-2
b.第1次使用后Ag3PO4的光催化性能降低
c.該實驗條件下,Ag3PO4使用兩次即基本失效
②第1次光降解時,0~25min內的反應速率為mol/(L?min)(廢水中RhB初始濃度co為100mg/L,RhB的摩爾質量為Mg/mol)。組卷:128引用:3難度:0.4 -
19.實驗小組探究不同濃度CuCl2溶液的電解反應。分別用石墨電極電解0.1mol/LCuCl2溶液和5mol/LCuCl2溶液,記錄實驗現象如下表。
(1)經檢驗,陽極產生的氣體能使濕潤的淀粉KI試紙變藍。①中電解反應的化學方程式為實驗裝置 實驗編號及試劑 實驗現象 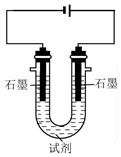
①0.1mol/LCuCl2溶液(藍色) 陽極:產生有刺激性氣味的氣體
陰極:電極上有紅色固體析出②5mol/LCuCl2溶液(綠色) 陽極:產生有刺激性氣味的氣體
陰極:電極上有少量紅色固體和白色固體析出,同時電極附近液體變為黑色。
Ⅰ.探究②中產生白色固體的原因。
查閱資料:
ⅰ.陰極附近的白色固體為CuCl,Ksp(CuCl)=1.2×10-6;
ⅱ.Cu+在水溶液中單獨存在時不穩定,容易發生反應:2Cu+(aq)?Cu(s)+Cu2+(aq)。
結合資料分析CuCl產生的路徑有如下兩種可能:
(2)路徑1:陰極發生電極反應分兩步:
ⅰ.
ⅱ.Cu++e-=Cu,同時伴隨反應Cu++Cl-=CuCl↓,生成白色沉淀。
(3)路徑2:陰極發生電極反應Cu++e-=Cu,而后發生反應a:(寫出離子方程式),生成白色沉淀。同學們通過實驗證明反應a可以發生,其實驗操作和現象是。
Ⅱ.探究②中陰極區液體中黑色物質的成分。
進一步查閱資料,提出以下猜想。
猜想1.生成氫氧化銅,進而轉化為極細小的氧化銅;
猜想2.生成銅的速率快,形成黑色納米銅;
猜想3.發生反應Cu2++Cu++4Cl-+H2O?[Cu(Ⅱ)Cu(Ⅰ)Cl4(H2O)]-(棕黑色)。
(4)若猜想1成立,則陰極一定還存在的電極反應是。
取2mL黑色液體于試管中,分別加入不同試劑,記錄實驗現象如下表。
(5)甲同學根據實驗③產生的現象得出結論:黑色液體中一定有納米銅。乙同學認為甲同學的結論不合理,他做出判斷的依據是實驗編號 ③ ④ ⑤ 加入試劑 4mL濃HNO3 4mL濃HCl 4mLH2O 實驗現象 溶液變澄清,呈綠色,試管口有淺紅棕色氣體生成 黑色液體顏色變深 溶液變澄清,呈綠色,同時出現少量白色沉淀 。
(6)由上述實驗可得到的關于黑色物質成分的結論是。組卷:124引用:2難度:0.5


