2021-2022學年河南省焦作市高一(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共16小題,每小題3分,共48分.在每小題給出的四個選項中,只有一項是符合題目要求的.
-
1.下列活動或現象不涉及氧化還原反應的是( )
A.工業煉鐵 B.光合作用 C.鋼鐵銹蝕 D.石灰硬化 組卷:6引用:2難度:0.6 -
2.工業生產中多采用廉價的石灰乳吸收氣體,如用石灰乳吸收工業廢氣中的Cl2:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O。下列說法正確的是( )
A.中子數為22的鈣原子: Ca2220B.Cl-的結構示意圖: 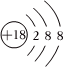
C.該反應中的氧化劑是Ca(OH)2 D.Ca(ClO)2是漂白粉的有效成分 組卷:3引用:1難度:0.7 -
3.化學與生活、生產、科學技術有密切關系.下列說法正確的是( )
A.豆腐具有丁達爾效應 B.制造飛機的硬鋁為含銅、鎂等的鋁合金 C.在鐵強化醬油中加入鐵粉作為鐵強化劑 D.氕、氘、氚均可用于制造“兩彈一星”中的氫彈 組卷:1引用:1難度:0.6 -
4.下列實驗操作錯誤的是( )
A.用沸水制備Fe(OH)3膠體時,需佩戴護目鏡 B.將氯氣尾氣通入NaOH溶液中,以防止污染 C.將金屬鈉放在表面皿中進行鈉的燃燒實驗 D.在規格為500mL的燒杯中盛200mL水,進行鈉與水的反應實驗 組卷:7引用:1難度:0.7 -
5.下列說法正確的是( )
A.堿金屬單質在氧氣中燃燒均生成過氧化物 B.堿金屬單質均能與水反應生成氫氣 C.鹵素單質與氫氣化合均需光照或加熱 D.氫鹵酸均為強酸 組卷:27引用:1難度:0.7 -
6.同溫同壓下,對于相同質量的CH4氣體和HF氣體,下列說法錯誤的是( )
A.分子數之比為5:4 B.密度之比為4:5 C.體積之比為4:5 D.共價鍵數之比為5:1 組卷:7引用:1難度:0.6 -
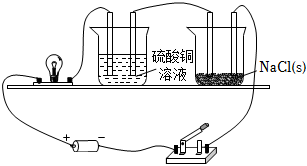 7.如圖是電解質導電實驗裝置,接通電源后,下列說法正確的是( )
7.如圖是電解質導電實驗裝置,接通電源后,下列說法正確的是( )A.CuSO4、NaCl均為電解質,燈泡亮起來 B.在NaCl粉末中加入適量水,燈泡會亮起來 C.CuSO4的電離方程式:CuSO4 Cu2++SO42-通電D.將NaCl(s)改為NaCl溶液,在CuSO4溶液中加入少量NaOH固體,燈泡明顯變暗 組卷:29引用:1難度:0.6
二、非選擇題:本題共5小題,共52分.
-
20.聚合氯化鋁鐵[AlFe(OH)nCl6-n]m廣泛應用于生活污水和工業污水的處理.一種以某工業金屬廢料(主要含Fe、Al、Fe2O3、Al2O3)為原料制備聚合氯化鋁鐵的工藝流程如圖:
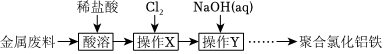
回答下列問題:
(1)聚合氯化鋁鐵中鐵元素的化合價是.
(2)“酸溶”后的混合液中金屬陽離子一定有,檢驗該混合液中是否存在Fe3+的試劑是(填標號).
a.KSCN溶液
b.KMnO4溶液
c.NaOH溶液
(3)“操作X”是向混合液體系中通入Cl2,目的是.若測得混合液中c(Fe2+)=1.2mol?L-1,則向1m3該混合液中至少通入L(標準狀況)Cl2.
(4)“操作Y”是向混合液中加入適量的NaOH溶液,若NaOH溶液過量,則會導致制備失敗,寫出NaOH過量時Fe3+、Al3+分別發生反應的離子方程式:.組卷:7引用:1難度:0.4 -
21.侯德榜是我國近代著名的化工學家,為我國化工事業的發展做出了卓越的貢獻,其貢獻之一是發明了聯合制堿法(即侯氏制堿法),該法先制備出NaHCO3再受熱分解生成純堿,如圖是NaHCO3分解及CO2與Na2O2反應的實驗.回答下列問題:
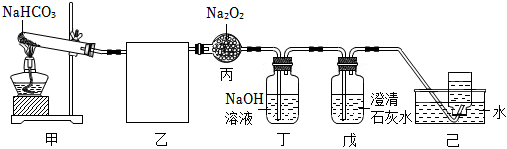
(1)侯氏制堿法的原料是飽和食鹽水、CO2、NH3,寫出侯氏制堿法中生成NaHCO3的離子方程式:.
(2)裝置乙為(填標號).
a.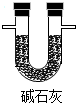 b.
b.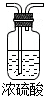 c.
c.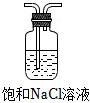 d.
d.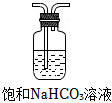
(3)裝置丙的名稱是,其中反應的化學方程式是,該反應中氧化劑與還原劑的質量比為.
(4)裝置丁中NaOH溶液的作用是,裝置戊中澄清石灰水的作用是.
(5)裝置甲中用托盤天平稱取的NaHCO3的質量如圖,則理論上裝置乙中收集的氣體體積在標準狀況下為L.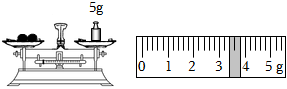 組卷:13引用:2難度:0.7
組卷:13引用:2難度:0.7


