2022年山東省濰坊一中學業水平等級考化學模擬試卷(一)
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每小題2分,共20分。每小題只有一個選項符合題意。
-
1.沈括《夢溪筆談》卷三云:“凡鐵之有鋼者,如面中有筋,濯盡柔面,則面筋乃見。煉鋼亦然,但取精鐵,鍛之百余火,每鍛稱之,一鍛一輕,至累鍛而斤兩不減,則純鋼也,雖百煉不耗矣。此乃鐵之精純者,其色清明,磨瑩之,則黯黯然青且黑,與常鐵迥異。亦有煉之至盡而全無鋼者,皆系地之所產。”下列說法正確的是( )
A.“純鋼”是一種純金屬材料 B.“百煉成鋼”的化學意義就是使用還原劑降低生鐵中碳的含量 C.用含硫較多的生鐵煉鋼,可加入生石灰 D.“煉之至盡而全無鋼”是技術的原因 組卷:10引用:1難度:0.6 -
2.下列敘述Ⅰ和敘述Ⅱ均正確并有因果關系的是( )
選項 敘述Ⅰ 敘述Ⅱ A Cl2和SO2均能用于漂白 用Cl2和SO2的混合氣體漂白有色物質效果更佳 B Fe具有還原性 可用鐵粉作包裝食品的除氧劑 C 濃硫酸具有脫水性 濃硫酸用作干燥劑 D 氫氟酸用于雕刻玻璃 SiO2是兩性氧化物 A.A B.B C.C D.D 組卷:31引用:1難度:0.5 -
3.下列實驗裝置不能達到目的的是( )
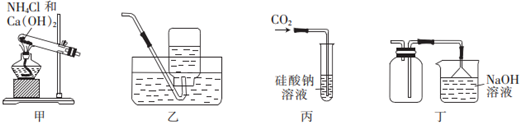
A.用甲裝置制取少量氨氣 B.用乙裝置收集NO C.用丙裝置驗證碳的非金屬性比硅強 D.用丁裝置收集SO2并進行尾氣處理 組卷:16引用:1難度:0.5 -
4.一定條件下發生反應:Fe+6HCN+2K2CO3=K4[Fe(CN)6]+H2↑+2CO2↑+2H2O。下列說法正確的是( )
A.K4[Fe(CN)6]的中心原子的核外電子排布式為[Ar]3d5 B.該反應中只存在離子鍵和共價鍵的斷裂和形成 C.HCN、CO2、CO32-中碳的雜化方式和空間構型均相同 D.HCN水溶液中存在4種氫鍵 組卷:36引用:2難度:0.7 -
5.在實驗室中,下列除去雜質的方法正確的是( )
A.乙酸乙酯中混有乙醇,加入氫氧化鈉溶液,振蕩、靜置后過濾 B.乙烷中混有乙烯,通入氫氣在一定條件下反應,使乙烯轉化為乙烷 C.甘油中混有乙酸,加入濃燒堿溶液,振蕩、靜置后分液 D.硝基苯中混有濃硝酸和濃硫酸,將其倒入濃燒堿溶液中,振蕩、靜置后分液 組卷:17引用:1難度:0.5 -
6.磷酸鋯結合劑可用氫氧化鋯[Zr(OH)4]與正磷酸(H3PO4)反應制得,磷酸鋯結合劑中具有膠結性能的化合物為磷酸二氫鋯和磷酸一氫鋯,也即中和度Nm[Nm=
]在0.5~1之間的物質具有膠結性能。當Nm=0.8時,該結合劑中磷酸二氫鋯和磷酸一氫鋯的物質的量之比為( )n(ZrO2)n(P2O5)A.1:3 B.2:3 C.2:5 D.4:5 組卷:17引用:3難度:0.7
三、非選擇題:本題共5小題,共60分。
-
19.5-氯-6-(2,3-二氯苯氧基)-2-甲硫基-1H-苯并咪唑對各種日齡的肝片形吸蟲均有明顯驅殺效果,其在醫藥工業中的一種合成路線如圖:
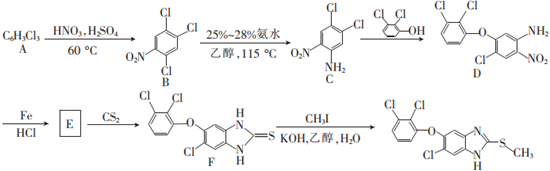
已知: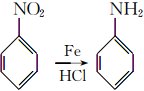 。
。
回答下列問題:
(1)A的化學名稱是,1molA完全反應生成B至少需要molHNO3參加反應。
(2)C中官能團的名稱是。
(3)C→D的反應類型為。
(4)已知E→F的化學反應還生成一種小分子物質,寫出E→F的化學方程式:。
(5)B的同分異構體中,與B所含官能團種類和數目均相同的芳香化合物還有種。
(6)參照上述合成路線,為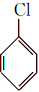 原料,設計合成
原料,設計合成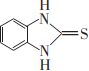 的路線 。組卷:90引用:1難度:0.5
的路線 。組卷:90引用:1難度:0.5 -
20.據統計,有90%以上的工業過程需要使用催化劑,因此,催化劑的研究已成為重要課題。
Ⅰ.結合實驗與計算機模擬結果,研究了N2與H2在固體催化劑表面合成NH3的反應歷程。圖1為反應歷程中的勢能面圖(部分數據省略),其中吸附在催化劑表面的物種用*標注。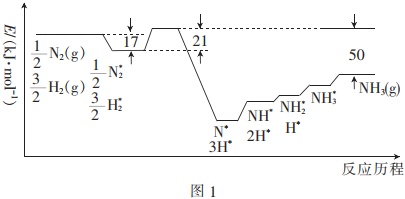
(1)氨氣的脫附是(填“吸熱”或“放熱”)過程,合成氨的熱化學方程式為。
(2)向某容器中充入物質的量之比為1:3的N2和H2,在不同條件下反應相同的時間,得到NH3的體積分數如圖2所示。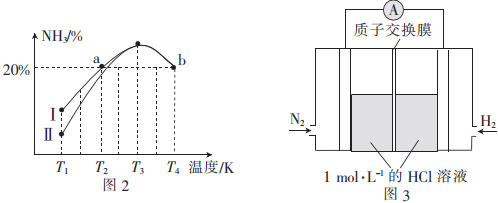
①圖中曲線Ⅰ與Ⅱ(填“能”或“不能”)表示不同的壓強條件下反應得出的兩條曲線。
②a點時正、逆反應速率大小:v正(填“>”、“<”或“=”)v逆。
③若容器體積恒為1L,N2和H2的總物質的量為4mol,則T4K時該反應的平衡常數為。
(3)美國化學家發明了一種新型催化劑可以在常溫下合成氨,將其附著在電池的正、負極上實現氮的電化學固定,其裝置示意圖如圖3所示,則開始階段正極反應式為;忽略過程中溶液體積變化,當電池中正極區溶液pH=7時,溶液中NH3?H2O的濃度為(Kb=2×10-5)。
Ⅱ.用催化劑催化CO2加氫合成乙烯的過程中,還會生成CH4、C3H6、C4H8等副產物,在催化劑中添加Na、K、Cu助劑(助劑也起催化作用)可改變反應的選擇性(選擇性指的是轉化的CO2中生成C2H4的百分比)。在其他條件相同時,添加不同助劑,經過相同時間后測得CO2轉化率和各產物的物質的量分數如表所示。
(4)欲提高單位時間內乙烯的產量,在Fe3(CO)12/ZSM-5中添加助劑 CO2轉化率(%) 各產物在所有產物中的占比(%) C2H4 C3H6 其他 Na 42.5 35.9 39.6 24.5 K 27.2 75.6 22.8 1.6 Cu 9.8 80.7 12.5 6.8 助劑效果最好。組卷:30引用:1難度:0.3


