2022年北京市西城區高考化學二模試卷
發布:2024/4/20 14:35:0
一、本部分共14題,每題3分,共42分。在每題列出的四個選項中,選出最符合題目要求的一項。
-
1.將氧化還原反應拆解為氧化反應和還原反應的分析過程,蘊含的化學學科的思想方法是( )
A.分與合相結合 B.量變與質變相結合 C.化學與社會和諧發展 D.物質變化是有條件的 組卷:32引用:3難度:0.7 -
2.下列圖示正確的是( )
A.3p電子的電子云輪廓圖: 
B.SO3的VSEPR模型: 
C.As的原子結構示意圖: 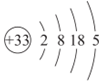
D.H-Cl的形成過程: 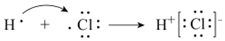 組卷:86引用:5難度:0.6
組卷:86引用:5難度:0.6 -
3.下列事實不能直接從原子結構角度解釋的是( )
A.化合物ICl中I為+1價 B.第一電離能:B>Al C.沸點:CS2>CO2 D.熱穩定性:NH3>PH3 組卷:106引用:8難度:0.7 -
 4.我國擁有獨立知識產權的抗高血壓藥物左旋氨氯地平的分子具有手性,其結構簡式如圖。下列關于左旋氨氯地平的說法不正確的是( )
4.我國擁有獨立知識產權的抗高血壓藥物左旋氨氯地平的分子具有手性,其結構簡式如圖。下列關于左旋氨氯地平的說法不正確的是( )A.分子中含有酯基 B.酸性條件下的所有水解產物均能與NaHCO3溶液反應 C.能與H2發生加成反應 D.有手性異構體 組卷:71引用:5難度:0.6 -
5.向含HCN的廢水中加入鐵粉和K2CO3可制備K4[Fe(CN)6],反應如下:6HCN+Fe+2K2CO3=K4[Fe(CN)6]+H2↑+2CO2↑+2H2O,下列說法不正確的是( )
A.依據反應可知:Ka(HCN)>Ka1(H2CO3) B.HCN的結構式是H—C≡N C.反應中每1mol Fe轉移2mol電子 D.[Fe(CN)6]4-中Fe2+的配位數是6 組卷:44引用:7難度:0.6 -
6.下列實驗方案能達到相應實驗目的的是( )
選項 實驗目的 實驗方案 A 制備無水FeCl3固體 將FeCl3溶液加熱蒸干 B 檢驗濃H2SO4催化纖維素水解的產物含有還原糖 向水解后的溶液中加入新制的Cu(OH)2,加熱 C 配制1L1.0mol/LNaCl溶液 將58.5gNaCl固體直接溶于1L水中 D 證明醋酸是弱電解質 測0.1mol/LCH3COOH溶液的pH A.A B.B C.C D.D 組卷:45引用:1難度:0.7
二、第二部分本部分共5題,共58分。
-
18.向含有NaOH的NaClO溶液中逐滴滴入FeSO4溶液,滴加過程中溶液的pH隨FeSO4溶液的體積的變化曲線及實驗現象見下表。
資料:i.飽和NaClO溶液的pH約為11變化曲線 實驗現象 
i.A→B產生紅褐色沉淀
ii.B→C紅褐色沉淀的量增多
iii.C→D紅褐色沉淀的量增多
iv.D點附近產生有刺激性氣味的氣體
v.D→E紅褐色沉淀的量略有增多
ii.Ksp[Fe(OH)3]=2.8×10-39
(1)Cl2和NaOH溶液制取NaClO的離子方程式是。
(2)A點溶液的pH約為13,主要原因是。
(3)結合離子方程式解釋A→B溶液的pH顯著下降的主要原因:。
(4)NaClO溶液中含氯各微粒的物質的量分數與pH的關系如圖。
①M點溶液含氯的微粒有。
②C點附近生成紅褐色沉淀的主要反應的離子方程式是。
(5)檢驗iv中氣體的方法是。
(6)A→D的過程中,溶液的pH一直下降,原因是。
(7)整個滴加過程中發生的反應與、微粒的濃度等有關。組卷:53引用:2難度:0.6 -
19.在處理NO廢氣的過程中,催化劑[Co(NH3)6]2+會逐漸失活變為[Co(NH3)6]3+。某小組為解決這一問題,實驗研究
和+2Co之間的相互轉化。+3Co
資料:i.Ksp[Co(OH)2]=5.9×10-15、Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3?Co(NH3)6]2+;K1=1.3×105
Co3++6NH3?[Co(NH3)6]3+;K2=2×1035
ii.[Co(NH3)6]2+和[Co(NH)6]3+在酸性條件下均能生成NH+4
(1)探究的還原性+2Co
實驗Ⅰ粉紅色的CoCl2溶液或CoSO4溶液在空氣中久置,無明顯變化。
實驗Ⅱ向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,無明顯變化。
實驗Ⅲ按如圖裝置進行實驗,觀察到電壓表指針偏轉。
①甲同學根據實驗Ⅰ得出結論:Co2+可以被酸性KMnO4溶液氧化。乙同學補充實驗Ⅲ,(補全實驗操作及現象),否定了該觀點。
②探究堿性條件下的還原性,進行實驗。+2Co
ii中反應的化學方程式是。
③根據氧化還原反應規律解釋還原性Co(OH)2>Co2+:Co2+-e-=Co3+在堿性條件下,OH-與Co2+、Co3+反應,使c(Co2+)和c(Co3+)均降低,但降低的程度更大,還原劑的還原性增強。
(2)探究Co的氧化性
①根據實驗Ⅱ和Ⅳ推測氧化性:Co3+>Cl2,設計實驗證明:向V中得到的棕褐色沉淀中,( 補全實驗操作及現象),反應的離子方程式是。
②向V中得到的棕褐色沉淀中,滴加H2SO4溶液,加入催化劑,產生無色氣泡,該氣體是。
(3)催化劑[Co(NH3)6]2+的失活與再生
①結合數據解釋[Co(NH)6]2+能被氧化為[Co(NH3)6]3+而失活的原因:。
②根據以上實驗,設計物質轉化流程圖實現[Co(NH3)6]2+的再生:。
實例:CoCoCl2Cl2Co(OH)2NaOH組卷:115引用:2難度:0.2


