2015-2016學年河南省洛陽市宜陽一高高二(上)第一周周練化學試卷(12月份)
發(fā)布:2024/4/20 14:35:0
一.選擇題(共16小題)
-
1.向足量H2SO4溶液中加入100mL 0.4mol?L-1Ba(OH)2溶液,放出的熱量是5.12kJ,如果向足量Ba(OH)2溶液中加入100mL 0.4mol?L-1鹽酸時,放出的熱量為2.2kJ.則Na2SO4溶液與BaCl2溶液反應的熱化學方程式為( )
A.Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-2.92kJ?mol-1 B.Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-18kJ?mol-1 C.Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-73kJ?mol-1 D.Ba2+(aq)+SO42-(aq)═BaSO4(s)△H=-0.72kJ?mol-1 組卷:52引用:23難度:0.7 -
2.在測定中和反應反應熱的實驗中,下列敘述錯誤的是( )
A.向量熱計中加入鹽酸,攪拌后的溫度為初始溫度 B.實驗中可使酸或堿略過量 C.向量熱計中加堿液時,堿液的溫度應與酸的溫度相同 D.可以用氫氧化鉀代替氫氧化鈉,濃硫酸代替鹽酸 組卷:177引用:4難度:0.9 -
3.下表中列出了25℃、101kPa時一些物質的燃燒熱數(shù)據(jù)
已知鍵能:C-H鍵:413.4kJ?mol-1、H-H鍵:436.0kJ?mol-1.則下列敘述正確的是( )物質 CH4 C2H2 H2 燃燒熱/kJ?mol-1 890.3 1299.6 285.8 A.C≡C鍵能為796.0 kJ?mol-1 B.C-H鍵鍵長小于H-H鍵 C.2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ?mol-1 D.2CH4(g)═C2H2(g)+3H2(g)△H=-376.4 kJ?mol-1 組卷:303引用:4難度:0.5 -
4.以下反應中,△H1>△H2 的是( )
A.S(s)+O2(g)→SO2(g)△H1 S(g)+O2(g)→SO2(g)△H2 B.2H2(g)+O2(g)→2H2O(l)△H 1 2H2(g)+O2(g)→2H2O(g)△H2 C.NaOH(aq)+HCl(aq)→NaCl(aq)+H2O(l)△H1 NaOH(aq)+CH3COOH(aq)→CH3COONa(aq)+H2O(l)△H2 D.H2(g)+F2(g)→2HF(g)△H1 H2(g)+Cl2(g)→2HCl(g)△H2 組卷:421引用:2難度:0.1 -
5.已知298K時反應2SO2( g )+O2( g )?2SO3( g );△H=-197kJ?mol-1,在相同溫度下向一密閉容器中加入2molSO2和1molO2,達化學平衡時放出熱量為a1 kJ;向另一容積相同的密閉容器中通入1molSO2和0.5molO2,達化學平衡時放出熱量為a2kJ,則下列關系式中正確的是( )
A.a2<a1<197 B.2a2>a1>197 C.2a2=a1>197 D.2a2=a1=197 組卷:65引用:2難度:0.5 -
6.某體積可變的密閉容器,盛有適量的A和B的混合氣體,在一定條件下發(fā)生反應:A+3B
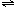 2C若維持溫度和壓強不變,當達到平衡時,容器的體積為V升,其中C氣體的體積占10%,下列推斷正確的是( )
2C若維持溫度和壓強不變,當達到平衡時,容器的體積為V升,其中C氣體的體積占10%,下列推斷正確的是( )
①原混和氣體的體積為1.2V升;
②原混和氣體的體積為1.1V升;
③反應達平衡時氣體A消耗掉0.05V升;
④反應達平衡時氣體B消耗掉0.05V升.A.②③ B.②④ C.①③ D.①④ 組卷:2683引用:48難度:0.5 -
7.在一定溫度下,向a L密閉容器中加入1mol X氣體和2mol Y氣體,發(fā)生如下反應:X(g)+2Y(g)?2Z(g),此反應達到平衡的標志是( )
A.容器內氣體密度不隨時間變化 B.v(X):v(Y)=1:2 C.容器內X、Y、Z的濃度不隨時間變化 D.單位時間消耗0.1molX同時生成0.2molZ 組卷:2956引用:12難度:0.9
二.簡單題(共7小題)
-
22.重鉻酸鈉(Na2Cr2O7?2H2O)俗稱紅礬鈉,在工業(yè)方面有廣泛用途.我國目前主要是以鉻鐵礦(主要成分為FeO?Cr2O3,還含有Al2O3、MgO、SiO2等雜質)為主要原料進行生產,其主要工藝流程如圖:
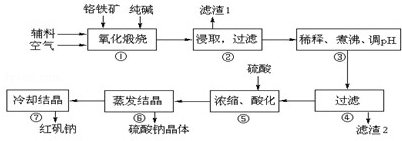
①中涉及的主要反應有:
主反應:4FeO?Cr2O3+8Na2CO3+7O28Na2CrO4+2Fe2O3+8CO2△
副反應:SiO2+Na2CO3Na2SiO3+CO2↑、Al2O3+Na2CO3△2NaAlO2+CO2↑△
部分陽離子以氫氧化物形式完全沉淀時溶液的pH:
試回答下列問題:沉淀物 Al(OH)3 Fe(OH)3 Mg(OH)2 Cr(OH)3 完全沉淀時溶液pH 4.7 3.7 11.2 5.6
(1)“①”中反應是在回轉窯中進行,反應時需不斷攪拌,其作用是.
(2)“③”中調節(jié)pH至4.7,目的是.
(3)“⑤”中加硫酸酸化的目的是使CrO42-轉化為Cr2O72-,請寫出該平衡轉化的離子方程式:.
(4)稱取重鉻酸鈉試樣2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol?L-1H2SO4和足量碘化鈉(鉻的還原產物為Cr3+),放于暗處5min,然后加入100mL水,加入3mL淀粉指示劑,用0.1200mol?L-1Na2S2O3標準溶液滴定(I2+2S2O32-═2I-+S4O62-).
①判斷達到滴定終點的依據(jù)是:;
②若實驗中共用去Na2S2O3標準溶液40.00ml,所得產品的中重鉻酸鈉的純度(設整個過程中其它雜質不參與反應).組卷:42引用:4難度:0.3 -
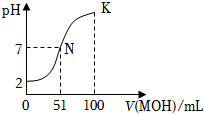 23.常溫下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,圖中所示曲線表示混合溶液的pH變化情況(體積變化忽略不計).回答下列問題:
23.常溫下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,圖中所示曲線表示混合溶液的pH變化情況(體積變化忽略不計).回答下列問題:
(1)由圖中信息可知HA為酸(填“強”或“弱”),理由是
(2)常溫下一定濃度的MA稀溶液的pH=a,則a7(填“>”、“<”或“=”),用離子方程式表示其原因為;,此時,溶液中由水電離出的c(OH-)=.
(3)請寫出K點所對應的溶液中離子濃度的大小關系:
(4)K點對應的溶液中,c(M+)+c(MOH)2c(A-)(填“>”、“<”或“=”);若此時溶液中,pH=10,則c(MOH)+c(OH-)=mol?L-1.組卷:245引用:18難度:0.5


