2021-2022學年黑龍江省哈爾濱三十二中高三(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(每小題只有1個選項符合題意,每小題4分,共60分)
-
1.中國是世界著名的陶瓷古國。下列國寶級文物主要由陶瓷制成的是( )
選項 A B C D 文物 



名稱 東漢銅車馬 舞馬銜杯紋銀壺 蕭何月下追韓信梅瓶 雪景寒林圖 A.A B.B C.C D.D 組卷:38引用:5難度:0.8 -
2.下列化學用語表示不正確的是( )
A.原子核內有8個中子的碳原子: C146B.乙烯的結構簡式:CH2CH2 C.羥基的電子式: 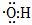
D.硫離子的結構示意圖: 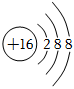 組卷:1引用:3難度:0.7
組卷:1引用:3難度:0.7 -
3.下列有關物質的性質和用途說法不正確的是( )
A.利用高純單質硅的半導體性能,可以制成光電池 B.石灰石在高溫下的分解產物可與SO2反應,可用于減少燃煤煙氣中的SO2 C.Na2O2與CO2反應放出氧氣,可用于制作呼吸面具 D.二氧化硅導電能力強,可用于制造光導纖維 組卷:5引用:3難度:0.6 -
4.近年我國在科學技術領域取得了舉世矚目的成就。對下列成就所涉及的化學知識的判斷錯誤的是( )
A.“奮斗者”號潛水器下沉時要攜帶兩組壓載鐵,生鐵是合金 B.“鯤龍”水陸兩棲飛機的燃料航空煤油屬于純凈物 C.“神舟十三號”運載火箭用到的碳纖維屬于新型無機非金屬材料 D.“嫦娥五號”月球探測器制作五星紅旗用的芳綸屬于合成纖維 組卷:16引用:5難度:0.6 -
5.NA是阿伏加德羅常數的值,下列說法正確的是( )
A.32g環狀S8( 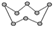 )分子中含有的S-S鍵數為NA
)分子中含有的S-S鍵數為NAB.標準狀況下,2.24LC2H5OH所含氫原子數為0.6NA C.0.1mol?L-1的Na2CO3溶液含 的數目為0.1NACO2-3D.2molNO與1molO2在密閉容器中充分反應后的分子數為2NA 組卷:17引用:7難度:0.8
二、非選擇題(共40分)
-
16.ZnO在化學工業中主要用作橡膠和顏料的添加劑,醫藥上用于制軟膏、橡皮膏等。工業上可由菱鋅礦(主要成分為ZnCO3,還含有Ni、Cd、Fe、Mn等元素)制備。工藝如圖所示:
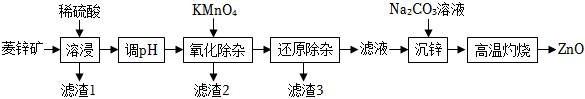
相關金屬離子[c0(Mn+)=0.1mol?L-1]形成氫氧化物沉淀的pH范圍如表:
已知:①“溶浸”后的溶液中金屬離子主要有:Zn2+、Fe2+、Cd2+、Mn2+、Ni2+。金屬離子 Fe3+ Fe2+ Zn2+ Cd2+ Mn2+ Ni2+ 開始沉淀的pH 1.5 6.3 6.2 7.4 8.1 6.9 沉淀完全的pH 2.8 8.3 8.2 9.4 10.1 8.9
②弱酸性溶液中KMnO4能將Mn2+氧化生成MnO2。
③氧化性順序:Ni2+>Cd2+>Zn2+
回答下列問題:
(1)“溶浸”過程中,提高浸出率的措施有。(寫一條即可)
(2)“調pH”是向“溶浸”后的溶液中加入少量(填化學式)調節至弱酸性(pH約為5)。
(3)加KMnO4“氧化除雜”發生反應的離子方程式分別是+3Fe2++7H2O═3Fe(OH)3↓+MnO2↓+5H+和MnO-4。
(4)“還原除雜”除去的離子是;加入的還原劑是。
(5)“沉鋅”生成堿式碳酸鋅[ZnCO3?2Zn(OH)2?2H2O]沉淀,寫出加入Na2CO3溶液沉鋅的化學方程式。組卷:24引用:5難度:0.6 -
17.磷酸亞鐵鋰(LiFePO4)能可逆地嵌入、脫出鋰,使其作為鋰離子電池正極材料的研究及應用得到廣泛關注。通過水熱法制備磷酸亞鐵鋰的一種方法如下(裝置如圖所示):
 Ⅰ.在A中加入40mL蒸餾水、0.01molH3PO4和0.01molFeSO4?7H2O,用攪拌器攪拌溶解后,緩慢加入0.03molLiOH?H2O,繼續攪拌。
Ⅰ.在A中加入40mL蒸餾水、0.01molH3PO4和0.01molFeSO4?7H2O,用攪拌器攪拌溶解后,緩慢加入0.03molLiOH?H2O,繼續攪拌。
Ⅱ.向反應液中加入少量抗壞血酸(即維生素C),繼續攪拌5min。
Ⅲ.快速將反應液裝入反應釜中,保持170℃恒溫5h。
Ⅳ.冷卻至室溫,過濾。
Ⅴ.用蒸餾水洗滌沉淀。
Ⅵ.干燥,得到磷酸亞鐵鋰產品。
回答下列問題:
(1)裝置圖中儀器A的名稱是,根據上述實驗藥品的用量,A的最適宜規格為(填選項)
A.100mL
B.250mL
C.500mL
D.1000mL
(2)步驟Ⅱ中,抗壞血酸的作用是,也可以用Na2SO3代替抗壞血酸,其原理是(用離子方程式表示)。
(3)步驟Ⅳ過濾用到的玻璃儀器除燒杯外還有。
(4)步驟Ⅴ檢驗LiFePO4是否洗滌干凈的方法是。
(5)干燥后稱量,產品的質量是1.2g,本實驗的產率為%(保留小數點后1位)。組卷:11引用:2難度:0.6


