2023-2024學(xué)年江蘇省泰州市姜堰四中九年級(上)第一次月考化學(xué)試卷
發(fā)布:2024/9/11 5:0:9
一、第1題一第10題,每小題只有一個選項符合題意;每小題3分,共10分;第11題~第15題,每小題有一個或兩個選項符合題意,每小題3分,共10分。
-
1.經(jīng)過一段時間的化學(xué)學(xué)習(xí),相信同學(xué)們已經(jīng)對化學(xué)有一定的認(rèn)識,下列認(rèn)識不正確的是( )
A.化學(xué)研究物質(zhì)的組成、結(jié)構(gòu)、性質(zhì)、變化、用途和制法 B.實驗是化學(xué)科學(xué)發(fā)展和化學(xué)學(xué)習(xí)的重要途徑 C.物質(zhì)發(fā)生化學(xué)變化時一定伴隨明顯現(xiàn)象 D.化學(xué)能創(chuàng)造出自然界不存在的物質(zhì) 組卷:9引用:1難度:0.7 -
2.下列四個短語中,其原意一定包含化學(xué)變化的是( )
A.花香四溢 B.木已成舟 C.蠟炬成灰 D.海市蜃樓 組卷:17引用:26難度:0.9 -
3.2021年世界環(huán)境日中國主題是“人與自然和諧共生”。下列做法不符合這一理念的是( )
A.廢舊電池回收處理 B.塑料垃圾焚燒處理 C.農(nóng)藥化肥合理使用 D.清潔能源推廣使用 組卷:38引用:4難度:0.7 -
4.如圖是進行木炭在氧氣中燃燒實驗的示意圖,有關(guān)實驗儀器名稱的判斷,錯誤的是( )

A.a(chǎn)是試管夾 B.b是酒精燈 C.c是集氣瓶 D.d是燒杯 組卷:247引用:4難度:0.7 -
5.下列物質(zhì)的用途中,利用其化學(xué)性質(zhì)的是( )
A.金剛石用于切割玻璃 B.金屬銅用于制作導(dǎo)線 C.固體二氧化碳用于制冷劑 D.一氧化碳用于做燃料 組卷:7引用:1難度:0.7 -
6.下列物質(zhì)中,屬于純凈物的是( )
A.從空氣中分離得到的稀有氣體 B.高錳酸鉀加熱完全分解后的剩余物 C.可作氮肥的碳酸氫銨 D.鐵釘銹蝕形成的鐵銹 組卷:2引用:1難度:0.8
二、非選擇題(共40分)
-
19.在實驗室和生活中選擇合適的藥品和裝置可以制取氧氣。
Ⅰ.實驗室用圖1和圖2所示裝置制取并收集氧氣。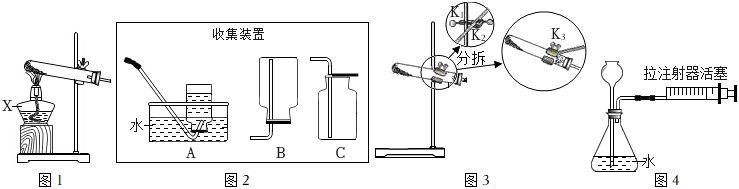
(1)加熱KClO3和MnO2的固體混合物制取氧氣,該反應(yīng)的符號表達式為,該反應(yīng)中MnO2的作用為。
(2)收集干燥氧氣應(yīng)選取的收集裝置為(選填字母)。
(3)搭建如圖2所示裝置時,需要調(diào)整試管的傾斜角度,可松開(選填“K1”、“K2”或“K3”)處的螺絲,待調(diào)整后再擰緊。
(4)用圖1裝置和圖2中A裝置加熱高錳酸鉀制取氧氣的符號表達式,在實驗過程中觀察到的現(xiàn)象時將導(dǎo)管伸入集氣瓶中開始收集,發(fā)現(xiàn)水槽中的水變紅,主要原因是,細心觀察發(fā)現(xiàn)B裝置中的廣口瓶與收集氣體的集氣瓶都有磨砂部分,所不同的是集氣瓶的磨砂部分位于。
A.瓶底內(nèi)壁
B.瓶口邊緣
C.瓶頸內(nèi)壁
D.瓶底外壁
(5)利用圖4裝置實驗室制取氧氣。檢查裝置的氣密性方法為加水浸沒長頸漏斗下端管口,導(dǎo)管上連接一個注射器,向外拉動注射器活塞,觀察到的現(xiàn)象為,說明裝置氣密性良好。
(6)某同學(xué)用如圖所示裝置驗證二氧化碳與水的反應(yīng)。已知氮氣的密度比空氣的小;該裝置氣密性良好,錐形瓶中放入的是用石蕊溶液染成紫色的干燥紙花。具體操作有: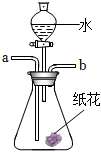
①從a端通入二氧化碳;②從a端通入氮氣;③從分液漏斗中滴加適量水;④從b端通入二氧化碳;⑤從b端通入氮氣。
下列實驗操作順序最合理的是。
A.①②③④
B.④②①③
C.①⑤③①
D.④②③①
(7)如圖是除去粗鹽中難溶性雜質(zhì)實驗的三步操作。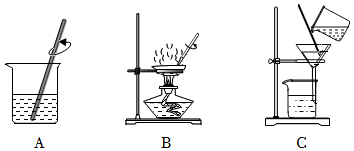
①三步操作的正確順序是(填序號)。
②B中,用玻璃棒不斷攪拌的目的是。
③A中需要控制水的用量,不宜過多,原因有(填序號)。
A.提高實驗效率
B.保證粗鹽全部溶解
C.節(jié)約能源組卷:22引用:1難度:0.5 -
20.某化學(xué)興趣小組進行了“尋找新的催化劑”的如下研究性實驗。
【提出問題】(1)二氧化錳常用作氯酸鉀和過氧化氫分解的催化劑,其它物質(zhì)是否也可以用作該反應(yīng)的催化劑呢?
(2)除了催化劑還有其它因素影響化學(xué)反應(yīng)的速率嗎?
【查閱資料】
研究表明,許多物質(zhì)對氯酸鉀的分解有催化作用,分別用它們作催化劑,氯酸鉀開始發(fā)生反應(yīng)和反應(yīng)劇烈時的溫度如下表所示:
通過分析資料中的數(shù)據(jù),實驗室用氯酸鉀制取氧氣,如果不用二氧化錳作催化劑,最好選用的物質(zhì)是氧化鐵 氧化鋁 氧化銅 氧化鎂 開始反應(yīng) 420℃ 515℃ 305℃ 490℃ 劇烈反應(yīng) 490℃ 540℃ 350℃ 545℃ 。
【實驗探究一】
①將3g氯酸鉀放在試管中加熱。
②將3g氯酸鉀與1g二氧化錳混合均勻后加熱。
③將xg氯酸鉀與1g氧化銅混合均勻后加熱。
④將實驗③反應(yīng)后的固體加水溶解、過濾、洗滌、、稱量,結(jié)果為1g。
⑤將實驗④后得到1g固體和xg氯酸鉀混合均勻后加熱,現(xiàn)象與實驗③相同。
【分析實驗】
(1)實驗③中x的值應(yīng)為。
(2)實驗④過濾操作中需要的玻璃儀器有燒杯、漏斗、,它在操作中的作用是,通過實驗④可以得出的結(jié)論是。
(3)通過實驗⑤可以得出的結(jié)論是。
(4)實驗②③對比的目的是。
【實驗結(jié)論】氧化銅確實也能做氯酸鉀分解的催化劑
【實驗探究二】
影響化學(xué)反應(yīng)的速率除了催化劑以外,還有其它因素嗎?以下是另一實驗小組探究影響過氧化氫反應(yīng)速率部分因素的相關(guān)實驗數(shù)據(jù)。
(1)通過實驗①和②對比可知,化學(xué)反應(yīng)速率還與實驗序號 H2O2溶
液濃度%H2O2溶液體積/mL 溫度℃ MnO2的用量/g 收集氧氣的體積/mL 反應(yīng)所需
的時間/s① 5 1 20 0.1 4 16.75 ② 15 1 20 0.1 4 6.04 ③ 30 5 35 0 2 49.21 ④ 30 5 55 0 2 10.76 有關(guān);
(2)通過對比實驗可知,溫度越高,化學(xué)反應(yīng)速率越快。組卷:184引用:4難度:0.6


