2017-2018學(xué)年山西大學(xué)附中高一(上)模塊化學(xué)試卷(12月份)
發(fā)布:2024/4/20 14:35:0
一、選擇題(包括18小題,每小題3分,共計(jì)54分,每小題只有一個(gè)選項(xiàng)符合題意)
-
1.已知金屬鈉投入水中會(huì)發(fā)生劇烈反應(yīng),并有氫氣生成。運(yùn)輸金屬鈉的包裝箱應(yīng)貼有的圖標(biāo)( )
A. 
易燃液體B. 
遇濕易燃物品C. 
氧化物D. 
腐蝕品組卷:8引用:3難度:0.6 -
2.下列說(shuō)法正確的是( )
A.按分散劑種類(lèi)可將分散系分為溶液、膠體和濁液 B.水玻璃、碘水、Fe(OH)3膠體均為混合物 C.CO2、SO3、CO均屬于酸性氧化物 D.KNO3溶液、Cu、熔融的NaCl均能導(dǎo)電,所以它們都屬于電解質(zhì) 組卷:5引用:1難度:0.8 -
3.合金是一類(lèi)用途廣泛的金屬材料.下列物質(zhì)中,不屬于合金的是( )
A.碳素鋼 B.水銀 C.青銅 D.黃銅 組卷:106引用:13難度:0.7 -
4.用NA表示阿伏加德羅常數(shù),下列敘述中正確的是( )
A.標(biāo)準(zhǔn)狀況下,22.4 L H2O含有的分子數(shù)為NA B.常溫常壓下,1.06 g Na2CO3含有的Na+數(shù)為0.02NA C.常溫常壓下,NA個(gè)CO2分子占有的體積為22.4 L D.物質(zhì)的量濃度為0.5 mol?L-1的MgCl2溶液中含有Cl-個(gè)數(shù)為NA 組卷:1140引用:27難度:0.9 -
5.下列離子方程式中,不正確的是( )
A.Na放入水中,產(chǎn)生氣體:2Na+2H2O═2Na++2OH-+H2↑ B.FeCl3溶液滴在淀粉碘化鉀試紙上,試紙變藍(lán):Fe3++2I-═2Fe2++I2 C.玻璃刻蝕:SiO2+4H++4Cl-═SiCl4+H2O D.Al片置于NaOH溶液中,產(chǎn)生氣體:2Al+2OH-+2H2O═2AlO2-+3H2↑ 組卷:5引用:1難度:0.7 -
6.某無(wú)色溶液能溶解Al(OH)3,則此溶液中一定能大量共存的離子組是( )
A.Fe2+、Cl-、Na+、 NO-3B.K+、Na+、 、NO-3HCO-3C.Na+、Ba2+、Cl-、 NO-3D.Na+、K+、 、AlO-2SO2-4組卷:56引用:6難度:0.9 -
7.已知單位體積的稀溶液中,非揮發(fā)性溶質(zhì)的分子或離子數(shù)越多,該溶液的沸點(diǎn)就越高,下列溶液沸點(diǎn)最高的是( )
A.0.01 mol?L-1的蔗糖溶液 B.0.01 mol?L-1的CaCl2溶液 C.0.02 mol?L-1的NaCl溶液 D.0.02 mol?L-1的氨水 組卷:30引用:4難度:0.9
二、非選擇題
-
22.已知某純堿試樣中含有NaCl雜質(zhì),為測(cè)定試樣中純堿的質(zhì)量分?jǐn)?shù),可用圖中的裝置進(jìn)行實(shí)驗(yàn)。

主要實(shí)驗(yàn)步驟如下:
①按圖組裝儀器,并檢查裝置的氣密性。
②將ag試樣放入錐形瓶中,加適量蒸餾水溶解,得到試樣溶液。
③稱(chēng)量盛有堿石灰的U型管的質(zhì)量,得到bg。
④從分液漏斗滴入6mol/L的硫酸,直到不再產(chǎn)生氣體時(shí)為止。
⑤從導(dǎo)管A處緩緩鼓入一定量的空氣。
⑥再次稱(chēng)量盛有堿石灰的U型管的質(zhì)量,得到cg。
⑦重復(fù)步驟⑤和⑥的操作,直到U型管的質(zhì)量基本不變,為dg。
請(qǐng)?zhí)羁蘸突卮饐?wèn)題:
(1)在用托盤(pán)天平稱(chēng)量樣品時(shí),如果天平的指針向左偏轉(zhuǎn),說(shuō)明
(2)裝置中干燥管B的作用是
(3)如果將分液漏斗中的硫酸換成濃度相同的鹽酸,測(cè)試的結(jié)果(填“偏 高”、“偏低”或“不變”)。
(4)步驟⑤的目的是
(5)步驟⑦的目的是
(6)該試樣中純堿的質(zhì)量分?jǐn)?shù)的計(jì)算式為。組卷:16引用:3難度:0.7 -
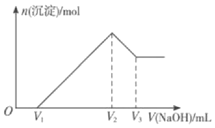 23.將mgAl2O3和Fe2O3的混合物溶于100mL鹽酸中,然后逐滴加入1mol/LNaOH溶液,其結(jié)果如圖所示:
23.將mgAl2O3和Fe2O3的混合物溶于100mL鹽酸中,然后逐滴加入1mol/LNaOH溶液,其結(jié)果如圖所示:
(1)最初加入V1mLNaOH溶液的作用是;
(2)鹽酸的物質(zhì)的量濃度是;
(3)若 m g 混合物中Al2O3和Fe2O3按不同比例進(jìn)行上述實(shí)驗(yàn)(其他條件不變),則V2的值會(huì)不會(huì)改變(填“會(huì)”或“不會(huì)”),(V2-V1)的取值范圍是。組卷:9引用:2難度:0.6


