2021-2022學年北京市昌平區高三(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(共14小題,每小題3分,滿分42分)
-
1.合金的應用極大地促進了人類社會的發展。下列不屬于合金的是( )
A. 
滑雪杖桿(鋁、鎂等)B. 
地鐵阻燃橡膠地板C. 
航母甲板(鋼)D. 
潛水器外殼(鈦、鋁等)組卷:35引用:5難度:0.6 -
2.下列說法中不正確的是( )
A.N2的電子式是 
B.NaOH中既含有離子鍵也含有共價鍵 C.NaF屬于鹽 D.KI是常見的還原劑 組卷:34引用:2難度:0.7 -
3.利用原子結構及元素周期律表相關知識得到的以下結論中正確的是( )
A.第IA族元素鈁的兩種核素:221Fr比223Fr少2個質子 B.第三周期元素的原子半徑:r(P)<r(S)<r(Cl) C.第ⅦA族元素從上到下,單質與氫氣化合越來越難 D.堿性:NaOH<Mg(OH)2<Al(OH)3 組卷:83引用:2難度:0.5 -
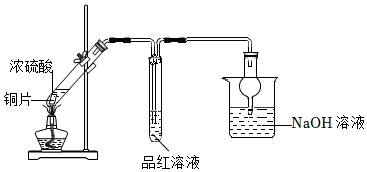 4.以下關于SO2的生成、檢驗、吸收的說法正確的是( )
4.以下關于SO2的生成、檢驗、吸收的說法正確的是( )A.利用反應Cu+2H2SO4 CuSO4+SO2↑+H2↑產生SO2△B.濃硫酸中S元素均從+6價降低為了+4價 C.SO2是酸性氧化物,因此可以用堿吸收 D.在此反應中,濃硫酸體現脫水性 組卷:199引用:2難度:0.7 -
5.下列變化與氧化還原反應無關的是( )
A.向CuSO4溶液中加入少量鋅粉,溶液藍色變淺 B.棕黃色FeCl3飽和溶液滴入沸水中變紅褐色 C.紫色酸性KMnO4溶液通入乙烯氣體后褪色 D.Na露置于空氣中逐漸變為暗灰色 組卷:6引用:1難度:0.5 -
6.以太陽能為熱源,熱化學硫碘循環分解水制氫方法中第一步反應的化學方程式是2H2O+SO2+I2═H2SO4+2HI,用NA表示阿伏加德羅常數的值,下列說法不正確的是( )
A.0.1molH2O中所含原子總數約為0.3NA B.25℃時,pH=1的H2SO4溶液中含有H+的數目約為0.1NA C.消耗1molSO2時,轉移的電子數為2NA D.產生2molHI時,消耗36gH2O 組卷:42引用:3難度:0.6
二、解答題(共5小題,滿分58分)
-
18.治療腎性貧血的藥物羅沙司他(J)的一種合成路線如圖(部分試劑及條件省略):
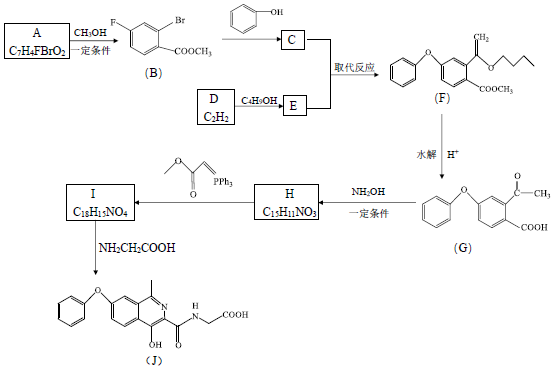
已知: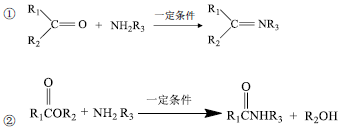
(1)A中的官能團有碳氟鍵、碳溴鍵和。
(2)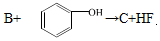 ,該反應的反應類型是 。
,該反應的反應類型是 。
(3)關于E的說法正確的是(填寫序號)。
a.核磁共振氫譜有6組峰
b.能使酸性高錳酸鉀溶液褪色
c.存在含2個環狀結構的醚類同分異構體
d.存在含一個醛基的同分異構體
(4)H分子中含有3個環狀結構,G→H的化學方程式是。
(5)由I轉化為J的過程中,另外一種產物是CH3OH,I的結構簡式是。
制備中間體I的另一種流程(部分)如圖: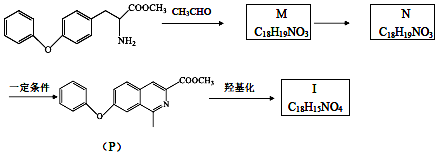
已知:M不穩定,會轉化為N,N分子中有3個環狀結構。
(6)M的結構簡式是。
(7)N轉化為P的同時還生成另外一種產物Q,則生成1molP的同時會生成molQ。組卷:33引用:1難度:0.4 -
19.鈦酸鋇具有優良的介電、壓電特性,主要用于電容器、自動溫控等領域。
(1)鈦元素在周期表中的位置;基態鈦原子的電子排布式為。
(2)鋇元素在自然界中主要以重晶石形式存在,其成分為BaSO4,其中所含三種元素的電負性從大到小的順序為(用元素符號表示);SO42-的空間構型為,其中S原子的雜化方式為。
(3)鹵化鈉(NaX)和四鹵化鈦(TiX4)的熔點如圖1所示,已知TiF4的晶體類型與TiCl4、TiBr4、TiI4不同,下列判斷不正確的是(選填字母序號)。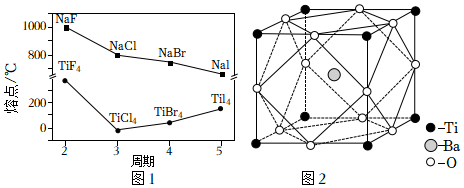
a.NaX均為離子晶體
b.隨X半徑的增大,NaX的離子鍵減弱,熔點逐漸降低
c.TiF4的熔點反常升高是由于氫鍵的作用
d.TiCl4、TiBr4、TiI4的相對分子質量依次增大,分子間作用力增大,熔點逐漸升高
(4)鈦酸鋇的晶胞結構如圖2所示,在該晶胞結構中,鈦離子、鋇離子、氧離子的個數比為;該物質的化學式為;晶體中每個鋇離子周圍與其距離最近且相等的氧離子的數量是;其晶胞參數約為apm,鈦酸鋇晶體的密度ρ=g?cm-3(設阿伏加德羅常數的值為NA,用含a、NA的代數式表示)組卷:73引用:3難度:0.7


