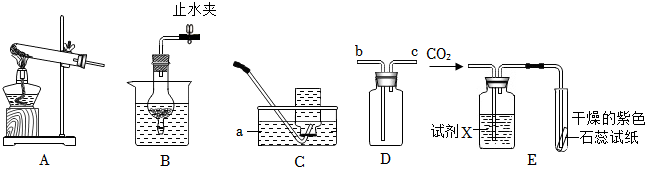
20.純堿是一種重要的化工原料,廣泛用于玻璃、造紙、紡織和洗滌劑的生產。某化學興趣小組對純堿的制備、性質及用途等開展項目式學習。
任務一:了解純堿的制備——“侯氏制堿法”
“侯氏制堿法”主要化學原理是利用飽和氯化鈉溶液吸收兩種氣體,生成碳酸氫鈉和氯化銨(NH4Cl),再加熱碳酸氫鈉即可制得純堿。
(1)純堿屬于
(填“酸”“堿”或“鹽”)。
(2)飽和氯化鈉溶液吸收的兩種氣體是
(填字母序號)。
A.Cl2
B.NH3
C.SO2
D.CO2
任務二:探究純堿的性質——Na2CO3溶液呈堿性
【查閱資料】
①溶液呈堿性,是因為溶液中存在較多的OH-。
②Na2CO3在水中全部解離出Na+和。
③CaCl2溶液呈中性,Ca2+、Cl-對溶液的酸堿性沒有影響。
【提出猜想】
(3)猜想一:H2O單獨起作用,產生較多的OH-,使溶液呈堿性。
猜想二:Na+與H2O作用,產生較多的OH-,使溶液呈堿性。
猜想三:
。
| 實驗操作 |
實驗現象 |
實驗結論 |
| (1)向試管中加入一定量的蒸餾水,滴入2滴酚酞溶液 |
溶液無明顯變化 |
猜想一不成立 |
| (2)向試管中加入一定量的NaCl溶液,滴入2滴酚酞溶液 |
溶液無明顯變化 |
猜想二不成立 |
(3)①向試管中加入一定量的Na2CO3溶液,滴入2滴酚酞溶液
②往①所得溶液中逐滴加入CaCl2溶液至過量 |
①溶液由無色變紅色
② |
猜想三成立 |
【實驗探究】
【解釋與結論】同學們和老師交流,得知
和H
2O作用,產生較多的OH
-和另一種陰離子。
【拓展與延伸】
(4)結合任務二的所有信息和結論,運用初中化學所學知識,經過分析推理可得出:Na
2CO
3溶液中含有的陰離子是
、
、
。
任務三:探究純堿的用途——用于生產洗滌劑
【查閱資料】Na
2CO
3可用于生產洗滌劑。Na
2CO
3溶液呈堿性,可清洗油污,溶液堿性越強,去油污效果越好。
【實驗探究】興趣小組繼續對影響Na
2CO
3溶液去油污效果的因素進行探究。
用不同溫度的水,配制溶質質量分數分別為2%、6%和10%的Na
2CO
3溶液,并測定溶液pH,記錄數據如下表:
| 實驗編號 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
| 溶質質量分數 |
2% |
2% |
2% |
6% |
6% |
6% |
10% |
10% |
10% |
| 溶液溫度(℃) |
20 |
40 |
60 |
20 |
50 |
60 |
20 |
40 |
70 |
| 溶液pH |
10.90 |
11.18 |
11.26 |
11.08 |
11.27 |
11.30 |
11.22 |
11.46 |
11.50 |
【解釋與結論】
(5)實驗①、②、③對比,可得出的結論是
。
(6)要證明Na
2CO
3溶液的溶質質量分數變化與pH變化關系,可選擇的3個實驗的編號是
。
【拓展與應用】
(7)下列物質可用于去油污的是
(填字母序號)。
A.NaCl
B.NaOH
C.K
2CO
3D.CaCO
3任務四:探究市售純堿樣品成分
市售純堿主要成分是碳酸鈉,還含少量氯化鈉等雜質。
已知:①部分銀鹽的溶解性如下表
②氯化銀不溶于稀硝酸。
驗證樣品中含有氯化鈉
實驗Ⅰ、取純堿樣品,加水溶解得溶液X,測得溶液pH約為12。
實驗Ⅱ、取溶液X,滴加過量試劑Y,產生能使澄清石灰水變渾濁的氣體。
實驗Ⅲ、向實驗Ⅱ后所得溶液中滴加硝酸銀溶液,有白色沉淀生成。
結論:樣品中含有氯化鈉。
(8)測定溶液pH的操作:用玻璃棒蘸取溶液滴在pH試紙上,與
相比較。
(9)實驗Ⅱ中所加的試劑Y應選用
(填字母)。
a.稀鹽酸
b.稀硝酸
c.氫氧化鈉溶液
d.氯化鈣溶液
任務四:測定樣品中碳酸鈉含量
準確稱取2g干燥純堿樣品,加水溶解,逐滴加入溶質質量分數為3.65%的稀鹽酸,邊滴加邊攪拌,當兩者恰好完全反應時(含碳物質全部轉化為CO
2),消耗鹽酸體積為37.00mL。(該鹽酸的密度近似等于1g/mL,雜質不與鹽酸反應)
(10)通過計算判斷該純堿樣品的等級
。(寫出計算過程)
無水碳酸鈉等級規定如下:
|
優等品 |
一等品 |
合格品 |
| 碳酸鈉質量分數 |
≥99.2% |
≥98.8% |
≥98.0% |
(11)實驗發現,當滴入鹽酸體積略少于37.00ml時,溶液pH就降至7以下,溶液pH小于7的原因是
。將此時的溶液煮沸,pH會略有升高,其原因
。