2020-2021學年天津市靜海一中高三(上)期末化學試卷
發布:2024/10/25 20:30:2
一、選擇題(共14小題,每小題3分,滿分42分)
-
1.化學與環境、工農業生產等密切相關,下列說法不正確的是( )
A.浸有酸性高錳酸鉀溶液的硅藻土可用于水果保鮮 B.NaCl不能使蛋白質變性,所以不能用作食品防腐劑 C.捕獲工業排放的CO2,可用來合成可降解塑料聚碳酸酯 D.在葡萄酒中添加微量SO2作抗氧化劑,可使酒保持良好品質 組卷:70引用:3難度:0.6 -
2.NA代表阿伏加德羅常數的值,下列敘述正確的是( )
A.1mol[Ag(NH3)2]+含有σ鍵數目為6NA B.1mol過氧化鈉含有陰離子的數目為0.2NA C.1mol羥基(-OH)所含的電子總數為9NA D.一定條件下,2mol SO2和1mol O2混合在密閉容器中充分反應后容器中的分子數為2NA 組卷:28引用:1難度:0.5 -
3.下列化學用語表述正確的是( )
A.核內質子數為117,核內中子數為174的核素Ts可表示為: TS174117B.乙醇的結構簡式:C2H6O C.COCl2 的結構式為: 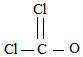
D.CaO2的電子式為: 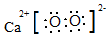 組卷:752引用:9難度:0.9
組卷:752引用:9難度:0.9 -
4.如圖所示的實驗方案,能達到實驗目的的是( )
A. 
如圖驗證FeCl3對H2O2分解反應有催化作用B. 
如圖用Cu和濃硝酸酸制取NOC. 
如圖除去CO2氣體中混有的HClD. 
如圖比較Cl、C和Si的非金屬性強弱組卷:18引用:2難度:0.5 -
5.下列有關敘述正確的是( )
A.常溫下,將0.1mol?L-1的醋酸溶液加水稀釋至原來體積的10倍,CH3COOH的電離平衡常數增大為原來的10倍 B.等濃度、等體積的鹽酸和醋酸,鹽酸中和氫氧化鈉的能力強 C.25℃時,NH3?H2O和CH3COOH的電離常數K相等,等溫等濃度的氨水和醋酸兩溶液加水稀釋到相同體積,溶液pH的變化值相同 D.向醋酸溶液中加入水, 不變(稀釋過程中溫度變化忽略不計)c(CH3COO-)c(CH3COOH)?c(OH-)組卷:58引用:1難度:0.7 -
6.利用圖中所示裝置及試劑,能達到相應實驗目的的是( )
選項 試劑甲 試劑乙 實驗目的 
A 飽和食鹽水 濃硫酸 從Cl2和SO2的混合氣體中分離出SO2 B NaOH溶液 濃硫酸 除去乙烷中的H2S C 溴水 濃硫酸 除去C2H4中的CH4 D NaOH溶液 濃硫酸 檢驗NO2中的NO A.A B.B C.C D.D 組卷:32引用:2難度:0.5
三、提高題(共2小題,滿分22分)
-
19.甲醇是重要的化工原料,又可作為燃料。利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,發生的主反應如下:
①CO(g)+2H2(g)?CH3OH(g)△H1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3
回答下列問題:
(1)已知反應①中的相關的化學鍵鍵能數據如下:(其中CO中的碳氧鍵為CO)←
由此計算△H1=化學鍵 H-H C-O C O←H-O C-H E/(kJ?mol-1) 436 343 1076 465 413 kJ?mol-1已知△H2=-58kJ?mol-1,由此計算,△H3=kJ?mol-1。
(2)圖1中能正確反映平衡常數K隨溫度變化關系的曲線為(填曲線標記字母),其判斷理由是。
(3)合成氣的組成=2.60時,體系中的CO平衡轉化率(α)與溫度和壓強的關系如圖2所示。α(CO)值隨溫度升高而n(H2)n(CO+CO2)(填“增大”或“減小”),其原因是。圖2中的壓強由大到小為,其判斷理由是。組卷:148引用:5難度:0.5 -
20.氨基甲酸銨是一種重要化工產品,常溫時為白色晶體或粉末,易溶于水,難溶于CCl4,59℃時分解為氨及二氧化碳,其制備原理:2NH3(g)+CO2(g)?NH2COONH4(s)△H=-272kJ?mol-1。某化學興趣小組利用如圖實驗裝置(部分固定裝置已省略)模擬制備NH2COONH4。試回答下列問題:

(1)儀器組裝完畢后,首先應進行的操作是。儀器b的名稱是。
(2)裝置A用于實驗室制取NH2COONH4的原料氣體之一,該反應的化學方程式為。
(3)裝置F中試劑的名稱為。
(4)為提高原料氣的利用率,應控制裝置C和E中最佳鼓泡速率比為,裝置D采用冰水浴的原因為。
(5)生成的氨基甲酸銨懸浮于CCl4中,下列操作可實現產品分離的是。(填字母)
(6)制得的氨基甲酸銨可能含有碳酸氫銨、碳酸銨中的一種或兩種雜質。
設計方案,進行成分探究,請填寫表中空格。
限選試劑:蒸餾水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀鹽酸。實驗步驟 預期現象和結論 步驟1:取少量固體樣品于試管中,加入蒸餾水至固體溶解。 得到無色溶液 步驟2:向試管中加入過量的BaCl2溶液,靜置 若溶液不變渾濁,證明固體中不含碳酸銨 步驟3:向試管中繼續加入 ,證明固體中含有碳酸氫銨組卷:18引用:1難度:0.5


