2022年江蘇省淮安市淮安區(qū)中考化學(xué)模擬試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(本題共10小題,每小題2分,共20分。每小題只有一個(gè)選項(xiàng)符合題意)
-
1.抗擊疫情,人人有責(zé)。下列防疫措施中一定發(fā)生化學(xué)變化的是( )
A.酒精消毒 B.測量體溫 C.清水洗手 D.佩戴口罩 組卷:56引用:42難度:0.8 -
2.下列實(shí)驗(yàn)操作不符合規(guī)范的是( )
A. 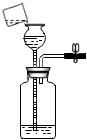
檢查氣密性B. 
過濾C. 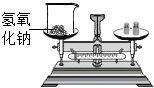
用托盤天平稱取固體NaOHD. 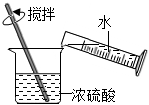
濃硫酸的稀釋組卷:5引用:1難度:0.7 -
3.央視“3?15”晚會(huì)曝光了多家食品加工企業(yè)“老壇酸菜”亂象。酸菜若未腌透,會(huì)富含亞硝酸鈉(化學(xué)式為NaNO2),食用后有損人體健康。亞硝酸鈉中氮元素的化合價(jià)為( )
A.-1 B.+1 C.+3 D.+5 組卷:62引用:2難度:0.5 -
4.“莊稼一枝花,全靠肥當(dāng)家”,下列屬于復(fù)合肥的是( )
A.KNO3 B.NH4HCO3 C.Ca3(PO4)2 D.K2SO4 組卷:136引用:5難度:0.9 -
5.下列對(duì)一些事實(shí)的解釋正確的是( )
A.鐵制品表面涂“銀粉”(鋁粉)防銹——鋁的化學(xué)性質(zhì)比鐵穩(wěn)定 B.用洗潔精清洗餐具上的油污——洗潔精能溶解油污 C.電解水產(chǎn)生氫氣和氧氣——水是由氫氣和氧氣組成的 D.6000L氧氣在150個(gè)大氣壓下裝入40L的鋼瓶——加壓后氧分子間空隙變小 組卷:29引用:2難度:0.7
二、非選擇題(本題共7小題,共40分)
-
16.某同學(xué)要探究燃燒的條件,進(jìn)行了如下實(shí)驗(yàn):
【實(shí)驗(yàn)】(已知:白磷的著火點(diǎn)為40℃)
(1)步驟1中所缺的操作名稱為實(shí)驗(yàn)裝置 實(shí)驗(yàn)步驟及現(xiàn)象 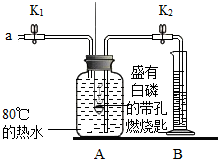
步驟1:連接裝置。
步驟2:將盛有白磷的帶孔燃燒匙伸入A瓶(空瓶)中,白磷不燃燒。
步驟3:向A瓶中加滿80℃熱水,塞緊瓶塞,白磷不燃燒。
步驟4:打開K1、K2,從a口向A瓶中鼓入空氣,待瓶中的液面低于燃燒匙底部時(shí),關(guān)閉K1、K2.此時(shí)進(jìn)入量筒B中水的體積為100mL,觀察到A瓶中的白磷燃燒。。
(2)寫出A中白磷燃燒的化學(xué)方程式:。
(3)對(duì)比步驟3和4的現(xiàn)象可知,可燃物燃燒的條件之一是。
(4)若把80℃的蒸餾水換成冷的蒸餾水,重復(fù)以上實(shí)驗(yàn)步驟進(jìn)行對(duì)比,該實(shí)驗(yàn)還能得出燃燒需要的條件是。
(5)待裝置冷卻至室溫,打開K2,如果觀察到量筒的水進(jìn)入A的體積明顯大于20mL,原因可能是。組卷:15引用:1難度:0.9 -
17.FeCO3能用于制備可溶性乳酸亞鐵補(bǔ)血?jiǎng)D郴瘜W(xué)興趣小組對(duì)其制備和性質(zhì)進(jìn)行了如下探究。
【查閱資料】
①溶液pH大于8.8時(shí),F(xiàn)e2+完全轉(zhuǎn)化為Fe(OH)2沉淀。
②FeCO3固體置于潮濕空氣中易變質(zhì)生成Fe(OH)3
③FeCl3溶液中滴加KSCN溶液,會(huì)出現(xiàn)血紅色絮狀物;而FeCl2溶液中滴加KSCN溶液,不會(huì)出現(xiàn)血紅色絮狀物。
④FeCO3是白色固體,難溶于水,能與酸發(fā)生復(fù)分解反應(yīng)反應(yīng)。
⑤堿石灰的主要成分是NaOH和CaO。
探究一:FeCO3的制備
(1)該興趣小組用pH=11.9的Na2CO3溶液和FeSO4溶液在燒杯中制備FeCO3時(shí),應(yīng)選用的加料方式是(填字母)。
A.將FeSO4溶液與Na2CO3溶液同時(shí)加入燒杯中
B.將FeSO4溶液緩慢加入盛有Na2CO3溶液的燒杯中
C.將Na2CO3溶液緩慢加入盛有FeSO4溶液的燒杯中
(2)制備FeCO3的化學(xué)方程式是。
探究二:FeCO3的性質(zhì)探究
【提出問題】久置于空氣中的FeCO3固體的成分是什么?
【猜想與假設(shè)】猜想1:FeCO3;猜想2:FeCO3和Fe(OH)3;猜想3:。
【定性探究】
【實(shí)驗(yàn)結(jié)論】久置于空氣中的FeCO3固體的成分是FeCO3和Fe(OH)3實(shí)驗(yàn)操作 實(shí)驗(yàn)現(xiàn)象 結(jié)論 取少量固體于試管中,加入足量的稀鹽酸 固體完全溶解,有氣泡產(chǎn)生 猜想 不成立取少量上述反應(yīng)后的溶液于試管中,滴加KSCN溶液 猜想2成立
【定量探究】該興趣小組為進(jìn)一步確定固體中FeCO3的質(zhì)量分?jǐn)?shù),稱取10.0g固體做了如圖所示的補(bǔ)充實(shí)驗(yàn)。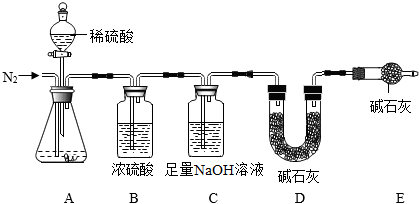
(3)A中涉及的中和反應(yīng)的化學(xué)反應(yīng)方程式為。
(4)裝置B的作用是。
(5)反應(yīng)結(jié)束后,繼續(xù)通入一段時(shí)間N2的目的是。
(6)如果去掉裝置E,會(huì)使實(shí)驗(yàn)結(jié)果填“偏大”、“偏小”或“不變”)。
(7)實(shí)驗(yàn)結(jié)束后,測得裝置C和D增重0.44g,則固體中FeCO3的質(zhì)量分?jǐn)?shù)。(寫出計(jì)算過程)組卷:36引用:1難度:0.5


