2015-2016學年浙江省紹興一中高三(上)第四次周考化學試卷
發布:2024/11/22 8:0:31
一、選擇題(本題共有17小題.在每小題給出的四個選項中,只有一個選項是符合題目要求的,選對得6分,選錯得0分)
-
1.下列說法正確的是( )
A.利用外接直流電源保護鐵質建筑物,屬于電化學中犧牲陽極的陰極保護法 B.科學儀器的使用利于我們認識物質的微觀世界,現在人們借助掃描隧道顯微鏡,應用SMT技術可以“看”到越來越細微的結構,并實現對原子或分子的操縱 C.人們通常用標準燃燒熱或熱值來衡量燃料燃燒放出熱量的大小,某物質的熱值越高則其標準燃燒熱越大 D.汽車尾氣催化轉化裝置可將尾氣中的NO和CO等有害氣體轉化為N2和CO2,該裝置中的催化劑可降低NO和CO反應的活化能,加快該反應的速率,同時能提高該反應的平衡轉化率 組卷:22引用:2難度:0.9 -
2.下列說法正確的是( )
A.除去硬脂酸鈉溶液中的甘油方法是:往溶液中加入飽和食鹽水,分液 B.向無水乙醇中加入濃H2SO4,加熱至170℃產生的氣體通入酸性KMnO4溶液,紅色褪去,證明生成的氣體全部是乙烯 C.潤洗酸式滴定管時應從滴定管上口加入3~5mL所要盛裝的酸溶液,傾斜著轉動滴定管,使液體潤濕其內壁,再從下口倒出,重復2~3次 D.取5mL 0.1mol?L-1KI溶液,滴加0.1mol?L-1FeCl3溶液5~6滴,繼續加入2mLCCl4,充分振蕩后靜置,取上層溶液加KSCN溶液,無明顯現象 組卷:285引用:3難度:0.5 -
3.X、Y、Z、R和W代表原子序數依次增大的5種短周期元素,X與Z、Y與W同主族,Y是地殼中含量最多的元素,W元素與X元素可以形成18電子的分子,R元素的簡單離子是同周期元素中半徑最小的,下列說法正確的是( )
A.R元素最高價氧化物所對應的水化物具有兩性,但不會溶于稀氨水 B.Y分別可與X和Z形成原子個數比為1:1的化合物,且形成的化合物晶體類型相同 C.Y的氫化物分子間存在氫鍵,因此Y的氫化物的穩定性大于W的氫化物的穩定性 D.原子半徑從小到大:X<Y<Z<R<W 組卷:25引用:5難度:0.9
二、解答題(共4小題,滿分58分)
-
10.乙醇汽油是被廣泛使用的新型清潔燃料,工業生產乙醇的一種反應原理為:
2CO(g)+4H2(g)?CH3CH2OH(g)+H2O(g)△H=-256.1kJ?mol-1.
已知:H2O(l)=H2O(g)△H=+44kJ?mol-1
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ?mol-1
(1)以CO2(g)與H2(g)為原料也可合成乙醇,其熱化學方程式如下:
2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(l)△H=.
(2)CH4和H2O(g)在催化劑表面發生反應CH4+H2O?CO+3H2,該反應在不同溫度下的化學平衡常數如下表:
①該反應是溫度/℃ 800 1000 1200 1400 平衡常數 0.45 1.92 276.5 1771.5 反應(填“吸熱”或“放熱”);
②T℃時,向1L密閉容器中投入1molCH4和1mol H2O(g),平衡時c(CH4)=0.5mol?L-1,該溫度下反應CH4+H2O?CO+3H2的平衡常數K=.
(3)汽車使用乙醇汽油并不能減少NOx的排放,這使NOx的有效消除成為環保領域的重要課題.某研究小組在實驗室以Ag-ZSM-5為催化劑,測得NO轉化為N2的轉化率隨溫度變化情況如下圖.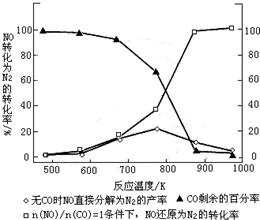
①若不使用CO,溫度超過775℃,發現NO的分解率降低,其可能的原因為;在=1的條件下,應控制的最佳溫度在n(NO)n(CO)左右.
②用CxHy(烴)催化還原NOx也可消除氮氧化物的污染.寫出CH4與NO2發生反應的化學方程式:.
(4)乙醇-空氣燃料電池中使用的電解質是攙雜了Y2O3的ZrO2晶體,它在高溫下能傳導O2-離子.該電池負極的電極反應式為.組卷:35引用:4難度:0.1 -
11.某學習小組按如下實驗流程探究海帶中碘含量的測定和碘的制取.
實驗(一) 碘含量的測定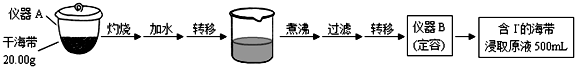
取0.0100mol?Lˉ1的AgNO3標準溶液裝入滴定管,取100.00mL海帶浸取原液至滴定池,用電勢滴定法測定碘含量.測得的電動勢(E)反映溶液中c(Iˉ)的變化,部分數據如下表:
實驗(二) 碘的制取V(AgNO3)/mL 15.00 19.00 19.80 19.98 20.00 20.02 21.00 23.00 25.00 E/mV -225 -200 -150 -100 50.0 175 275 300 325
另制海帶浸取原液,甲、乙兩種實驗方案如下: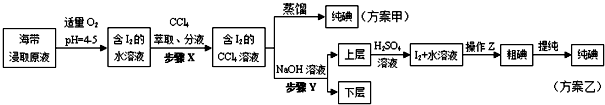
已知:3I2+6NaOH=5NaI+NaIO3+3H2O.
(1)實驗(一) 中的儀器名稱:儀器A,儀器B.
(2)①根據表中數據繪制滴定曲線: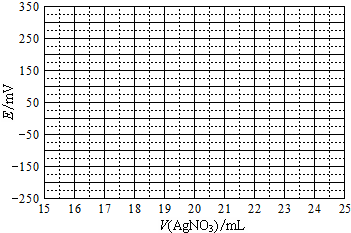
②該次滴定終點時用去AgNO3溶液的體積為mL,計算得海帶中碘的百分含量為%.(已知碘的相對原子質量為127)
(3)①分液漏斗使用前須檢漏,檢漏方法為.
②步驟X中,萃取后分液漏斗內觀察到的現象是.
③下列有關步驟Y的說法,正確的是.
A.應控制NaOH溶液的濃度和體積 B.將碘轉化呈離子進入水層
C.主要是除去海帶浸取原液中的有機雜質 D.NaOH溶液可以由乙醇代替
④實驗(二) 中操作Z的名稱是.
(4)方案甲中采用蒸餾不合理,理由是.組卷:69引用:2難度:0.3


