2017年江蘇省鎮(zhèn)江市丹徒區(qū)初中化學命制比賽試卷(七)
發(fā)布:2024/4/20 14:35:0
一、單項選擇題(本題包括15小題,每小題2分,共30分.每小題只有一個選項符合題意)
-
1.下列變化屬于物理變化的是( )
A.冰雪融化 B.糧食釀酒 C.工業(yè)煉鐵 D.火箭點火 組卷:35引用:19難度:0.9 -
2.下列物質屬于純凈物的是( )
A.鐵礦石 B.干冰 C.酸奶 D.海水 組卷:29引用:4難度:0.9 -
3.下列物質俗名與化學式相對應的是( )
A.純堿-NaOH B.食鹽-NaCl C.小蘇打-Na2CO3 D.雙氧水-H2O 組卷:16引用:3難度:0.9 -
4.下列做法正確的是( )
A.可用聚乙烯包裝食品 B.防治侏儒癥可補鈣 C.在食用豬血中添加甲醛溶液 D.在蒸饅頭時添加燒堿 組卷:4引用:1難度:0.6 -
5.下列物質歸類正確的是( )
選項 歸類 物質 A 常見合金 生鐵、金剛石、青銅 B 常見溶液 白酒、糖水、食鹽水 C 化石燃料 煤氣、石油、天然氣 D 常見干燥劑 濃硫酸、熟石灰、堿石灰 A.A B.B C.C D.D 組卷:10引用:1難度:0.7 -
6.實驗室配制氯化鈉溶液的操作中,錯誤的是( )
A. 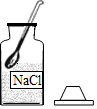
取氯化鈉B. 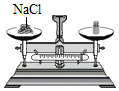
稱氯化鈉C. 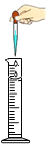
量取水D. 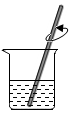
溶解組卷:170引用:67難度:0.7 -
7.下列實驗設計正確的是( )
A.用托盤天平稱取5.62g蔗糖 B.用活性炭使硬水轉化為軟水 C.用點燃的方法除去CO2中的CO D.加熱區(qū)分NaCl和NH4HCO3粉末 組卷:28引用:2難度:0.7 -
8.下列排列順序正確的是( )
A.硫元素的含量: 
B.金屬的活動性: 
C.溶液的pH: 
D.物質的溶解度:  組卷:28引用:3難度:0.7
組卷:28引用:3難度:0.7 -
9.下列對實驗現象的描述或實驗操作正確的是( )
A.打開盛放濃鹽酸的瓶蓋,產生大量白煙 B.向雞蛋清中滴加飽和硫酸銨溶液,析出白色固體 C.葡萄糖溶液中加新制氫氧化銅加熱煮沸,生成黑色沉淀 D.硫在空氣中燃燒,發(fā)出藍紫色火焰 組卷:30引用:3難度:0.7 -
10.甲和乙可以合成一種重要的化工原料,微觀過程如圖。下列說法錯誤的是( )
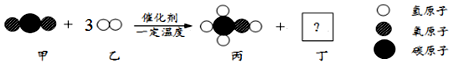
A.生成物丁屬于氧化物 B.丙中C、H、O的質量比為12:3:8 C.甲中碳元素的質量分數小于丙 D.該反應體現無機物可轉化為有機物 組卷:11引用:1難度:0.5
五、推斷題(本題包括2小題,共11分)
-
29.A和甲為礦石,A中主要成分含有兩種元素,元素質量之比為7:8,甲常用于建筑材料。B和E,D和F,丙和丁這三組物質都含有相同元素。B到F為硫酸型酸雨形成的一般過程。C為棕紅色固體粉末,M為常見金屬。
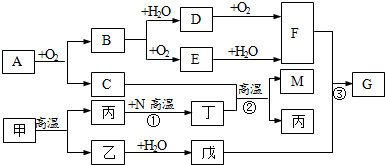
(1)寫出物質的化學式:A,D。
(2)寫出下列反應的化學方程式:
①,②。
(3)以上反應不涉及到的反應類型是反應。
(4)反應③體現了戊在農業(yè)生產中的一種用途:。組卷:74引用:4難度:0.3
六、綜合題(本題包括1小題,共14分)
-
30.堿式碳酸銅可用于生產木材防腐劑等。工業(yè)上常在含有硫酸銅的廢水中加入碳酸鈉溶液,得到堿式碳酸銅沉淀。
(1)產品生產中加入Na2CO3溶液時,實驗開始時出現藍色固體CuCO3,寫出開始時反應的化學方程式。反應液pH對產品中的含量以及反應液中Cu2+沉淀效率的影響如圖1所示,沉淀時溶液pH最好控制在SO2-4左右。
(2)實驗探究:Ⅰ.驗證堿式碳酸銅的分解產物,可選裝置如圖2所示。
甲同學將裝置按BCA的順序組合進行實驗,裝置A中盛放的試劑的作用是,裝置C中的現象為。裝置C、A順序不能顛倒的原因是。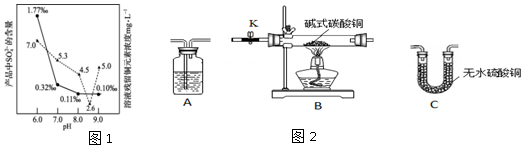
實驗結束,B裝置中粉末完全變黑。關于黑色物質的成分,有人認為可能有碳,請從物質的物理性質和元素守恒角度說明此猜想的依據是。
乙同學為確認該黑色粉末是氧化銅而不是碳粉,設計如下實驗,請完成下表:實驗步驟 觀察到的現象 獲得結論 反應的化學方程式 取少量黑色粉末于試管中,向其中加入足量的稀硫酸,振蕩 黑色粉末
均為氧化銅
Ⅱ.丙同學探究CO還原CuO所得固體產物的成分,實驗裝置如圖3:
資料:CO還原CuO的實驗過程中,固體產物可能有Cu2O(紅色固體)、Cu。反應前 反應后 玻璃管和內盛氧化銅
粉末的總質量為62.0g玻璃管和內盛紅色
粉末的總質量為61.7g玻璃管的質量為60.0g 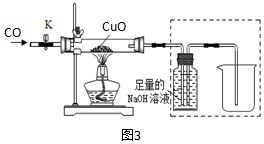
打開K,緩緩通入CO氣體,一段時間后加熱。當黑色固體全部變紅后停止加熱,繼續(xù)通入CO氣體直至玻璃管冷卻。
①由實驗數據計算可知,CuO中銅元素的質量為g,紅色固體粉末成分為。
②下列有關該實驗的說法正確的是。
A.先通入一會CO再加熱是為了排凈裝置中的空氣
B.實驗結束必須先將玻璃管與虛線框內的裝置分開,防止溶液倒吸
C.裝置圖中虛線框內的裝置既能吸收二氧化碳,又能收集一氧化碳
D.排入到燒杯中的溶液可能顯堿性,也可能顯中性
Ⅲ.工業(yè)上所制得的堿式碳酸銅種類較多,其組成表示為:xCuCO3?yCu(OH)2?zH2O。
資料:CuCO3、Cu(OH)2受熱時會分解得到相應的氧化物。
為測定某種產品的組成,丁同學設計的實驗方案中有如下步驟:①稱取12.0g的樣品;②高溫分解;③測出生成CO2的質量為2.2g;④測出生成水蒸氣的質量為1.8g。請根據相關實驗以及數據判斷:
(1)寫出生成CO2的化學方程式。
(2)反應后生成的CuO的質量為g。
(3)該堿式碳酸銅的化學式是。組卷:64引用:1難度:0.5


