2021-2022學年江蘇省無錫市江陰市南菁高級中學實驗學校九年級(下)月考化學試卷(3月份)
發(fā)布:2025/1/7 7:30:2
一、選擇題(本題包括20小題,每小題只有1個選項符合題意。1-10題每小題1分,11-20題每小題1分。共30分)
-
1.PM2.5是指大氣中直徑小于或等于2.5微米的顆粒物,下列事實與形成PM2.5無關(guān)的是( )
A.水力發(fā)電 B.風揚塵土 C.汽車尾氣 D.煤炭燃燒 組卷:81引用:1難度:0.7 -
2.下列變化屬于物理變化的是( )
A.燒制瓷器 B.火藥爆炸 C.糧食釀醋 D.玉石雕印 組卷:32引用:2難度:0.8 -
3.下列物質(zhì)屬于純凈物的是( )
A.礦泉水 B.石油 C.液氧 D.不銹鋼 組卷:47引用:1難度:0.7 -
4.下列物質(zhì)俗稱與化學式對應正確的是( )
A.水銀——Ag B.苛性鈉——NaOH C.小蘇打——Na2CO3 D.干冰——H2O 組卷:19引用:2難度:0.6 -
5.下列物質(zhì)由原子構(gòu)成的是( )
A.金剛石 B.氯化鈉 C.氫氣 D.水 組卷:26引用:6難度:0.6 -
6.下列化學用語表示正確的是( )
A.氦元素:HE B.3個氧原子:O3 C.1個鈣離子:Ca2+ D.高錳酸鉀:K2MnO4 組卷:43引用:4難度:0.5 -
7.下列實驗操作正確的是( )
A. 
蒸發(fā)食鹽水B. 
取液時擠入空氣C. 
收集氧氣D. 
測定溶液的pH組卷:4引用:1難度:0.7 -
8.氯是一種重要的“成鹽元素”,在自然界中以NaCl、CaCl2等形式大量存在。氯元素的原子結(jié)構(gòu)示意圖如圖所示。下列敘述錯誤的是( )
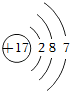
A.氯氣屬于非金屬單質(zhì) B.氯原子中核內(nèi)質(zhì)子數(shù)為17 C.氯元素在元素周期表中位于第3周期 D.氯原子在化學反應中易失電子 組卷:101引用:2難度:0.6 -
9.下列物質(zhì)的用途僅與其化學性質(zhì)有關(guān)的是( )
A.農(nóng)業(yè)上用氯化鈉溶液來選種 B.氮氣用作食品保護氣 C.大理石用于建筑材料 D.武德合金作保險絲 組卷:45引用:3難度:0.7
二、非選擇題(共50分)
-
27.關(guān)于酸的性質(zhì)是一項重要的課題。某小組以“探究硫酸的性質(zhì)”為主題開展項目式學習。

【任務(wù)一】濃硫酸稀釋過程中的能量變化。
圖1實驗中,觀察到用石蠟固定在銅片下的乒乓球脫落,此現(xiàn)象說明濃硫酸溶于水。
【任務(wù)二】溶液濃度對硫酸化學性質(zhì)的影響。
圖2實驗中,觀察到很快變黑的是濾紙(填“A”或“B”),由此可知,硫酸溶液的濃度不同,腐蝕性不同。
【任務(wù)三】稀硫酸的化學性質(zhì)。
小組同學按圖3進行實驗。
(1)試管2中可觀察到的現(xiàn)象是。
(2)該組同學利用數(shù)字化傳感器測得試管3中不斷滴加稀硫酸時pH的變化圖象如圖4所 示,二者恰好完全反應的微觀示意圖如圖5所示。
①圖5中a點所示溶液中含有的溶質(zhì)是。
②該反應的實質(zhì)是。
(3)小組同學對試管4反應后的物質(zhì)成分產(chǎn)生了興趣,繼續(xù)進行實驗。
【提出問題】試管4反應后的溶液中溶質(zhì)成分是什么?
【作出猜想】猜想一:可能是K2SO4
猜想二:可能是
猜想三:可能是K2SO4、H2SO4
【實驗與結(jié)論】
(4)某同學為驗證猜想三,用潔凈干燥的玻璃棒蘸取該反應后溶液滴到濕潤的pH試紙上,測得pH=4,她認為猜想三正確。對她的操作方法、測量結(jié)果及結(jié)論的評價,正確的是。
A.方法不正確,結(jié)果偏小,結(jié)論正確
B.方法正確,結(jié)果偏大,結(jié)論不正確
C.方法不正確,結(jié)果偏大,結(jié)論正確
D.方法正確,結(jié)果偏小,結(jié)論不正確
【任務(wù)四】廢液回收處理。
實驗結(jié)束后,在老師指導下同學們將四支試管中的液體倒入廢液缸,并對廢液缸中的固體物質(zhì)進行了回收。在檢驗廢液時發(fā)現(xiàn)硫酸過量,為防止其污染環(huán)境,從實驗成本的角度考慮,向該廢液中加入適量的(填一種具體物質(zhì)),處理后再排放。組卷:32引用:1難度:0.5 -
28.NaCl是一種重要的化工原料。

(1)粗鹽的提純:
①從“海水→粗鹽→精鹽”的過程中,不涉及到的實驗操作是。
a.過濾
b.蒸發(fā)
c.洗氣
d.溶解
②粗鹽中還含有Na2SO4、MgCl2、CaCl2等可溶性雜質(zhì)。為進一步除雜,向食鹽水中加入四種試劑除雜,有①稀鹽酸、②Na2CO3溶液、③NaOH溶液、④BaCl2溶液(均過量)(該四種試劑未排除雜順序),加入稍過量的Na2CO3溶液,除了能除盡粗鹽中的含有CaCl2外,它還有一個作用是(用化學方程式表示)。
(2)配制NaCl飽和溶液:
①20℃時,NaCl的溶解度為36.0g。配制20℃時50gNaCl的飽和溶液,需要NaCl的質(zhì)量為(計算結(jié)果保留一位小數(shù))。
②下列操作會導致配得的NaCl溶液溶質(zhì)質(zhì)量分數(shù)偏小的是(填序號)。
a.稱量氯化鈉時,砝碼放在左盤,并使用了游碼
b.用量筒量水時,仰視凹液面的最低處讀數(shù)
c.配好的溶液轉(zhuǎn)移至細口瓶時,有液體濺出
(3)工業(yè)上用電解飽和食鹽水的方法生產(chǎn)燒堿,其原理示意圖如圖2:
①寫出電解槽中發(fā)生反應的化學方程式:。
②氯堿工業(yè)生產(chǎn)的堿樣品中常含有Na2CO3和NaCl等雜質(zhì),用“離子交換膜法”生產(chǎn)的堿樣品質(zhì)量主要標準如表所示:
③檢驗堿樣品中是否含有Na2CO3,下列試劑中可選擇使用的是等級 氫氧化鈉含量 碳酸鈉含量 優(yōu)等品 ≥99.0% ≤0.5% 一等品 ≥98.5% ≤0.8% 合格品 ≥98.0% ≤1.0% (填序號)。
a.酚酞
b.稀鹽酸
c.澄清石灰水
④李老師設(shè)計和完成了如下實驗來判斷堿樣品的等級。
稱取20.3g堿樣品,加足量水溶解,再加入足量的氯化鋇溶液,充分反應后,過濾得到濾渣和濾液;將濾渣洗滌,干燥得到碳酸鋇(BaCO3)固體0.197g;向濾液中加入幾滴酚酞,再逐滴加入稀鹽酸至恰好完全反應,共消耗溶質(zhì)質(zhì)量分數(shù)為5%的稀鹽酸365g。則該堿樣品的等級是(不考慮其他雜質(zhì)參加反應)(寫出計算過程)。組卷:48引用:3難度:0.4


