2021-2022學年福建省福州市八縣(市、區)一中高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、單選題(每題3分,共45分)
-
1.2022年4月16日9時56分,搭載翟志剛、王亞平、葉光富3名航天員的神舟十三號載人飛船返回艙在東風著陸場成功著陸,三名航天員平安凱旋。神舟飛船使用了各種新材料,新技術與化學密切相關,下面有關說法正確的是( )
A.飛船中使用到的鋁合金熔、沸點比鋁高 B.飛船中使用的碳纖維是新型有機高分子材料 C.飛船使用的控制計算機、數據管理計算機的芯片材料是硅 D.飛船返回艙外表面使用的高溫結構陶瓷屬于有機高分子材料 組卷:14引用:2難度:0.7 -
2.化學在抗擊新冠肺炎疫情中發揮了巨大作用。下列說法錯誤的是( )
A.95%的酒精比75%的酒精消毒能力強 B.用于消毒的“84”消毒液屬于混合物 C.修建“火神山”醫院時所用的HDPE(高密度聚乙烯)膜是一種高分子材料 D.科研人員積極研發抗擊新冠病毒的疫苗,疫苗一般應冷藏存放,以避免蛋白質變性 組卷:25引用:2難度:0.8 -
3.下列表示不正確的是( )
A.乙醇的結構式: 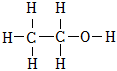
B.乙烯的分子結構模型: 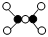
C.硫離子的結構示意圖: 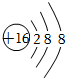
D.雙氧水的電子式: 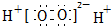 組卷:11引用:3難度:0.7
組卷:11引用:3難度:0.7 -
4.設NA為阿伏加德羅常數的值,下列敘述正確的是( )
A.標準狀況下,2.24L四氯化碳含碳原子數為0.1NA B.32gCu與足量濃硝酸反應,產物為NO2和NO,則反應中濃硝酸得到的電子數為NA C.一定條件下,將1molN2和3molH2混合后充分反應,生成NH3的分子數為2NA D.0.1molCH4與0.1molCl2混合充分光照,生成CH3Cl分子數為0.1NA 組卷:14引用:2難度:0.7 -
5.對于反應2SO2(g)+O2(g)?2SO3(g),保持其他條件不變,能使生成SO3的反應速率變小的是( )
A.壓縮容器體積 B.增加O2的濃度 C.恒容下充入Ne D.恒壓下充入Ne 組卷:41引用:4難度:0.6 -
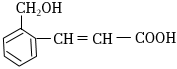 6.有機化合物可能發生的化學反應有( )
6.有機化合物可能發生的化學反應有( )
①加成 ②氧化 ③燃燒 ④加聚 ⑤取代.A.①②③ B.①③④ C.①②③④ D.①②③④⑤ 組卷:44引用:12難度:0.7
二.填空題(共5題,共55分)
-
19.有機物A~G之間有如圖1所示轉化關系。已知:A的產量用來衡量國家的石油化學工業的發展水平。
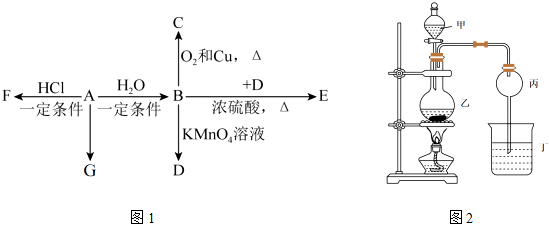
請回答下列問題:
(1)B、D的官能團的名稱是、。
(2)比賽中,當運動員肌肉挫傷或扭傷時,隨行醫生會對準受傷部位噴射物質F(沸點:12.27℃)進行應急處理。寫出由A制F的反應的化學方程式:。
(3)G是一種高分子化合物,可用于食品包裝材料,G的結構簡式為。
(4)①實驗室采用如圖2所示裝置制備E。E是一種具有香味的油狀液體,寫出反應B→E的化學反應方程式:。
②實驗結束后,取下盛有飽和Na2CO3溶液的燒杯,再沿該試管內壁緩緩加入1mL紫色石蕊試液(整個過程不振蕩試管),發現石蕊試液層存在于乙酸乙酯層與飽和Na2CO3溶液層之間。下列有關該實驗的分析正確的是。
A.乙酸乙酯的密度小于飽和Na2CO3溶液
B.石蕊試液層的顏色由上而下分別呈紅、紫、藍
C.石蕊試液層的顏色由上而下分別呈藍、紫、紅
(5)實驗中發現裝置乙中溶液逐漸變黑,某同學猜測產生這種現象的原因是。組卷:16引用:2難度:0.5 -
20.硫酸鋅(ZnSO4)是制備各種含鋅材料的原料,在防腐、電鍍、醫學上有諸多應用。硫酸鋅可由菱鋅礦制備,菱鋅礦的主要成分為ZnCO3,雜質為SiO2以及Ca、Mg、Fe、Cu等的化合物。其制備流程如圖:
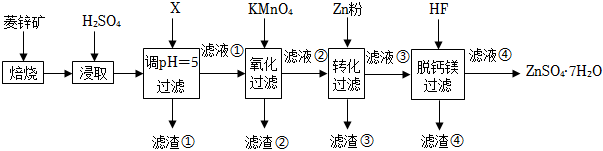
本題中所涉及金屬陽離子開始沉淀和完全沉淀的pH如表所示:
注意:CaF2和MgF2難溶于水和醇。金屬離子 Fe3+ Fe2+ Cu2+ Mg2+ Zn2+ 開始沉淀pH 2.10 7.45 5.4 9.60 6.41 完全沉淀pH 3.20 8.95 6.4 11.13 8.41
回答下列問題:
(1)菱鋅礦焙燒生成氧化鋅的化學方程式為。
(2)為了提高鋅的浸取速率,可采取的措施有、。
(3)加入Ca(OH)2 調溶液的pH=5,則濾渣①的主要成分是CaSO4、SiO2、。
(4)向80~90°C的濾液①中分批加入適量 KMnO4溶液充分反應后過濾,濾渣②中有MnO2,請配平該步反應的離子方程式為:Fe2+++MnO-4H2O═Fe(OH)3↓+MnO2↓+H+。
(5)濾液②中加入鋅粉的目的是。
(6)濾渣④與濃H2SO4反應可以釋放HF并循環利用,同時得到的副產物是CaSO4、。
(7)從“濾液④”中獲得浸提的方法是:蒸發濃縮、、過濾、洗滌。組卷:34引用:2難度:0.5


