魯科版(2019)必修第二冊《2.3.1 化學反應的快慢 》2020年同步練習卷(2)
發布:2024/4/20 14:35:0
一.選擇題:本題共10小題,每題2分,共20分。每小題只有一個選項符合題意。
-
1.在溫度不變的條件下,恒定的容器中進行下列反應:N2O4?2NO2,若N2O4的濃度由0.1mol/L降到0.07mol/L要用10s,那么N2O4的濃度從0.07mol/L降到0.04mol/L時,所用時間( )
A.等于10s B.等于5 s C.大于10 s D.小于10 s 組卷:59引用:7難度:0.9 -
2.下列關于化學反應速率的說法正確的是( )
A.化學反應速率是指一定時間內任何一種反應物濃度的減小或任何一種生成物濃度的增加 B.化學反應速率為“0.8 mol?L-1?s-1”所表示的意思是:時間為1 s時,某物質的濃度為0.8 mol?L-1 C.根據化學反應速率的大小可以知道化學反應進行的快慢 D.對于任何化學反應來說,反應現象越明顯,反應速率越大 組卷:43引用:3難度:0.7 -
3.硫代硫酸鈉溶液與稀硫酸反應的化學方程式為:Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O
下列各組實驗中最先出現渾濁的是( )實驗 反應溫度/℃ Na2S2O3溶液 稀H2SO4 H2O V/mL c(mol?L-1)V/mL c(mol?L-1)V/mL A 25 5 0.1 10 0.1 5 B 25 5 0.2 5 0.2 10 C 35 5 0.1 10 0.1 5 D 35 5 0.2 5 0.2 10 A.A B.B C.C D.D 組卷:507引用:21難度:0.9 -
4.已知Na2S2O3與H2SO4發生反應:Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O,在相同溫度下,下列化學反應速率最慢的是( )
A.10mL 0.1mol/L Na2S2O3溶液和10mL 0.1mol/LH2SO4溶液 B.5mL 0.1mol/L Na2S2O3溶液和5mL 0.1mol/LH2SO4溶液 C.5mL 0.1mol/L Na2S2O3溶液和5mL 0.05mol/LH2SO4溶液 D.10mL 0.5mol/L Na2S2O3溶液和10mL 0.05mol/LH2SO4溶液 組卷:30引用:1難度:0.9 -
5.在2L的密閉容器中,發生反應3A(g)+B(g)?2Z(g),若最初加入的A和B都是4mol,測得10s內A的平均反應速率υ(A)=0.15mol/(L?s),則反應進行到10s時容器中B的物質的量是( )
A.3mol B.2.4mol C.2.2mol D.3.2mol/L 組卷:63引用:7難度:0.9 -
6.在2A(g)+B(g)?3C(g)+4D(g)反應中,表示該反應速率最快的是( )
A.v(A)=0.5 mol?L-1?s-1 B.v(B)=0.5 mol?L-1?s-1 C.v(C)=1.8 mol?L-1?min-1 D.v(D)=1 mol?L-1?s-1 組卷:55引用:108難度:0.9
三.非選擇題:本題共5小題,共60分
-
19.某學生為了探究鋅與鹽酸反應過程中的速率變化,他在100mL稀鹽酸中加入足量的鋅粉,用排水集氣法收集反應放出的氫氣,實驗記錄如表(累計值):
(1)哪一時間段(指0~1、1~2、2~3、3~4、4~5min)反應速率最大時間(min) 1 2 3 4 5 氫氣體積(mL) 50 120 232 290 310 ,原因是;哪一段時段的反應速率最小,原因是.
(2)如果反應太激烈,為了減緩反應速率而又不減少產生氫氣的量,他在鹽酸中分別加入等體積的下列溶液:A 蒸餾水、B NaCl溶液、C NaNO3溶液、D CuSO4溶液、E Na2CO3溶液,你認為可行的是.組卷:66引用:6難度:0.5 -
 20.某化學小組為了研究外界條件對化學反應速率的影響,進行了如下實驗:
20.某化學小組為了研究外界條件對化學反應速率的影響,進行了如下實驗:
【實驗原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【實驗內容及記錄】
請回答:實驗編號 室溫下,試管中所加試劑及其用量/mL 室溫下溶液顏色褪至無色所需時間/min 0.6 mol/L
H2C2O4溶液H2O 0.2 mol/L KMnO4溶液 3 mol/L
稀硫酸1 3.0 2.0 3.0 2.0 4.0 2 3.0 3.0 2.0 2.0 5.2 3 3.0 4.0 1.0 2.0 6.4
(1)根據上表中的實驗數據,可以得到的結論是.
(2)利用實驗1中數據計算,用KMnO4的濃度變化表示的反應速率為:υ(KMnO4)=.
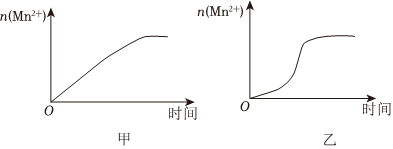
(3)該小組同學根據經驗繪制了n(Mn2+) 隨時間變化趨勢的示意圖,如圖1所示.但有同學查閱已有的實驗資料發現,該實驗過程中n(Mn2+) 隨時間變化的趨勢應如圖2所示.該小組同學根據圖2所示信息提出了新的假設,并繼續進行實驗探究.
①該小組同學提出的假設是.
②請你幫助該小組同學完成實驗方案,并填寫表中空白.
③若該小組同學提出的假設成立,應觀察到的現象是實驗編號 室溫下,試管中所加試劑及其用量/mL 再向試管中加入少量固體 室溫下溶液顏色褪至無色所需時間/min 0.6 mol/L
H2C2O4溶液H2O 0.2 mol/L KMnO4溶液 3 mol/L
稀硫酸4 3.0 2.0 3.0 2.0 t .組卷:68引用:20難度:0.1


