2017-2018學年北京三中高二(上)期中化學試卷(理)
發布:2024/4/20 14:35:0
一.第一部分(選擇題共50分)每小題只有一個正確答案:1-10題每小題1分,11-30題,每小題1分
-
1.下列設備工作時,將化學能轉化為熱能的是( )
A B C D 



硅太陽能電池 鋰離子電池 太陽能集熱器 燃氣灶 A.A B.B C.C D.D 組卷:900引用:106難度:0.9 -
2.下列物質屬于弱電解質的是( )
A.BaSO4 B.CO2 C.NH3?H2O D.Cl2 組卷:1引用:1難度:0.8 -
3.決定化學反應速率的根本因素是( )
A.溫度和壓強 B.反應物的濃度 C.參加反應的各物質的性質 D.催化劑 組卷:1引用:2難度:0.7 -
4.下列措施中,不能加快化學反應速率的是( )
A.將食物儲存在冰箱里 B.往H2O2溶液中加入幾滴FeCl3溶液 C.用粉末狀碳酸鈣代替塊狀碳酸鈣與稀鹽酸反應 D.用稀H2SO4溶液與鋅粒反應時加入幾滴CuSO4溶液 組卷:52引用:6難度:0.9 -
5.下列反應中生成物總能量高于反應物總能量的是( )
A.鋁粉與氧化鐵粉末反應 B.乙醇燃燒 C.碳酸鈣受熱分解 D.氧化鈣溶于水 組卷:39引用:179難度:0.9 -
6.在不同情況下測得A(g)+3B(g)?2C(g)+2D(g)的下列反應速率,其中反應速率最大的是( )
A.v(D)=0.4mol?L-1?s-1 B.v(C)=0.5mol?L-1?s-1 C.v(B)=0.6mol?L-1?s-1 D.v(A)=0.15mol?L-1?s-1 組卷:35引用:5難度:0.9 -
7.250℃和1.01×105Pa時,該反應能自發進行:2N2O5(g)=4NO2(g)+O2(g)△H=+56.76kJ/mol,其自發進行的原因是( )
A.是吸熱反應 B.是放熱反應 C.是熵減少的反應 D.熵增效應大于能量效應 組卷:2引用:1難度:0.7 -
8.未來新能源的特點是資源豐富,在使用時對環境無污染或污染很小,且有些可以再生.下列屬于最有希望的新能源的是( )
①天然氣 ②煤 ③核能 ④太陽能 ⑤生物質能 ⑥風能 ⑦氫能.A.①②③④ B.②⑤⑥⑦ C.①③④⑤⑥ D.除①②外 組卷:27引用:2難度:0.9 -
9.下列電離方程式書寫正確的是( )
A.CH3COOH═H++CH3COO- B.K2SO4═2K++ SO2-4C.H2CO3?2H++ CO2-3D.Na2CO3?2Na++ CO2-3組卷:11引用:2難度:0.9 -
10.下列溶液導電性最強的是( )
A.1L0.1mol/L醋酸 B.0.1L1mol/L H2SO4溶液 C.0.5L0.1mol/L鹽酸 D.2L0.1mol/L H2SO3溶液 組卷:3引用:1難度:0.5 -
 11.某同學按照課本實驗要求,用50mL 0.50mol/L的鹽酸與50mL 0.55mol/L的NaOH 溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量計算中和熱。下列說法中,正確的是( )
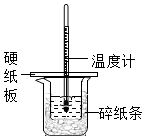
11.某同學按照課本實驗要求,用50mL 0.50mol/L的鹽酸與50mL 0.55mol/L的NaOH 溶液在如圖所示的裝置中進行中和反應。通過測定反應過程中所放出的熱量計算中和熱。下列說法中,正確的是( )A.實驗過程中沒有熱量損失 B.圖中實驗裝置缺少環形玻璃攪拌棒 C.燒杯間填滿碎紙條的作用是固定小燒杯 D.若將鹽酸體積改為60 mL,理論上所求中和熱不相等 組卷:302引用:25難度:0.7
二.第二部分(非選擇題共50分)
-
34.在酸性溶液中,碘酸鉀(KIO3)和Na2SO3可發生如下反應:2IO3-+5SO32-+2H+=═I2+5SO42-+H2O,生成的碘可以用淀粉溶液檢驗,根據溶液出現藍色所需的時間來衡量該反應的速率.某學生設計實驗如下表所示:
(1)該反應的氧化劑是0.01mol/L KIO3溶液的體積/mL Na2SO3溶液的體積/mL H2O的體積/mL 實驗溫度/℃ 溶液出現藍色所需的時間 實驗1 5 5 V1 0 a 實驗2 5 5 40 25 b 實驗3 5 V2 35 25 c ,若生成1mol I2,轉移電子的物質的量是.
(2)V1=mL,V2=mL.
(3)如果研究濃度對反應速率的影響,使用實驗和實驗.
(4)對比實驗1和實驗2,可以研究對化學反應速率的影響.
(5)溶液出現藍色所需的時間從多到少的順序是(用a、b、c表示).組卷:114引用:3難度:0.3 -
35.(1)鉻酸根
呈黃色,重鉻酸根Cr2CrO2-4呈橙色.在水溶液中,鉻酸根離子和重鉻酸根離子存在下列平衡:Cr2O2-7+H2O?2O2-7+2H+.把重鉻酸鉀溶于水配成稀溶液呈橙色.向上述溶液中加入幾滴濃硫酸,溶液橙色CrO2-4(填“變深”、“變淺”或“不變”),因為.
(2)已知2NO2(g)?N2O4 (g)△H=-56.9kJ?mol-1,將NO2球浸泡在冰水中,氣體的顏色將會(填“變深”、“變淺”或“不變”),原因是.
(3)在燒杯里混合10mL 0.01mol/L FeCl3溶液和10ml 0.01mol/L KSCN溶液,溶液立即變紅.已知反應:Fe3++3SCN-?Fe(SCN)3
①再向溶液中滴入1mol/LFeCl3溶液,現象(變深、不變、變淺),平衡向(正、逆)反應方向移動.
②在燒杯中加入KCl固體,顏色(變深、不變、變淺),平衡移動.組卷:13引用:2難度:0.3


