2022-2023學年重慶市渝高中學高一(下)期中化學試卷
發布:2024/4/20 14:35:0
選擇題
-
1.下列有關物質組成、性質和用途的說法中,正確的是( )
A.合金的熔點一般比組成合金的各成分金屬的高 B.氮化硅、光導纖維、氧化鋁陶瓷等屬于新型無機非金屬材料 C.水泥、玻璃和水晶都是硅酸鹽產品 D.光導纖維的主要成分是硅,可廣泛用于通信和醫療領域 組卷:23引用:3難度:0.5 -
2.下列反應屬于吸熱反應的是( )
A.木炭燃燒 B.CaCO3受熱分解 C.Na與水反應 D.鹽酸與NaOH溶液反應 組卷:21引用:5難度:0.7 -
3.某公司研發出了一種新型除草劑,其結構如圖所示,其中X、Y、Z、W、M是原子序數依次增大的短周期主族元素,M與Z同主族,W是地殼中含量最多的元素。下列敘述錯誤的是( )
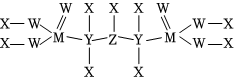
A.簡單原子半徑:M>Z>W B.氧化物對應水化物的酸性:Z強于M C.X與Y組成的最簡單化合物的穩定性小于Z與X組成的化合物的穩定性 D.X、Z、W三種元素既可組成共價化合物又可組成離子化合物 組卷:18引用:1難度:0.7 -
4.下列平衡建立判斷依據中,敘述不正確的項有( )
A.2HI(g)?H2(g)+I2(g),若1molH-H鍵斷裂的同時有2molH-I鍵斷裂,則平衡建立 B.3Z(s)?X(g)+2Y(g)加入Z后,若氣體平均摩爾質量不變,則平衡建立 C.N2(g)+3H2(g)?2NH3(g),若恒容條件下裝置壓強不變,則平衡建立 D.C(s)+H2O(g)?CO(g)+H2(g),若恒容條件下氣體密度不變,則平衡建立 組卷:96引用:3難度:0.5 -
 5.現用傳感技術測定噴泉實驗中的壓強變化來認識噴泉實驗的原理,下列說法錯誤的是( )
5.現用傳感技術測定噴泉實驗中的壓強變化來認識噴泉實驗的原理,下列說法錯誤的是( )A.制取氨氣時燒瓶中的固體常用CaO或NaOH B.將濕潤的紅色石蕊試紙置于三頸瓶口,試紙變藍,說明NH3已經集滿 C.關閉a,將單孔塞(插有吸入水的膠頭滴管)塞緊頸口c,打開b,完成噴泉實驗,電腦繪制三頸瓶內壓強變化曲線如圖2,則D點時噴泉最劇烈 D.實驗后,可用稀鹽酸處理多余的氨氣 組卷:168引用:7難度:0.5 -
6.下列說法正確的是( )
A.在食品袋中放入盛有硅膠和鐵粉的透氣小袋,可防止食物受潮、氧化變質 B.工業上用鐵制容器盛裝濃硫酸是因為常溫下鐵與濃硫酸不反應 C.向膽礬晶體滴加濃硫酸,晶體由藍色變為白色,此過程濃硫酸表現脫水性 D.常溫下,0.56g鐵片與足量濃硝酸反應轉移的電子數目為0.03NA 組卷:19引用:1難度:0.8
解答題
-
17.Ⅰ.氮及其化合物在生產生活中應用廣泛,工業上制硝酸的關鍵一步便是NH3的催化氧化,可用如圖裝置模擬NH3的催化氧化,回答下列問題:

(1)寫出玻璃管中發生反應的化學方程式。
(2)停止加熱后玻璃管內仍能保持紅熱,該反應是反應(填“吸熱”或“放熱”),為保證在裝置2中觀察到紅棕色氣體,裝置1應裝入,作用是。
Ⅱ.氮元素在海洋中的循環,是整個海洋生態系統的基礎和關鍵,海洋中無機氮的循環過程可用如圖表示。
(3)海洋中的氮循環起始于氮的固定,其中屬于固氮作用的一步是(填圖中數字序號)。
(4)下列關于海洋氮循環的說法正確的是。
a.海洋中的氮循環起始于氮的氧化
b.向海洋排放含的廢水會影響海洋中NO-3的含量NH+4
c.海洋中存在游離態的氮
d.海洋中的反硝化作用一定有氧氣的參與
(5)有氧時,在硝化細菌作用下,可實現過程④的轉化,寫出④的離子方程式并用單線橋標電子轉移情況NH+4。組卷:12引用:1難度:0.5 -
18.硫氰化鉀(KSCN)是一種用途廣泛的化學藥品,常用于合成樹脂、殺蟲殺菌劑等。某實驗小組用如圖所示的裝置制備硫氧化鉀。

已知:NH3不溶于CS2,CS2不溶于水且密度比水大。
Ⅰ.制備NH4SCN溶液
(1)組裝儀器后應先進行的操作是,a裝置為實驗室制氨氣的裝置,所發生反應的化學方程式為。
(2)三頸燒瓶內盛放有CS2、水和固體催化劑,發生反應CS2+3NH3HS。實驗開始時,打開K1,水浴加熱裝置d,反應發生,判斷CS2已反應完全的依據是催化劑。
Ⅱ.制備KSCN溶液
(3)關閉K1,將三頸燒瓶繼續加熱至100℃,待NH4HS完全分解后、再打開K2,繼續保持水浴溫度為100℃,緩慢滴入稍過量的KOH溶液,制得KSCN溶液。e中用H2SO4酸化的CuSO4吸收尾氣時可以看到有黑色的沉淀生成,則生成黑色沉淀的離子方程式為。
(4)下列說法正確的是(填字母)。
A.通過觀察c中的氣泡流速,控制a中產生氨氣的速率
B.裝置b可以填充P2O5
C.三頸燒瓶中長導氣管可以不插入到CS2中
D.d中橡皮管的作用是平衡氣壓,使KOH溶液能順利滴下
Ⅲ.制備KSCN晶體
(5)先通過過濾除去三頸燒瓶中的固體催化劑,再通過蒸發濃縮、冷卻結晶、過濾、洗滌、干燥,得到硫氰化鉀晶體。
(6)測定產品中KSCN的含量:稱取1.00g實驗產品,用蒸餾水溶解后,定容于100mL容量瓶中,移取25.00mL用0.1000mol/LAgNO3溶液反應,消耗AgNO3溶液的體積為24.00mL。反應時發生的離子反應為:SCN-+Ag+=AgSCN↓(白色),則產品中KSCN的質量分數為(計算結果保留三位有效數字)。組卷:15引用:1難度:0.6


