魯科版(2019)選擇性必修1《1.4 金屬的腐蝕與防護》2023年同步練習卷(8)
發布:2024/8/17 9:0:1
一、選擇題
-
 1.在一塊表面無銹的鐵片上滴食鹽水,放置一段時間后看到鐵片上有鐵銹出現,鐵片腐蝕過程中發生的總化學方程式:2Fe+2H2O+O2═2Fe(OH)2,Fe(OH)2進一步被氧氣氧化為Fe(OH)3,再在一定條件下脫水生成鐵銹,其原理如圖,下列說法正確的是( )
1.在一塊表面無銹的鐵片上滴食鹽水,放置一段時間后看到鐵片上有鐵銹出現,鐵片腐蝕過程中發生的總化學方程式:2Fe+2H2O+O2═2Fe(OH)2,Fe(OH)2進一步被氧氣氧化為Fe(OH)3,再在一定條件下脫水生成鐵銹,其原理如圖,下列說法正確的是( )A.鐵片發生還原反應而被腐蝕 B.鐵片腐蝕最嚴重區域應該是生銹最多的區域 C.鐵片腐蝕中負極發生的電極反應:2H2O+O2+4e-═4OH- D.鐵片里的鐵和碳與食鹽水形成無數微小原電池,發生了電化學腐蝕 組卷:303引用:9難度:0.5 -
2.相同材質的鐵在圖中的四種情況下最不易被腐蝕的是( )
A. 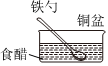
B. 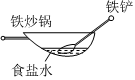
C. 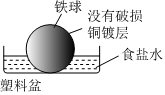
D. 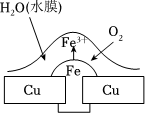 組卷:47引用:9難度:0.7
組卷:47引用:9難度:0.7 -
3.在日常生活中,我們經常看到鐵制品生銹、鋁制品表面出現白斑等眾多的金屬腐蝕現象.可以通過下列裝置所示實驗進行探究.下列說法正確的是( )

A.按圖Ⅰ裝置實驗,為了更快更清晰地觀察到液柱上升,可采用下列方法:用酒精燈加熱具支試管 B.圖Ⅱ是圖Ⅰ所示裝置的原理示意圖,圖Ⅱ的正極材料是鐵 C.鋁制品表面出現白斑可以通過圖Ⅲ裝置進行探究,Cl-由活性炭區向鋁箔表面區遷移,并發生電極反應:2Cl--2e-═Cl2↑ D.圖Ⅲ裝置的總反應為4Al+3O2+6H2O═4Al(OH)3,生成的Al(OH)3進一步脫水形成白斑 組卷:434引用:16難度:0.9 -
4.港珠澳大橋設計壽命為120年,對橋體鋼制構件采用了多種防腐措施,下列防腐措施錯誤的是( )
A.用導線與石墨相連 B.用導線與電源負極相連 C.鋼制構件上焊接鋅塊 D.表面噴涂分子涂層 組卷:54引用:3難度:0.8 -
5.在城市中地下常埋有許多金屬管道和輸電線路,地面上還鋪有鐵軌,當有電流泄漏入潮濕的土壤中,并與金屬管道或鐵軌形成回路時,下列有關說法錯誤的是( )
A.會引起金屬管道或鐵軌腐蝕 B.該過程金屬管道或鐵軌只發生了吸氧腐蝕 C.應將埋在地下的金屬管道或鐵軌涂上絕緣膜防止被腐蝕 D.為防止金屬管道或鐵軌腐蝕,可以將它們與直流電源的負極相連 組卷:41引用:2難度:0.7
三、解答題
-
15.某課外小組同學對不同條件下鐵釘的銹蝕進行了實驗.
一周后觀察:實驗序號 ① ② ③ ④ 實驗
內容



(1)鐵釘被腐蝕程度最大的是(填實驗序號).
(2)實驗③中主要發生的是(填“化學腐蝕”或“電化學腐蝕”).
(3)鐵發生電化學腐蝕的負極反應式為:.
(4)根據上述實驗,你認為鐵發生電化學腐蝕的條件是.
(5)據資料顯示,全世界每年因腐蝕而報廢的金屬材料相當于其年產量的20%以上.為防護金屬被腐蝕可采取的措施有(填序號).
①健身器材刷油漆 ②自行車鋼圈鍍鉻
③將鋼管用導線與鎂條連接 ④將鋼管用導線與碳棒連接.組卷:41引用:5難度:0.3 -
16.我國提出爭取在2030年前實現碳達峰,2060年前實現碳中和,這對于改善環境、實現綠色發展至關重要。因此,研發CO2利用技術,降低空氣中CO2含量成為研究熱點。
(1)科學家發明了一種新型Zn-CO2水介電池。電池示意圖如圖1所示,電極為金屬鋅和選擇性催化材料。放電時,CO2被轉化為儲氫物質甲酸等。
①放電時,Zn電極上發生(填“氧化”或“還原”)反應。
②充電時,陽極上發生的電極反應為。
(2)研究證實,在酸性水溶液中可以通過電解CO2生成甲醇,生成甲醇的電極反應式為,電路中每轉移0.3mol電子,消耗CO2的體積為L(已換算成標準狀況)。
(3)CH4和CO2都是比較穩定的分子,科學家利用電化學裝置實現兩種分子的耦合轉化,其原理如圖2所示。
①M為電源的(填“正極”或“負極”)。
②若生成的乙烯和乙烷的物質的量分別為3mol、2mol,則裝置中轉移的電子數為。組卷:15引用:4難度:0.7


