2020-2021學年江西省宜春市上高二中高一(下)第四次月考化學試卷(4月份)
發布:2024/4/20 14:35:0
一、選擇題(本題共16小題,每小題3分,共48分。每小題只有一個選項符合題意)
-
1.化學與能源開發、環境保護、資源利用等密切相關,下列說法正確的是( )
A.天然氣、石油、流水、風力、氫氣為一次能源 B.垃圾是放錯地方的資源,應分類回收利用 C.PM2.5含有的鉛、鎘、鉻、釩、砷等對人體有害的元素均是金屬元素 D.無論是風力發電還是火力發電,都是將化學能轉化為電能 組卷:8引用:1難度:0.5 -
2.下列有關化學用語使用正確的是( )
A.純堿的電離方程式:NaHCO3=Na++HCO3- B.氯離子的結構示意圖: 
C.H2S的結構式:H-S-H D.過氧化氫的電子式:  組卷:1引用:1難度:0.7
組卷:1引用:1難度:0.7 -
3.設NA為阿伏加德羅常數的數值,下列說法正確的是( )
A.1mol/L的NaCl溶液中含有的離子總數為2NA B.1 mol Na2O2與CO2完全反應時轉移電子數為2NA C.標準狀況下,22.4LH2O含有的 H-O鍵數為2NA D.18g 18O2中含有的中子數為10NA 組卷:7引用:4難度:0.7 -
4.最新報道:科學家首次用X射線激光技術觀察到CO與O在催化劑表面形成化學鍵的過程。反應過程的示意圖如下:
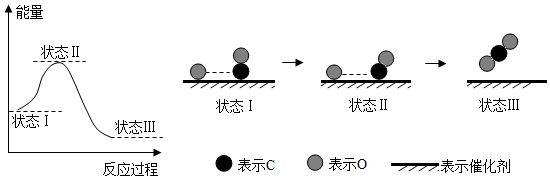
下列說法正確的是( )A.CO和O生成CO2是吸熱反應 B.在該過程中,CO斷鍵形成C和O C.CO和O生成了具有極性共價鍵的CO2 D.狀態Ⅰ→狀態Ⅲ表示CO與O2反應的過程 組卷:946引用:78難度:0.9 -
5.下列說法中正確的個數是( )
①化學反應的本質是有舊鍵的斷裂和新建的形成
②共價化合物均是非電解質
③金屬單質在反應中失去電子數越多,其還原性越強
④金屬單質只有還原性,非金屬單質只有氧化性
⑤化學鍵可以使離子相結合也可以使原子相結合
⑥化學鍵包括離子鍵、共價鍵、氫鍵
⑦同主族元素的單質熔沸點從上到下逐漸升高
⑧液態氯化氫能導電,所以氯化氫是電解質A.1個 B.2個 C.3個 D.4個 組卷:2引用:1難度:0.6 -
6.根據元素周期表和元素周期律判斷,下列關于短周期主族元素的說法一定正確的是( )
A.X元素的簡單陽離子與Y 元素的簡單陰離子具有相同的電子層結構,則兩元素的最高化合價:X<Y B.原子半徑最大和最小的元素都在第ⅠA族,且可形成離子化合物 C.根據同主族兩非金屬元素氫化物的沸點高低,可判斷兩元素非金屬性強弱 D.非金屬元素單質的氧化性越強,其氧化物對應水化物的酸性就越強 組卷:10引用:3難度:0.6 -
7.下列各分子中,所有原子都滿足最外層為8電子結構的是( )
A.BeCl2 B.H2S C.PCl5 D.NF3 組卷:12引用:1難度:0.6
二、填空題(本題共5小題,共52分)
-
20.有甲、乙兩位同學均想利用原電池反應檢測金屬的活動性順序,兩人均用鎂片和鋁片作電極,但甲同學將電極放入6mol/L的H2SO4溶液中,乙同學將電極放入6mol/L的NaOH溶液中,如圖所示。
(1)甲中SO42-移向(填“鋁片”或“鎂片”),寫出甲中正極的電極反應式。
(2)乙中負極為(填“鋁片”或“鎂片”)寫出其電極反應式:。
(3)鉛蓄電池中,正極材料為PbO2,負極材料為Pb,電解液為硫酸,放電時其正極反應式為。
(4)如圖為綠色電源“二甲醚(CH3OCH3)燃料電池”的工作原理示意圖,請寫出負極的電極反應式:。 組卷:5引用:1難度:0.6
組卷:5引用:1難度:0.6 -
21.某研究性學習小組設計了一組實驗驗證元素周期律。
Ⅰ.甲同學在a、b、c、d四只燒杯中分別加入50mL冷水,再各滴加幾滴酚酞試液,依次加入大小相近的鈉(Na)、鎂(Mg)、鋁(Al)、鉀(K)金屬塊,觀察現象。
(1)反應最劇烈的燒杯中金屬是。(填字母序號)
A.鈉
B.鎂
C.鋁
D.鉀
(2)實驗中發現b、c兩只燒杯中幾乎沒有什么現象,要想達到實驗目的,請你幫助選擇下列合適的方法。(填字母序號)
A.把鎂、鋁的金屬塊換成金屬粉末
B.把燒杯中的冷水換成熱水
C.把燒杯中的冷水換成鹽酸
D.把燒杯中的冷水換成氫氧化鈉溶液
Ⅱ.乙同學設計實驗探究碳、硅元素的非金屬性的相對強弱。根據要求完成下列各題
實驗裝置:(已知酸性強弱:亞硫酸>碳酸)
(3)銅與濃硫酸反應的化學方程式是;裝置E中酸性KMnO4溶液的作用是。
(4)能說明碳元素的非金屬性比硅元素非金屬性強的實驗現象是;試管F中發生反應的離子方程式為。組卷:29引用:1難度:0.6


