2021-2022學年重慶八中高二(上)期末化學試卷
發布:2024/12/24 1:0:2
一、選擇題(共42分,14個小題,每個小題只有一個答案符合題意)
-
1.下列現象或應用與電子躍遷無關的是( )
A.激光 B.焰色試驗 C.丁達爾效應 D.原子光譜 組卷:42引用:3難度:0.6 -
2.下列說法正確的是( )
A.CH4分子的球棍模型: 
B.基態氮原子的電子排布圖: 
C.鈹原子最外層的電子云圖: 
D.用原子軌道描述氫氣分子中化學鍵的形成:  組卷:2引用:1難度:0.6
組卷:2引用:1難度:0.6 -
3.下列物質發生變化時,所克服的粒子間相互作用屬于同種類型的是( )
A.液溴和碘分別受熱變為氣體 B.干冰和氯化銨分別受熱變為氣體 C.二氧化硅和氧化鈉分別受熱熔化 D.食鹽和氯化氫分別溶解在水中 組卷:113引用:2難度:0.3 -
4.肼(N2H4)是火箭燃料,發射時發生反應:2N2H4+2NO2=3N2+4H2O,以下有關該反應中涉及的四種物質的說法正確的是( )
A.N2和H2O都是非極性分子 B.N2H4分子中沒有孤電子對 C.H2O與NO2互為等電子體 D.該反應每當4molN-H鍵斷裂,則形成π鍵3mol 組卷:6引用:1難度:0.6 -
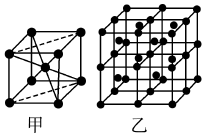 5.單質鐵的一種晶體如甲、乙所示,若按甲虛線方向切乙得到的圖應為( )
5.單質鐵的一種晶體如甲、乙所示,若按甲虛線方向切乙得到的圖應為( )A. 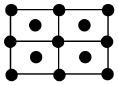
B. 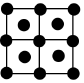
C. 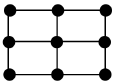
D. 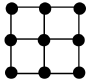 組卷:139引用:3難度:0.5
組卷:139引用:3難度:0.5 -
 6.圖1表示某種含氮有機化合物的結構,其分子內4個氮原子分別位于正四面體的4個頂點(見圖2),分子內存在空腔,能嵌入某離子或分子并形成4個氫鍵予以識別.下列分子或離子中,能被該有機化合物識別的是( )
6.圖1表示某種含氮有機化合物的結構,其分子內4個氮原子分別位于正四面體的4個頂點(見圖2),分子內存在空腔,能嵌入某離子或分子并形成4個氫鍵予以識別.下列分子或離子中,能被該有機化合物識別的是( )A.CF4 B.CH4 C. NH+4D.H2O 組卷:125引用:9難度:0.9
二、填空題(共58分,5個小題,按照題目要求填空)
-
18.釩、鎢、鋅在工業上用途廣泛。
(1)基態釩(V)元素在周期表中的位置為,其最高化合價為,與其同周期且未成對電子數相同的元素符號為。
(2)釩能形成多種配合物。釩的兩種配合物X、Y化學式均為V(NH3)3ClSO4,取X、Y的溶液進行如下實驗(已知配體難電離出來),所用試劑及所得現象如表所示:
則X的配離子為原溶液 X溶液 X溶液 Y溶液 Y溶液 所加試劑 BaCl2溶液 AgNO3溶液 BaCl2溶液 AgNO3溶液 現象 白色沉淀 無明顯變化 無明顯變化 白色沉淀 ,Y的配體為。
(3)NaxWO3是一類色彩豐富的非整比化合物,其晶體結構如圖2所示,若Na+無空缺,化學式為NaWO3,完全空缺則為WO3,每填入1個Na+,相應有1個W6+還原為W5+。NaxWO3的顏色與x值的對應關系如圖1所示,已知NaxWO3晶體中=n(W6+)n(W5+),則其顏色為23色。
(4)如圖3是金屬鎢晶體中的一個晶胞的結構模型(原子間實際是相互接觸的)。其中心的原子位于立方體的體心。實驗測得金屬鎢的半徑為rcm,假定金屬鎢為等直徑的剛性球,請回答以下各題:
①每一個晶胞中分攤到個鎢原子。
②計算晶胞的空間利用率(寫出表達式,不計算具體數值)。組卷:5引用:1難度:0.3 -
19.銅在我國有色金屬材料的消費中僅次于鋁,廣泛地應用于電氣、機械制造、國防等領域。回答下列問題:
(1)銅原子基態價電子排布式為;Cu2O和Cu2S都是離子晶體,兩種晶體熔點較高的是,原因是。
(2)氯和鉀與不同價態的銅(+1、+2)可生成兩種化合物,這兩種化合物都可用于催化乙炔聚合,其陰離子均為無限長鏈結構(如圖1所示),a位置上Cl原子的雜化軌道類型為;已知其中一種化合物的化學式為KCuCl3,另一種可能的化學式為。
(3)金屬銅單獨與氨水或單獨與過氧化氫都不能反應,但可與氨水和過氧化氫的混合溶液反應,其原因是,反應的化學反應方程式為。
(4)銅鎳合金的立方晶胞結構如圖2所示:
①原子B的分數坐標為;
②若該晶體密度為dg?cm-3,以NA表示阿伏加德羅常數,則銅鎳原子間最短距離為pm。組卷:7引用:1難度:0.3


